Навигация
Основы инженерной энзимологии
1.3 Основы инженерной энзимологии
Применение ферментов
Ферменты сохраняют свои уникальные свойства (эффективность, специфичность действия) и вне клеток, поэтому их традиционно широко применяют в практике. Биологические катализаторы нетоксичны, работают в мягких условиях, используют доступное сырье (в том числе и отходы), в связи с чем, их применение в промышленности выгодно с экономической и экологической точек зрения. По объему производства ферменты занимают третье место после аминокислот и антибиотиков. Из более чем 2000 известных в настоящее время ферментов в промышленности используется около 30.
Таблица 2. Применение ферментов
| Название фермента | Источники фермента | Химический и биологический процессы. Область использования. |
| Амилазы | Bacillus sp., Aspergillus niger | Гидролиз крахмала до декстринов, мальтозы и глюкозы. Спиртовая, пивоваренная промышленность, хлебопечение, получение патоки, глюкозы. |
| Глюкоизомераза | Более 80 видов микроорганизмов | Изомеризация D-глюкозы в D-фруктозу. Кондитерская, ликероводочная, безалкогольная промышленность, хлебопечение. |
| Глюкооксидаза | Penecillium chrysogenum, Aspergillus niger | Удаление кислорода и глюкозы (из яичного порошка, мясных и других продуктов). Виноделие, пивоваренная, консервная, соковая и безалкогольная промышленность. |
| Липазы | Поджелудочные железы животных, семена растений, микроорганизмы | Гидролиз жиров и масел. Пищевая, легкая, медицинская промышленность, сельское хозяйство, коммунальное хозяйство, бытовая химия. |
| Пектиназа | Многие микроорганизмы (Aspergillus ssp., Fusarium ssp.) | Гидролиз галактуронана, осветление вина и фруктовых соков. |
| Пептидогидролазы | Поджелудочные железы и слизистая желудка животных; плоды, побеги, отходы переработки некоторых растений (дынное дерево, инжир, ананас) | Лизис белка. Получение аминокислот, производство и получение сыра, мягчение мясных и рыбных изделий, выделка кожи, активизация пищеварения. Пивоварение, виноделие, хлебопечение, пищевая промышленность, сельское хозяйство, медицина. |
| Целлюлазы | Clostridium ssp., Aspergillus oryzae, Fusarium culmorum | Гидролиз целлюлозы до глюкозы. Производство пищевых и кормовых белковых препаратов, этанола, глюкозо-фруктозных сиропов. Спиртовая, пивоваренная, пищеконцентратная промышленность, хлебопечение, кормопроизводство. |
| Фруктофуранозидаза | Bacillus subtilis, E. coli, Streptococcus mutans | Инверсия сахарозы. Кондитерская, ликероводочная, безалкогольная промышленность, сиропопроизводство. |
Задачи инженерной энзимологии заключаются в развитии прогрессивных методов выделения ферментов, их стабилизации и иммобилизации; конструировании катализаторов с нужными свойствами и разработке научных основ их применения. В частности, методами белковой инженерии, сущность которых состоит в изменении первичной структуры природной молекулы фермента посредством химической модификации самого энзима или его гена, удается принципиально трансформировать структуру активного центра и его функцию, модулировать субстратную специфичность и физико-химические свойства фермента. Так, замена остатка глутамина-102 в молекуле лактатдегидрогеназы на аргинин превратила фермент в высокоактивную малатдегидрогеназу. Созданы гибридные формы ферментной системы, ценной в иммуноферментном анализе, сочетающие в себе свойства β-галактозидазы и β-галактокиназы. Важным этапом развития инженерной энзимологии стала разработка способов получения и использования иммобилизованных ферментов.
Иммобилизованные ферменты
Иммобилизованными ферментами называют ферменты, искусственно связанные с нерастворимым носителем, но сохраняющие свои каталитические свойства[7].
Ещё в 1916 г. Дж. Нельсон и Е. Гриффин показали, что сахараза, сорбированная на угле, сохраняла свою каталитическую активность, но лишь в 1953 г. Н. Грубхофер и Д. Шлейт впервые осуществили ковалентные связывания амилазы, пепсина, РНКазы и карбоксипептидазы с нерастворимым носителем. В 1971 г. на первой конференции по инженерной энзимологии был узаконен термин «иммобилизованные ферменты». Однако в понятие «иммобилизация» в настоящее время вкладывают более широкий смысл, чем связывание на нерастворимом носителе, а именно – полное или частичное ограничение движения белковых молекул.
Иммобилизованные ферменты имеют ряд преимуществ в сравнении со свободными молекулами. Прежде всего, такие ферменты, представляя собой гетерогенные катализаторы, легко отделяются от реакционной среды, могут использоваться многократно и обеспечивают непрерывность каталитического процесса. Иммобилизованные ферменты долговечны и в тысячи и десятки тысяч раз стабильнее свободных энзимов.
По Дж. Порату (1974), идеальные материалы, используемые для иммобилизации ферментов, должны обладать следующими основными свойствами: нерастворимостью; высокой химической и биологической стойкостью; значительной гидрофильностью; достаточной проницаемостью, как для ферментов, так и для коферментов, субстратов и продуктов реакции; способностью носителя легко активироваться (переходить в реакционноспособную форму). В зависимости от природы носители делятся на органические и неорганические материалы.
Иммобилизация многих ферментов осуществляется на полимерных носителях органической природы. Существующие органические полимерные носители можно разделить на два класса: природные и синтетические полимерные носители. Среди природных полимеров выделяют белковые, полисахаридные и липидные носители, а среди синтетических – полиметиленовые, полиамидные и полиэфирные.
К преимуществу природных носителей следует отнести их доступность, полифункциональность и гидрофильность, а к недостаткам – биодеградируемость и достаточно высокую стоимость. Из полисахаридов для иммобилизации наиболее часто используют целлюлозу, декстран, агарозу и их производные. Для придания химической устойчивости линейные цепи целлюлозы и декстрана поперечно сшивают эпихлоргидрином. Химической модификацией крахмала сшивающими агентами (формальдегид, глиоксаль, глутаровый альдегид) синтезирован новый носитель – губчатый крахмал, обладающий повышенной устойчивостью к гликозидазам. Из природных аминосахаридов в качестве носителей для иммобилизации применяют хитин. Среди белков практическое применение в качестве носителей нашли структурные протеины, такие, как кератин, фиброин, коллаген и продукт переработки коллагена – желатин.
К синтетическим полимерным носителям относятся полимеры на основе стирола, акриловой кислоты, поливинилового спирта; полиамидные и полиуретановые полимеры. Большинство синтетических полимерных носителей обладают механической прочностью, а при образовании обеспечивают возможность варьирования в широких пределах величины пор, введения различных функциональных групп.
В качестве носителей неорганической природы наиболее часто применяют материалы из стекла, глины, керамики, графитовой сажи, силикагеля, а также силохромы, оксиды металлов. Их можно подвергать химической модификации, для чего носители покрывают пленкой оксидов алюминия, титана, гафния, циркония или обрабатывают органическими полимерами. Основное преимущество неорганических носителей – легкость регенерации.
Существуют два принципиально различных метода иммобилизации ферментов: без возникновения ковалентных связей между ферментом и носителем (физические методы иммобилизации) и с образованием ковалентной связи между ними (химические методы иммобилизации).
При адсорбционной иммобилизации белковая молекула удерживается на поверхности носителя за счет электростатических, гидрофобных, дисперсионных взаимодействий и водородных связей. Адсорбция была первым методом иммобилизации ферментов (Дж. Нельсон, Э. Гриффин, 1916), но и сейчас не потеряла своего значения и стала наиболее широко распространенным способом получения иммобилизованных ферментов в промышленности. Процесс адсорбции ферментов достигается при контакте водного раствора фермента с носителем (статистическим способом, при перемешивании, динамическим способом с использованием колонок). К недостаткам адсорбционного метода следует отнести невысокую прочность связывания фермента с носителем. При изменении условий иммобилизации могут происходить десорбция фермента, его потеря и загрязнение продуктов реакции.
Способ иммобилизации ферментов путем включения в трехмерную структуру полимерного геля широко распространен благодаря своей простоте и уникальности. Метод применим для иммобилизации не только индивидуальных ферментов, но и мультиэнзимных комплексов и даже интактных клеток. Иммобилизацию ферментов в геле осуществляют двумя способами. В первом случае фермент вводят в водный раствор мономера, а затем проводят полимеризацию, в результате которой возникает пространственная структура полимерного геля с включенными в его ячейки молекулами фермента. Во втором случае фермент вносят в раствор уже готового полимера, который впоследствии переводят в гелеобразное состояние. Для первого варианта используют гели полиакриламида, поливинилового спирта, поливинилпирролидона, силикагеля, для второго – гели крахмала, агар-агара, каррагинана, агарозы, фосфата кальция. Метод непригоден для иммобилизации ферментов, действующих на водонерастворимые субстраты.
Сущность способа иммобилизации ферментов в полупроницаемые структуры заключается в отделении водного раствора фермента от водного раствора субстрата с помощью полупроницаемой мембраны, пропускающей низкомолекулярные молекулы субстратов и кофакторов, но задерживающей большие молекулы фермента. Разработано несколько модификаций этого метода, из которых интерес представляет микрокапсулирование и включение ферментов в липосомы. Первый способ предложен Т. Чангом в 1964 г. и состоит в том, что водный раствор фермента включается внутрь замкнутой микрокапсулы, стенки которой образованы полупроницаемым полимером. Один из механизмов возникновения мембраны на поверхности водных микрокапсул фермента заключается в реакции межфазной поликонденсации двух соединений, одно из которых растворено в водной, а другое – в органической фазе. Примером может служить образование на поверхности раздела фаз микрокапсулы, получаемой путем поликонденсации гексаметилендиамина – 1,6 (водная фаза) и галогенангидрида себациновой кислоты (органическая фаза).
nН2N(CH2)6NH2+nClC(O) (CH2)8C(O) Cl = (-NH(CH2)6NHC(O) (CH2)8C(O)-)n+2nHCl
К недостаткам метода следует отнести невозможность инкапсулированных ферментов осуществлять превращения высокомолекулярных субстратов.
Близким к инкапсулированию методом иммобилизации можно считать включение водных растворов ферментов в липосомы, представляющие собой сферические или ламеллярные системы двойных липидных бислоев. Впервые данный способ был применен для иммобилизации ферментов Дж. Вайсманом и Дж. Сессом в 1970 г. Для получения липосом из растворов липида (чаще всего лецитина) упаривают органический растворитель. Оставшуюся тонкую пленку липидов диспергируют в водном растворе, содержащем фермент. В процессе диспергирования происходит самосборка бислойных липидных структур липосомы, содержащих включенный раствор фермента. Ферменты, иммобилизованные путем включения в структуру липосом, используют преимущественно в медицинских и научных целях, ибо значительная часть ферментов в клетке локализована в составе липидного матрикса биологических мембран.
Иммобилизация ферментов путем образования новых ковалентных связей между ферментом и носителем – наиболее массовый способ получения промышленных биокатализаторов. В отличие от физических методов этот способ иммобилизации обеспечивает прочную и необратимую связь фермента с носителем и часто сопровождается стабилизацией молекулы энзима. Однако расположение фермента относительно носителя на расстоянии одной ковалентной связи создает стерические трудности в осуществлении каталитического процесса. Фермент отделяют от носителя с помощью вставки (сшивка, спейсер), в роли которой чаще всего выступают бифункциональные и полифункциональные агенты (бромциан, гидразин, сульфурилхлорид, глутаровый диальдегид и др.). Все методы химической иммобилизации классифицируют в зависимости от природы реакционной группы носителя, вступающей во взаимодействие с молекулой фермента.
1) Иммобилизация ферментов на носителях, обладающих гидроксогруппами.
Наиболее распространенным методом образования ковалентной связи между ферментом и полисахаридным носителем или синтетическим диольным соединением является бромциановый метод, который был предложен Р. Аксеном, Дж. Поратом и С. Эрнбаком в 1967 г. При обработке носителя бромцианом возникают реакционноспособные цианаты и имидокарбонаты, которые при взаимодействии с нуклеофильными аминогруппами фермента образуют производные изомочевины и уретанов.
Н-OH+BrCN = H-OCN+H2N-Ф=H-OC(NH) – NH-Ф
2) Иммобилизация ферментов на носителях, обладающих аминогруппами.
Первичные аминогруппы носителя, связанные с ароматическим кольцом, предварительно превращают в соли диазония, которые затем подвергают разнообразным реакциям сочетания. В реакции сочетания вступают фенольные, имидазольные, аминные, гуанидиновые, тиольные группы белков. Н-N2++H2N-Ф = H-N=N-NH-Ф+Н+
3) Иммобилизация на носителях, обладающих активированными производными карбоксильной группы.
Наиболее часто для соединения аминогрупп белка с ацильными группировками носителя используют ангидриды, галогенангидриды, активированные эфиры и другие производные карбоновых кислот.
Н-С(О) Cl+H2N-Ф = H-C(O) NH-Ф+НCl
4) Иммобилизация на носителях, обладающих сульфгидрильными группами.
Сульфгидрильные группы носителя и фермента легко окисляются с образованием дисульфидных связей под действием кислорода воздуха.
H-SH+0,5О2+HS-Ф = Н-S-S-Ф+Н2О
Наряду с иммобилизацией ферментов в последнее время все большее внимание уделяется иммобилизации клеток и субклеточных структур. Это объясняется тем, что при использовании иммобилизованных клеток отпадает необходимость выделения и очистки ферментных препаратов, применение кофакторов; создается возможность получения полиферментных систем, осуществляющих многостадийные непрерывно действующие процессы.
Промышленные процессы с использованием иммобилизованных ферментов и клеток
Получение глюкозофруктозных сиропов.
Первая промышленная установка для превращения глюкозы во фруктозу с помощью иммобилизованной глюкоизомеразы была запущена лишь в 1973 г. Исходным сырьем для этого процесса служит глюкоза, которую получают при гидролизе кукурузного или картофельного крахмала в присутствии минеральных кислот. Для конструирования промышленного биокатализатора глюкоизомеразу сорбируют на пористых неорганических носителях или ионообменных смолах. Возникающий в результате каталитического процесса глюкозофруктозный сироп содержит 42–45% фруктозы, около 51% глюкозы, небольшое количество олигосахаридов и по сладости соответствует инвертному сахару, получаемому при гидролизе сахарозы.
Получение L-аминокислот из их рацемических смесей.
Наряду с микробиологическими способами важное значение имеют химические методы промышленного получения природных аминокислот, в том числе незаменимых. Однако в результате химических реакций, используемых для синтеза аминокислот, содержащих асимметрические атомы углерода, с одинаковой скоростью образуются как D-, так и L-стереоизомеры, т.е. всегда возникает рацемическая смесь. Разделение рацемических смесей на составляющие их оптические изомеры (представляющее труднейшую задачу) явилось первым промышленным процессом с использованием иммобилизованных ферментов. Этот процесс был осуществлен в Японии в 1969 г.с помощью аминоацилазы, иммобилизованной на ДЕАЕ-целлюлозе. В качестве исходных соединений в данном превращении используют N-ацилированные производные D-, L – аминокислот, получаемые с помощью химического синтеза. Аминоацилаза гидролизует лишь N-ацил-L-стереоизомер, отщепляя от него ацильный радикал, в результате чего растворимость образующейся L-аминокислоты резко возрастает и ее легко можно отделить от своего антипода физико-химическими методами. При нагревании оставшаяся N-ацил-D-аминокислота рацемизируется, т.е. превращается в исходную смесь, которая вновь подвергается воздействию фермента.
Аминоацилаза строго специфична к структуре только ацильной части субстрата, поэтому одна и та же установка с иммобилизованным ферментом используется для получения различных аминокислот.
Получение L-аспарагиновой кислоты.
Аспарагиновая кислота широко употребляется в качестве пищевой добавки (подсластитель и подкислитель). Первая в мире промышленная установка для синтеза L-аспарагиновой кислоты из получаемого химическим путем фумарата аммония была запущена в 1973 г. в Японии. В ней использованы иммобилизованные в полиакриламидном геле клетки кишечной палочки E.coli, содержащие аспартат-аммиак-лиазу.
H4NOOC-CH=CH-COOH = HOOC-CH2-CH(NH2) – COOH
Получение L-аланина.
В настоящее время основной промышленный способ получения L-аланина – ферментативное декарбоксилирование L-аспарагиновой кислоты. Процесс превращения L-аспартата в L-аланин катализируется аспартат-β-декарбоксилазой ряда микроорганизмов (Pseudomonas dacunhae, Alcaligenes faecalis, Achromobacter pestifier), иммобилизованных в полиакриламидном геле.
HOOC-CH2-CH(NH2) – COOH = CH3-CH(NH2) – COOH+CO2
Усовершенствование процесса связано с использованием в качестве сырья фумарата аммония. В данном случае процесс получения L-аланина становится двустадийным и реализуется в двух последовательно расположенных колонках. На первом этапе фумарат аммония превращается в L-аспарагиновую кислоту, которая без выделения из реакционной среды на втором этапе претерпевает β-декарбоксилирование с образованием аланина.
Получение L-лизина
Процесс получения лизина основан на стереоспецефическом ферментативном гидролизе (конверсии) D-, L-α-амино-ε-капрлактама, который сначала получают химическим путём из циклогексена. Рацемат используют в качестве субстрата, который под действием лактамазы превращается в L-лизин, а непрореагировавшая D-форма переводится в смесь антиподов рацемазой. Лактамаза найдена у некоторых дрожжей (Candida laurentil). Рацемаза обнаружена у ряда бактерий (Alkaligenes obae).
Получение триптофана
Химико-ферментативный способ получения триптофана состоит в прямой конденсации индола, аммиака и ПВК. Реакцию катализирует пиридоксальзависимая триптофаназа. Фермент найден у E.coli.
Получение L-яблочной кислоты.
Яблочная кислота – заменитель лимонной в продуктах питания и лекарственных препаратах. Яблочную кислоту получают, используя иммобилизованные в полиакриламидном геле клетки, содержащие фумаратгидратазу. В присутствии этого фермента происходит присоединение воды по двойной связи в молекуле фумаровой кислоты.
HOOC-CH=CH-COOH+H2O = HOOC-CH(OH) – CH2-COOH
Перспективы технологии иммобилизованных ферментов[4]
Сегодня в промышленности реализовано всего четыре крупномасштабные технологии на основе иммобилизованных ферментов (глюкоизомеразы, аминоацилазы, пенициллазы и лактазы). В обозримом будущем иммобилизованные ферменты могут быть использованы для следующих целей.
1. Холинэстераза может применяться для определения пестицидов. Степень ингибирования этого фермента в присутствии пестицидов оценивают электрохимическими или колориметрическими методами.
2. Иммобилизованная диизопропилфторфосфатаза нервных клеток кальмара может найти применение для обезвреживания фосфорорганических нервных газов.
3. Иммобилизованная гепариназа может применяться для предотвращения тромбообразования в аппаратах искусственного кровообращения.
4. Предложен новый способ применения иммобилизованного гемоглобина. Включённый в полиуретановую матрицу белок образует «гемогубку», способную поглощать кислород прямо из воды с эффективностью 80%. Далее кислород высвобождается из полимера под действием слабого электрического разряда. Предполагается, что такая система может снабжать кислородом водолазов либо работающие под водой двигатели.
5. Возможно, вскоре удастся создать системы из нескольких иммобилизованных ферментов. Так, если заключить в микрокапсулы уреазу, глутаматдегидрогеназу и глюкозодегидрогеназу, то их можно будет использовать для удаления мочевины из крови больных с почечной недостаточностью.
6. Разнообразные иммобилизованные ферменты находят применение в датчиках быстрого анализа.
7. В последнее время большое внимание уделяется использованию различных микробных оксигеназных систем в стереоспецефическом эпоксиокислении олефинов.
1.5 Основы получения метаболитов
Процессами биотрансформации называют реакции превращения исходных органических соединений (предшественников) в целевой продукт с помощью клеток живых организмов или ферментов, выделенных из них.
По отношению к процессу роста низкомолекулярные продукты метаболизма живых клеток делятся на первичные и вторичные метаболиты. Первичные метаболиты необходимы для роста клеток. К ним относятся структурные единицы биополимеров – аминокислоты, нуклеотиды, моносахариды, а также витамины, коферменты, органические кислоты и другие соединения. Вторичные метаболиты (антибиотики, пигменты, токсины) – низкомолекулярные соединения, не требующиеся для выживания клеток и образующиеся по завершении фазы их роста.
Механизмы интенсификации процессов получения продуктов клеточного метаболизма
В норме обмен веществ в клетке осуществляется по принципам строжайшей экономии, что обеспечивается сложнейшей системой регуляции обмена веществ. Задача биотехнолога состоит в обеспечении сверхсинтеза одного из продуктов метаболизма, что достигается как путем изменения генетической программы организма, так и посредством нарушения регуляторных систем метаболизма в нем[7].
Для выделения из природных популяций высокопродуктивных штаммов микроорганизмов используют методы селекции, т.е. направленного отбора организмов со скачкообразным изменением геномов. Для возникновения мутаций интересующий ген должен удвоиться 106-108 раз. Более эффективен метод искусственного повреждения генома. Таким методом является индуцированный мутагенез, основанный на использовании мутагенного действия ряда химических соединений, рентгеновских и ультрафиолетовых лучей.
Координация химических превращений, обеспечивающая экономность метаболизма, осуществляется у микроорганизмов тремя основными механизмами: регуляцией активности ферментов, в том числе путем ретроингибирования; регуляцией объема синтеза ферментов (индукция и репрессия биосинтеза ферментов); катаболитной репрессией.
В процессе ретроингибирования (ингибирование по принципу обратной связи) активность фермента, стоящего в начале многоступенчатого превращения субстрата, тормозится конечным метаболитом, что детально разработано при изучении регуляции биосинтеза пиримидиновых нуклеотидов и новообразования ряда аминокислот.
На обмен веществ, аналогичный конечным метаболитам, оказывают эффект их аналоги. Для отбора объектов продуценты выращивают на селективной среде, содержащей подходящий аналог или антиметаболит, которые не включаются в обмен веществ (в частности, аналоги аминокислот не включаются в состав белков), что ведет к подавлению роста организма. Выжившие мутанты обладают дефектами в механизме регуляции активности фермента по принципу обратной связи и поэтому служат важными объектами в обеспечении сверхсинтеза целевого продукта.
Так, мутации по участкам цистрона, детерминирующим структуру аллостерического центра фермента, могут привести к изменениям в конформации белка, которые делают молекулу энзима нечувствительной к концентрации конечного продукта. Это обеспечивает возможность образования в клетке избыточного количества целевого продукта.
Мутации в гене-регуляторе проводят таким образом, чтобы его продукт – белок-репрессор – утрачивал способность связываться либо с индуктором, либо с оператором. В результате мутаций индуцибельные ферменты становятся конститутивными. Мутантные организмы, у которых изменены нуклеотидные последовательности в зоне гена-оператора, не могут связывать нормальный репрессор и также приобретают способность к конститутивной экспрессии структурных генов. Мутанты с дефектами регуляторной области оперона называются регуляторными. Из-за отсутствия или выключения фермента, катализирующего промежуточную стадию процесса, в среде накапливается не конечный продукт, а промежуточный целевой метаболит. Мутанты с ограниченной способностью к образованию конечных продуктов называются ауксотрофными.
Биотехнология получения первичных метаболитов
Производство аминокислот
Среди соединений, получаемых биотехнологическими методами, аминокислоты занимают первое место по объему производства и второе место по стоимости, уступая по последнему параметру лишь антибиотикам. Объем мирового производства аминокислот составляет более 500 тыс. т в год, из которых 300 тыс. т приходится на глутамат натрия, 100 тыс. т на лизин и 140 тыс. т на метионин.
В промышленных масштабах белковые аминокислоты получают:
1) гидролизом природного белоксодержащего сырья;
2) химическим синтезом;
3) микробиологическим синтезом;
4) биотрансформацией предшественников аминокислот с помощью микроорганизмов или выделенных из них ферментов (химико-микробиологический метод).
В ходе кислотного гидролиза белков происходят рацемизация и разрушение некоторых составляющих их аминокислот. При кислотном гидролизе полностью разрушается триптофан и достаточно значительны потери цистеина, метионина и тирозина (10–30%).
Существенный недостаток методов химического синтеза аминокислот состоит в получении целевых препаратов в виде рацемической смеси D- и L-стереоизомерных форм. Подавляющее большинство природных аминокислот относится к L-ряду. Исключением в этом отношении является лишь метионин, метаболизм которого нестереоизбирателен, благодаря чему данная аминокислота получается преимущественно путем химического синтеза.
Наиболее перспективен и экономически выгоден микробиологический синтез аминокислот. Более 60% всех производимых в настоящее время промышленностью высокоочищенных препаратов белковых аминокислот получают именно этим способом, главное преимущество которого в сравнении с методами химического синтеза состоит в возможности получения L-аминокислот на основе возобновляемого сырья.
Промышленное производство аминокислот стало возможным после открытия способности у некоторых микроорганизмов выделять в культуральную среду значительные количества какой-либо одной аминокислоты (С. Киносита, 1955). При этом было подмечено, что большинство из нескольких тысяч проанализированных диких штаммов микроорганизмов продуцировали аминокислоты во внешнюю среду, но в очень незначительных количествах. И лишь один из обследованных микроорганизмов – Corynebacterium glutamicum был способен к сверхсинтезу глутамата. Этот штамм использовали при организации первого в мире крупномасштабного производства глутаминовой кислоты микробиологическим способом в Токио (1956). Распространенные объекты селекции продуцентов – микроорганизмы, относящиеся к родам Brevibacterium, Microcjccus, Corynebacterium, Arthrobacter.
Производство лизина. В клетках микроорганизмов лизин синтезируется из аспарагиновой кислоты и служит конечным продуктом разветвленного метаболического пути биосинтеза, общего для трех аминокислот – лизина, метионина и треонина.
Эффекта накопления в среде всего одной целевой аминокислоты добиваются путем блокирования процессов, ведущих к синтезу побочных аминокислот, возникающих в связи с разветвлением метаболического пути. У типичных продуцентов L-лизина – Brevibacterium flavum и Corynebacterium glutamicum – фермент аспартаткиназа, открывающий метаболический путь, является аллостерическим белком, чувствительным к ингибированию по принципу обратной связи при совместном действии побочных продуктов L-треонина и L-лизина.
Чтобы добиться образования лизина в больших количествах, получают мутанты двух типов. У мутантов первого типа не синтезируется или не функционирует гомосериндегидрогеназа, в результате чего блокируется синтез метионина и треонина. Мутанты второго типа дефектны по структурному гену, детерминирующему конформацию аспартаткиназы. В итоге фермент теряет чувствительность к высоким концентрациям аллостерического ингибитора – лизина.
Производство триптофана. Подобно лизину триптофан образуется в ходе разветвленного метаболического пути, поэтому для его производства используют ауксотрофных мутантов, у которых блокированы реакции, ведущие к синтезу фенилаланина и тирозина. Однако при выращивании мутантных штаммов в среде с минимальной концентрацией этих аминокислот, не вызывающей регуляторных эффектов, избыточное накопление триптофана в среде не наблюдается, что объясняется особенностью процессов регуляции биосинтеза триптофана у микроорганизмов.
Триптофан оказывает ингибирующее действие на антранилатсинтетазу, поэтому для обхода метаболического контроля синтез фермента индуцируют ступенчатым введением предшественника – антраниловой кислоты:
В связи с этой особенностью промышленное производство триптофана организовано преимущественно по двухступенчатой схеме. На первом этапе химическим способом синтезируют антраниловую кислоту, которую с помощью энзиматической системы мутантных штаммов дрожжей Candida utilis переводят в триптофан.
Кроме триптофана микробиологическим способом с использованием предшественников получают гистидин, изолейцин, метионин, серин и треонин.
Для получения аминокислот – конечных продуктов неразветвленных метаболических путей, например аргинина, ауксотрофные мутанты не используют. В этом случае применяют мутанты с дефектами регуляции биосинтеза аминокислоты, т.е. регуляторные мутанты.
Производство витаминов
Благодаря изучению физиологии и генетики микроорганизмов – продуцентов витаминов и выяснению путей биосинтеза каждого из них создана теоретическая основа для получения микробиологическим способом практически всех известных в настоящее время витаминов. Однако с помощью энзимов целесообразнее производить лишь особо сложные по строению витамины: В2, В12, β-каротин (провитамин А) и предшественники витамина D. Остальные витамины либо выделяют из природных источников, либо синтезируют химическим путем.
Получение витамина В2 (рибофлавин). Вплоть до 30-х годов прошлого столетия рибофлавин выделяли из природного сырья. В наибольшей концентрации он присутствует в моркови и печени трески. Из 1 т моркови можно изолировать лишь 1 г рибофлавина, а из 1 т печени – 6 г. В 1935 г. обнаружен активный продуцент рибофлавина – гриб Eremothecium ashbyii, способный при выращивании на 1 т питательной смеси синтезировать 25 кг витамина В2. Сверхсинтеза рибофлавина добиваются действием на дикие штаммы мутагенов, нарушающих механизм ретроингибирования синтеза витамина В2, флавиновыми нуклеотидами. Отбор мутантов ведут по устойчивости к аналогу витамина В2 – розеофлавину.
В 1983 г. во ВНИИ генетики микроорганизмов сконструирован рекомбинантный штамм продуцента Bacillus subtilis, характеризующийся увеличенной дозой оперонов, которые контролируют синтез рибофлавина. Клонированием генов рибофлавинового оперона в одной из созданных плазмид был получен производственный штамм-продуцент витамина В2, способный синтезировать втрое большее по сравнению с E. ashbyii количество рибофлавина всего за 40 ч ферментации.
Получение витамина В12 (цианокобамид). Первоначально витамин В12 получали исключительно из природного сырья, но из 1 т печени можно было выделить всего лишь 15 мг витамина. Единственный способ его получения в настоящее время – микробиологический синтез. Обнаружение витамина в качестве побочного продукта при производстве антибиотиков в значительной степени стимулировало поиск организмов-продуцентов витамина и изучение путей его образования. Однако механизмы регуляции биосинтеза витамина В12 до настоящего времени полностью не расшифрованы. Известно, что при высоких концентрациях витамин полностью репрессирует синтез ключевых ферментов своего новообразования.
Продуцентами витамина В12 при его промышленном получении служат актиномицеты, метанобразующие и фотосинтезирующие бактерии, одноклеточные водоросли. В 70-х годах ХХ в. интерес ученых привлекли пропионовокислые бактерии, известные ещё с 1906 г. и широко использующиеся при приготовлении препаратов животноводства. Выделено 14 видов пропионовокислых бактерий, продуцирующих витамин В12.
Получение β-каротина и витамина D2. β-Каротин можно выделить из ряда растительных объектов – моркови, тыквы, облепихи, люцерны. В начале 60-х годов ХХ в. разработана схема микробиологического синтеза β-каротина, которая стала основой промышленного способа его получения. Установлено, что многие микроорганизмы – фототрофные бактерии, актиномицеты, плесневые грибы, дрожжи – синтезируют каротин. Характерно, что содержание β-каротина у микроорганизмов во много раз превышает содержание этого провитамина у растений. Так, в 1 г моркови присутствует всего 60 мкг β-каротина, в то время как в 1 г биомассы гриба Blaneslea trispora – 3–8 тыс. мкг.
Микробиологическим способом получают и витамин D2 (эргокальциферол), при производстве которого освоено дешевое сырье (углеводороды) и установлен стимулирующий эффект ультрафиолетовых лучей на синтез эргостерина культурой дрожжей.
Производство органических кислот
Получение лимонной кислоты. Лимонную кислоту широко используют в пищевой, фармацевтической и косметической промышленности. Ею заменяют фосфаты в составе детергентов, так как она полностью метаболизируется живыми организмами. Лимонная кислота образует хелаты с металлами, поэтому её применяют для их очистки. Объем мирового производства цитрата составляет 400 тыс. т/год. Производство лимонной кислоты принадлежит к числу старейших промышленных микробиологических процессов: оно было организовано в 1893 г.
Для промышленного производства лимонной кислоты используют главным образом культуру гриба Aspergillus niger. Метаболическим источником лимонной кислоты в организме служит цикл трикарбоновых кислот. Реакция образования лимонной кислоты, катализируемая цитратсинтазой, открывает цикл Кребса. Цитратсинтаза определяет скорость реакций, составляющих цикл Кребса. Активность фермента зависит от концентрации ЩУК, содержание которой может поддерживаться за счет функционирования конститутивной пируваткарбоксилазы, обеспечивающей переключение в аэробных условиях процессов гликолиза и глиоксилевого цикла. Скорость оборота цикла Кребса определяется поддержанием необходимого уровня окисленных форм коферментов дегидрогеназ, поэтому высокий выход цитрата получается лишь при условии хорошей аэрации. Дефицит фосфата ведет к сверхпродукции цитрата.
Одновременно с лимонной было налажено производство молочной кислоты при участии молочнокислых бактерий рода Lactobacillus.
С 20-х годов налажено промышленное производство D-глюконовой кислоты из глюкозы при участии A.niger. Глюконат натрия, в виде которого обычно выделяют глюконовую кислоту, используют для извлечения металлов, борьбы со ржавчиной, как моющее средство и в качестве медицинского препарата.
Производства, основанные на ацетон-бутанольном брожении и микробиологическая конверсия этанола в ацетат в настоящее время не рентабельны по экономическим соображениям.
Биотехнология получения вторичных метаболитов
Биосинтез вторичных метаболитов фазоспецифичен и происходит по завершении стадии роста, в идиофазе, благодаря чему их ещё называют идиолитами. Среди вторичных метаболитов ведущее место по объему производства занимают антибиотики.
Получение антибиотиков
Организация крупномасштабного производства антибиотиков сыграла решающую роль в становлении промышленной биотехнологии. К антибиотикам относятся низкомолекулярные эффекторы изначально природного происхождения, способные подавлять рост живых клеток. Способность нитчатого гриба зеленой плесени Penicillium notatum вызывать гибель микроорганизмов впервые была установлена в 1928 г. английским микробиологом А. Флеммингом. Однако лечебные свойства этой плесени были описаны ещё в 1871 г. русским дерматологом А.Г. Полотебновым. Количество открываемых антибиотиков постоянно растет. В 1940 г. было известно всего 6 антибиотиков, а в настоящее время описано более 12 000 аналогичных соединений, из которых в клинике применяют около 200 препаратов. 97% известных антибиотиков токсичны, поэтому в практике не используются. Изыскание новых антибиотиков обусловлено как потребностями практики, так и накоплением резистентных форм микроорганизмов по отношению ко многим антибиотикам.
Главное направление получения новых антибиотиков состоит в химической трансформации природных молекул для создания полусинтетических антибиотиков. Методы получения антибиотиков путем химического синтеза чрезвычайно сложны и не могут конкурировать с их биосинтезом методами биотехнологии. Направленный биосинтез антибиотиков осуществляется путем прямой ферментации микроорганизма – продуцента с подходящим предшественником, что индуцирует синтез ферментов вторичного метаболизма в идиофазе. Вводимый предшественник должен лимитировать скорость биосинтеза антибиотика. Например, производство бензилпенициллина в значительной степени стимулируется добавками его метаболического предшественника – фенилуксусной кислоты; пропионовая кислота и пропиловый спирт инициируют биосинтез макролидов через метилмалонилКоА; L-фенилаланин – предшественник фенилаланина – ускоряет образование грамицидина S. Аналогичный эффект вызывает использование ингибиторов метаболизма. Так, при подавлении процесса введения хлора микроорганизм S. aureofaciens образует тетрациклин, а не хлортетрациклин.
Другой способ получения антибиотиков состоит в использовании для их биосинтеза блокированных мутантов, у которых отсутствует (блокировано) определенное звено в цепи реакций, ведущих к синтезу антибиотика. Блокированные мутанты не способны образовывать нужный антибиотик. Используя низкую субстратную специфичность ферментов вторичного метаболизма и вводя аналоги предшественников антибиотика, последние переводят в аналоги самого антибиотика в ходе процесса, известного как мутационный биосинтез или мутасинтез. Так, мутанты Nocardia mtditerranei, у которых нарушена способность к ацилированию, образуют аналог предшественника рифамицина В-рифамицин SV.
Особенно успешны разработки в области биосинтеза полусинтетических пенициллинов и цефалоспоринов. Получение новых более эффективных аналогов пенициллина основано на изменении природы его ацильной группировки при сохранении в неизменном виде ядра пенициллина – 6-аминопенициллановой кислоты (6-АПК). В промышленности 6-АПК получают путем гидролиза природных пенициллинов с помощью специфического фермента – пенициллинацилазы. Некоторые из ацилаз способны катализировать и обратные реакции – процессы ацилирования аминогруппы 6-АПК с образованием модифицированного пенициллина. Таким путем было получено более 4000 полусинтетических пенициллинов.
Получение промышленно важных стероидов
Способность клеток микроорганизмов к сложнейшим процессам биотрансформации наиболее полно реализовалась при получении промышленно важных стероидов. Биотрансформация стероидов обычно заключается в селективном воздействии на одно из положений стероидного скелета. Первый промышленный процесс (1937 г.) микробной биотрансформации стероидов основывался на технологии направленного гидроксилирования (11-α-гидроксилирование) прогестерона.
Важнейший источник стероидных гормонов (эндостраны и эстраны) – культура клеток растений. Так, культура клеток диоскореи дельтовидной (Dioscorea deltoidea) корневого происхождения продуцирует фитостерин диосгенин и его гликозидные производные (сапонины). Дальнейшие успехи в производстве стероидных препаратов связывают с применением иммобилизованных клеток.
Похожие работы
... весь цилиндр. Это опыт демонстрирует одну из биологических функций железа. По химической природе, каталаза – геминовый фермент, содержащий железо. [3] 2. Разработка темы «Основания» в курсе неорганической и органической химии 2.1 Урок по теме «Основания» Цели урока: познакомить учащихся с новым классом химических соединений – основаниями, их свойствами (отношение к воде, действие на ...
... области создания новых конструкционных материалов с заданными химическими и физическими свойствами. Обсудить возможности и перспективы синтеза таких материалов на основе органических и неорганических полимеров. Прикладная химия неотделима и от социально-бытовой сферы общества. В лекциях необходимо знакомить студентов с областями применения продуктов химических производств. Это расширит кругозор ...
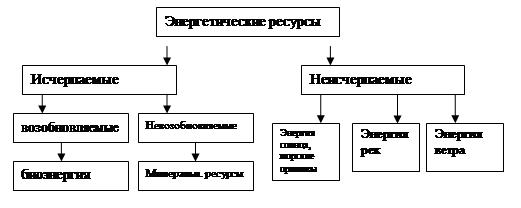
... период многие страны приняли решение о полном или постепенном отказе от развития атомной энергетики. 1.3 Особенности альтернативной водородной энергетики Водородная энергетика включает следующие основные направления: Разработка эффективных методов и процессов крупномасштабного получения дешевого водорода из метана и сероводородсодержащего природного газа, а также на базе разложения воды; ...
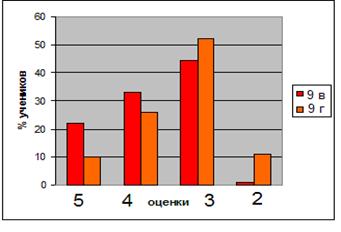
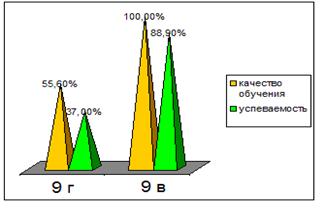
... экспериментальной площадки был выбран 9 А класс. В этом классе 29 человек: 17 мальчиков и 12 девочек. Цель эксперимента: выявление психолого-педагогических условий профессионального самоопределения учащихся в процессе обучения биологии; а также формирование устойчивой положительной мотивации к изучению курса биологии и развитие профессионального самоопределения учащихся при изучении курса “Общая ...

0 комментариев