Навигация
6. Практическая часть
6.1 Вопросы
Каким правилом выражается связь между числом степеней свободы, числом фаз и числом компонентов в гетерогенной системе?
Дать понятия: гетерогенная система, фаза, составляющее вещество системы.
С помощью какого уравнения выражается связь между основными термодинамическими параметрами однокомпонентной двухфазной системы, находящейся в состоянии равновесия? Вывести это уравнение.
Свяжите составы жидкости и ее пара с общим давлением и парциальным давлением пара.
Интерпретируйте диаграмму температура – состав и используйте для ее определения поведение смеси при дистилляции.
Справедливо ли уравнение Клапейрона – Клаузиуса для фазовых переходов между твердым и газообразным агрегатными состояниями вещества? Аргументируйте свой ответ.
Что характеризует число степеней свободы равновесной термодинамической системы?
Сформулируйте основной закон фазового равновесия. Как классифицируются системы?
Охарактеризуйте однокомпонентные гетерогенные системы. Диаграмма состояния воды. Кстати, что такое фазовая диаграмма?
Что такое моно- и энантиотропные фазовые переходы? Охарактеризовать каждый из них.
6.2 Задачи
Температура кипения ртути под нормальным атмосферным давлением 357![]() . Теплота парообразования 283,2 Дж/г. Определить изменение упругости пара ртути при изменении температуры на 1
. Теплота парообразования 283,2 Дж/г. Определить изменение упругости пара ртути при изменении температуры на 1![]() вблизи температуры кипения ртути под нормальным атмосферным давлением.
вблизи температуры кипения ртути под нормальным атмосферным давлением.
Решение: используем формулу ![]() откуда
откуда
![]() ,
,
где ![]() - мольная теплота испарения. Находим
- мольная теплота испарения. Находим
![]() ; Т=630К
; Т=630К ![]() .
.
Давление паров воды при 97![]() равно 90919,9
равно 90919,9 ![]() , а при 103
, а при 103![]() 112651,8
112651,8![]() . Определить давление паров воды при 110
. Определить давление паров воды при 110![]() (Р110).
(Р110).
Решение: Из формулы
![]() ,
,
где ![]() - упругости паров, рассчитаем
- упругости паров, рассчитаем ![]() .
.
![]()
![]()
![]()
Определим ![]() , используя полученное значение
, используя полученное значение ![]() и
и ![]() при
при ![]() (К).
(К).
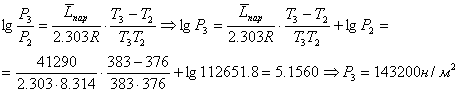
Сравним с табличной величиной ![]() .
.
3. Удельная теплота плавления нафталина при его нормальной температуре плавления 79,9![]() равна 149,25 Дж/г. Разность удельных объемов в жидком и твердом состояниях при температуре плавления
равна 149,25 Дж/г. Разность удельных объемов в жидком и твердом состояниях при температуре плавления ![]() 0,146
0,146![]() . Определить изменение температуры плавления нафталина при увеличении давления в 100 раз по сравнению с нормальным атмосферным давлением (101,325
. Определить изменение температуры плавления нафталина при увеличении давления в 100 раз по сравнению с нормальным атмосферным давлением (101,325![]() ).
).
Решение: Используя уравнение ![]() , т.к. давление дано в
, т.к. давление дано в ![]() , то изменение удельного объема нужно выразить в
, то изменение удельного объема нужно выразить в ![]() , а теплоту плавления в Дж/кг. Поскольку
, а теплоту плавления в Дж/кг. Поскольку ![]() - разность удельных объемов, то вместо мольной теплоты плавления можно взять удельную теплоту плавления (Дж/кг).
- разность удельных объемов, то вместо мольной теплоты плавления можно взять удельную теплоту плавления (Дж/кг).
![]()
Изменение температуры плавления ![]() при увеличении давления в 100 раз по сравнению с нормальным атмосферным давлением (т.е. при 1,013
при увеличении давления в 100 раз по сравнению с нормальным атмосферным давлением (т.е. при 1,013![]()
![]() )=3,453
)=3,453![]()
![]() =3,5
=3,5![]() .
.
4. Докажите, что на диаграмме “давление – температура” линии равновесия жидкость – пар в однокомпонентной системе всегда должна иметь положительный наклон.
Решение:
![]()
![]() и
и ![]() , поэтому
, поэтому
![]()
5. Как изменится точка кипения воды (100![]() ) при изменении атмосферного давления на 1 мм рт.ст.? При 100
) при изменении атмосферного давления на 1 мм рт.ст.? При 100![]() и 1 атм. теплота испарения воды 539,7
и 1 атм. теплота испарения воды 539,7 ![]() , мольный объем жидкой воды 18,78 мл, мольный объем пара 30,19 литров.
, мольный объем жидкой воды 18,78 мл, мольный объем пара 30,19 литров.
Решение:
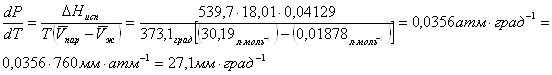
Отсюда![]() .
.
6. Плотность твердого фенола 1072 ![]() , жидкого 1056
, жидкого 1056 ![]() , теплота его плавления 1,044
, теплота его плавления 1,044![]() Дж/кг, температура замерзания 314,2 К. Вычислите dP/dT и температуру плавления фенола при 5,065
Дж/кг, температура замерзания 314,2 К. Вычислите dP/dT и температуру плавления фенола при 5,065 ![]() Па.
Па.
Решение: по уравнению Клапейрона – Клаузиуса рассчитываем dP/dT:

Чтобы вычислить температуру плавления при заданном внешнем давлении, принимаем, что dT/dP в интервале давлений 1,0132![]() -5,065
-5,065![]() Па – величина постоянная, равная 4,214
Па – величина постоянная, равная 4,214![]() К/Па. Тогда
К/Па. Тогда
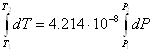 и
и ![]() .
.
Похожие работы
... MnY2S4 и фазы MgLn4S7 моноклинной сингонии. Условие существования фаз, характер плавления не известны. Ограниченность и неполнота литературных данных определяет актуальность задачи изучения фазовых равновесий в системе MgS – Y2S3. Глава 2. Методическая часть. 2.1. Методы физико-химического анализа Исходя из свойств полуторных сульфидов, таких, как термическая стабильность, летучесть, и ...
... Точками области 1 соответствует газообразное, области 2 - жидкое, области 3 - твердое состояние вещества. Плоскость ТР с указанными тремя кривыми равновесия называется диаграммой состояния. Диаграмма состояния позволяет судить, какие будут происходить фазовые превращения при том или ином процессе. Допустим, например, что производится нагревание при постоянном давлении. На диаграмме состояния такой ...
... равны удельным значениям энтропии, взятой с обратным знаком, и объеме: (4.30) Если в точках, удовлетворяющих фазовому равновесию: , первые производные химического потенциала для разных фаз испытывают разрыв: , (4.31) говорят, что термодинамическая система испытывает фазовый переход I-го рода. Для фазовых переходов первого рода характерно наличие срытой теплоты фазового перехода, ...
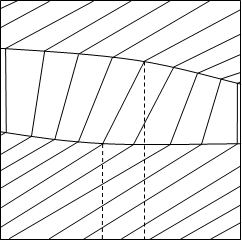
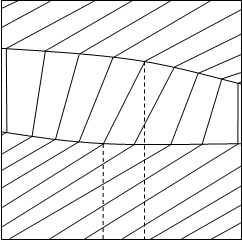
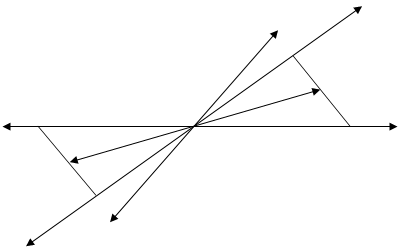
... как в азеотропных смесях коннода вертикальна, нода вырождается в точку. 3. Фазовые эффекты и уравнение Ван-дер-Ваальса для бинарных азеотропных смесей. Фазовые эффекты в бинарных азеотропных смесях. На рисунках 3.1 - 3.4 изображены диаграммы объем - состав фаз, и энтропия – состав фаз для азеотропа с минимумом температуры кипения. Если рассматриваемый состав равен составу ...
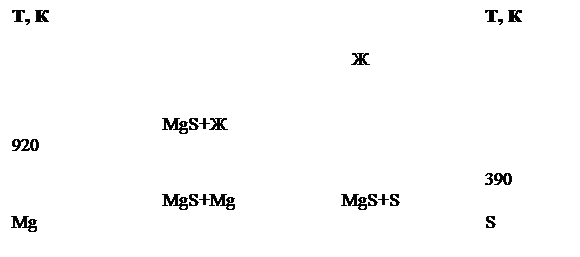

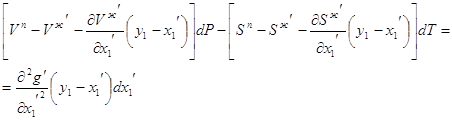
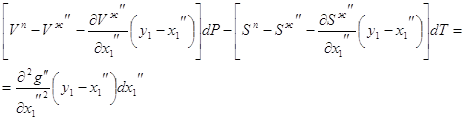
0 комментариев