Навигация
Общие сведения о перегруппировке
1. Общие сведения о перегруппировке.
Перегруппировка Арбузова- это превращение полных эфиров кислот трехвалентного Р под действием алкилирующих или арилирующих реагентов в фосфорильные соединения с образованием связи С-Р.
Перегруппировка Арбузова является нуклеофильной, интрамолекулярной, протекает без изомеризации, с миграцией от атома улерода к атому кислорода в алифатических системах, не стереоспецифическая.
2.Механизм перегруппировки.
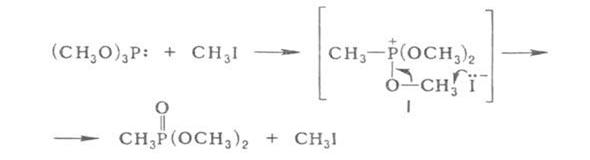
1 1.На первой стадии происходит органического галогенида к эфиру трехвалентного фосфора с образованием промежуточного квазифосфониевого соединения типа (1). Первая стадия_ бимолекулярное, нуклеофильное замещение второго порядка.
2Далее происходит разрыв связи углерода с кислородом с образованием эфира фосфористой кислоты и галогеналкила.
3.Влияние структуры исходного эфира трехвалентного фосфора и галогенсодержащего реагента на легкость (и возможность) протекания перегруппировки.
В процессе длительного изучения реакций Арбузова были сформулированы обобщения, связывающие влияние структуры исходного эфира трехвалентного фосфора и галогенсодержащего реагента на легкость (и возможность) протекания между ними реакции. Активность производного трехвалентного фосфора зависит от величины электронной плотности (подвижности неподеленной электронной пары) на атоме фосфора. Электронодонорные заместители у атома фосфора, увеличивая электронную плотность на нем, повышают реакционную способность этих соединений с галогенсодержащими соединениями, относящимися к группе электрофильных реагентов. Электроноакцепторные заместители, снижая электронную плотность на атоме фосфора, будут затруднять протекание реакции. В некоторых случаях низкую активность эфира трехвалентного фосфора в реакции Арбузова можно компенсировать повышенной активностью галогенопроизводного.
Если в производном P(III) наряду с атомом фосфора имеется еще один центр алкилирования, реакция протекает неоднозначно. Так, в случае тиоэфиров Р(III) взаимодействие с галоидными алкилами осуществляется в двух направлениях: по схеме реакции Арбузова и с замещением алктиольной группы у трехвалентного фосфора на атом галогена. Это объяснялось возможностью конкурирующего алкилирования атомов фосфора и серы на первой стадии реакции
В течение нескольких десятков лет в литературе дискутировался вопрос о соотношении этих направлений. По последним данным превалирует направление по схеме реакции Арбузова, тогда как направление с сохранением координации атома фосфора является незначительным.
4.Различные продукты реакции, образующиеся при использовании разных реагентов.
Если вводимый в реакцию алкилгалогенид идентичен образующемуся, его берут в каталитических количествах, в других случаях - в избытке.
В реакцию вступают фосфиты (R'O)3P, фосфониты RP(OR')2, фосфиниты R2P(OR'), а также их производные, содержащие хотя бы одну группу OR'. Заместители у атома Р, понижающие его нуклеофильность, уменьшают реакц. способность соединения. Так, галогенфосфиты реагируют обычно только в присутствии кислот Льюиса. Ариловые эфиры вступают в реакцию с трудом, при этом удается выделить промежуточно образующееся квазифосфониевое соединение типа I.
Триметилфосфит и другие метиловые эфиры в присутствии кислот Льюиса дают те же продукты, которые образовались бы в реакции Арбузова, например:
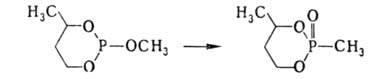
В качестве алкилирующих и арилирующих агентов в реакции Арбузова могут участвовать алкил- и алкиленгалогениды, галогенпроизводные гетероциклические соединения, галогенкарбонильные соединения, ангидриды карбоновых кислот. При применении галогенарилов и галогенгетероциклических соединений реакцию Арбузова обычно проводят в условиях фотохимической активации (через стадию образования комплекса с переносом заряда).
Винилгалогениды вступают в реакцию Арбузова с трудом, однако в этом случае реакция катализируется NiCl2, что позволяет получать некоторые винилфосфорильные соединения. Для синтеза соединения, содержащих алкильные заместители в![]() положении, используют реакцию триалкилфосфитов с 1-нитро-1-алкеном:
положении, используют реакцию триалкилфосфитов с 1-нитро-1-алкеном:
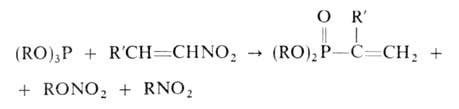
Геминальные и другие дигалогеналканы в зависимости от соотношения реагентов образуют различные соединения:
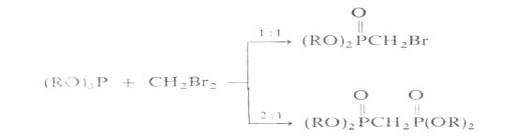
Четыреххлористый углерод образует как трихлорметильные фосфорильные соединений [например, (RO)2P(O)CC13], так и дихлорметилендифосфорильные [напр., (RO)2P(O)—CC12—(O)P(OR)2]; реакция ускоряется пероксидами или УФ-облучением.
Вицинальные галогенпроизводные, содержащие хотя бы у одного атома С два электроноакцепторных заместителя, с полными фосфитами реагируют не по схеме реакции Арбузова:
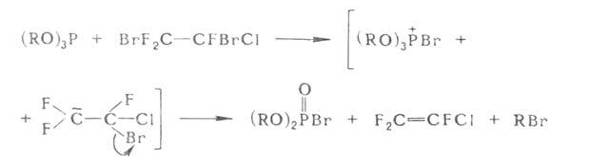
Перфторолефины взаимод. с триалкилфосфитами с образованием в качестве промежуточных соединений фосфоранов:
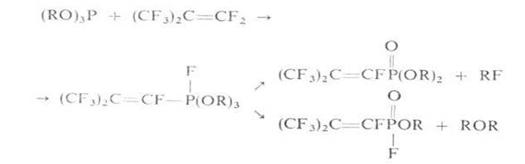
Реагенты, молекулы которых содержат электрофильные атомы Н, Hal, S, N и другие, вступают в реакции, родственные реакции Арбузова , в этом случае связь С—Р не образуется, например:
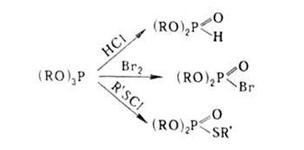
Полные тиолфосфиты обычно взаимодействуют с алкилгалогенидами и галогенациламинами не по схеме реакции Арбузова . Промежуточно здесь образуются не квазифосфониевые, а квазисульфониевые соединения, распадающиеся до галогентиофосфитов, например:
![]()
Реакции Арбузова широко используют для получения соединений со связью С—Р, в том числе пестицидов, лекарственных препаратов, экстрагентов и др. Реакция открыта А. Е. Арбузовым в 1905.
5.Возможность протекания перегруппировки по другому направлению.
В некоторых случаях гомолитический механизм может направлять процесс по схеме реакции Арбузова, тогда как в обычных условиях взаимодействие протекает в другом направлении. Так, хлорацетон как a-галогенкарбонильное соединение в обычных условиях реагирует с триалкилфосфитами по схеме реакции Перкова с образованием диалкилизопропенилфосфата. При фотолизе смеси хлорацетона с триалкилфосфитом протекает реакция Арбузова с образованием ацетонилфосфоната.
Это еще один удачный пример применения гомолитической реакции Арбузова для синтеза функционально замещенных фосфорорганических соединений.
Галоген альдегиды и![]() галогенкетоны в зависимости от строения реагентов и условий протекания реакции образуют винилфосфаты (Перкова реакция)или
галогенкетоны в зависимости от строения реагентов и условий протекания реакции образуют винилфосфаты (Перкова реакция)или![]() кетофосфонаты:
кетофосфонаты:
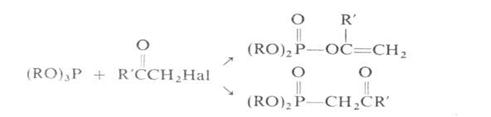
Ацилгалогениды в р-ции с триалкилфосфитами образуют![]() кетофосфонаты
кетофосфонаты
Выводы
Таким образом, универсальность реакции Арбузова (как ее классического варианта, так и новых видов) состоит в том, что она может быть осуществлена с широким выбором электрофильных реагентов в условиях гетеро- и гомолитического взаимодействия. Не исключается возможность протекания реакции по двум механизмам в одном процессе. Предпочтение тому или иному варианту реакции Арбузова отдают с учетом конкретных препаративных целей. Эта реакция принесла всемирное признание ее автору, дала ключ к пониманию структуры органических соединений фосфора и тем самым подтвердила плодотворность основных положений теории химического строения А.М. Бутлерова.
Значение новых идей в науке проверяется временем. Прошедшие десятилетия не состарили реакцию Арбузова. Наоборот, в химии фосфорорганических соединений, которая своим становлением и развитием во многом обязана этой реакции, в настоящее время нет другого столь универсального метода синтеза. И хотя химия органических соединений фосфора располагает широким арсеналом синтетических методов (в том числе и приводящих к образованию новых фосфоруглеродных связей), тем не менее реакция Арбузова продолжает оставаться важнейшей.
Реакция Арбузова позволяет вводить фосфорсодержащий заместитель с различным числом фосфоруглеродных связей в другие органические молекулы. Можно сказать и по-другому: с помощью этой реакции мы получаем возможность вводить к атому фосфора самые различные фрагменты органических молекул. Если же в последних имеются функциональные группы или кратные связи, то такие соединения могут явиться исходными для дальнейших синтезов. Направления дальнейших химических превращений будут определяться природой функциональных групп, фосфорсодержащего заместителя и их взаимным влиянием. Вот в чем уникальность и неисчерпаемые синтетические возможности реакции Арбузова.
Перегруппировка Виттига.
1.Общие сведения о перегруппировке.
Перегруппировка Виттига заключается в превращении простых эфиров при металлировании или другом аналогичном воздействии в спирты с перемещением одной алкильной группы в a - положение другой. Только такие группы, как бензил или аллил, образующие достаточно устойчивые анионы, т.е. способные легко подвергаться металлированию, вызывают миграцию.
Приведем пример:
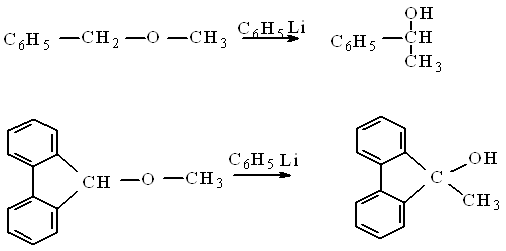
Перегруппировка Виттига является электрофильной,внутримолекулярной, стереоспецифической, протекает без изомеризации, с миграцией от атома углерола к другому атому углерода в насыщенных системах.
2.Механиз перегруппировки.
1.Перегруппировка Виттига происходит в результате обработки эфиров фениллитием. Первая стадия процесса состоит в замещении a - водородного атома бензильной или другой реакционноспособной алкильной группы на литий. (см. Схему перегруппировки стадия I)
2.Виттиг предположил, что в металлическом производном либо уже имеется, либо легко образуется карбанион, к отрицательному центру, которого перемещается в виде электрофильного остатка другая алкильная группа, имеющая только шесть электронов в оболочке с главным квантовым числом 2. (см. Схему перегруппировки стадия II)
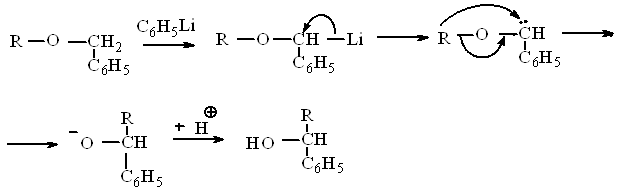
3.Доказательства механизма перегруппировки и ее стереоспецифичности.
Хаузер и Кантор проводили эту же реакцию путем обработки эфиров амидом калия в жидком аммиаке с последующим добавлением этилового эфира. Условия этой реакции соответствуют предложенному Виттигом механизму реакции. Были получены некоторые качественные данные по относительным скоростям миграции различных алкильных групп. В случае 9-флуорениловых эфиров Виттиг наблюдали следующую последовательность скоростей: аллил, бензил> метил, этил> фенил. Из исследования Хаузера и Кантора следует, что втор-бутил> трет–бутил. Тот факт, что в ряду простых ненасыщенных алкильных групп неопептильная и трет-бутильная группы обладают относительно низкими скоростями миграции, указывает на согласованное изменение связей с мигрирующей группой. Мигрирующая группа перемещается от ониевого атома к углеродному атому, т.е. от центра, предрасположенного к потере катиона, к углеродному центру, способному сохранять отрицательный заряд и реагировать в форме аниона, это доказывает механизм реакции. Причем при введении в систему щелочи, скорость увеличивается, т.е. при наличии щелочи полностью образуется анионный центр,- это подтверждает двух стадийный механизм реакции. Это же может служить доказательством стереоспецифичности перегруппировки.
Похожие работы
... которых можно осуществить превращения:→ 3.1. этанол → бутадиен-1,3 → бутадиеновый каучук 3.2. 2-метилбутан → изопрен → цис-полиизопрен ГЛАВА IV. ТЕСТЫ И ЗАДАЧИ ПО ТЕМЕ «НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ» Задачи 1. При пропускании 11,2 л (н.у.) смеси этана, этилена и ацетилена через склянку с бромной водой масса склянки увеличилась на 10,9 г. При пропускании исходной ...
... в химию магнитные взаимодействия. Будучи пренебрежимо малыми по энергии, магнитные взаимодействия контролируют химическую реакционную способность и пишут новый, магнитный «сценарий» реакции. Дизайн молекулярных магнетиков — одно из новых научных направлений современной химии, связанное с синтезом систем высокой размерности. Сегодня достижения современной химии таковы, что химики могут ставить ...
... новые возможности, которые возникали с появлением новых методов исследования, позволяли делать открытия, радикально менявшие взгляды на патологию, начинать качественно новые этапы её развития. Патологическая анатомия использует три основных метода исследования — вскрытие трупов людей, умерших от болезней (1); микроскопические методы изучения тканей (2); эксперимент, позволяющий моделировать на ...
... М., 1976; Система, структура и процесс развития международных отношений / Отв. ред. В.И. Ганпман. — М., 1984. 17. См., например: Антюхчна-Московченко В.И., Злобин А.А., Хруста-лев М.А. Основы теории международных отношений. — М., 1988, с. 68. 18. Возе К. 5осю1ое1е (1е 1а ра1х. — Рапа, 1965, р. 47—48. 19. ВгаШаг<1 РН., Д/аИН М.-К. Ьех ге1аиоп5 т1етайопа1е&. — Рапа, 1988, р. 65-71. 20. ...

0 комментариев