Навигация
5. Аппарат трансляции
Основными участниками процесса считывания информации, закодированной в последовательности мРНК, являются аминоацил-тРНК-синтетазы, тРНК, рибосомы, белки, связанные с рибосомами, и некоторые другие белки. Они ответственны за инициацию, элонгацию и терминацию сборки полипептида. В этом разделе мы опишем свойства каждого из перечисленных компонентов, а в следующем обсудим, как они функционируют на разных этапах процесса трансляции.
а. Присоединение аминокислот к «родственным» тРНК
Функционирование тРНК при трансляции сводится к двум уникальным процессам. Первый из них состоит в присоединении аминокислоты к 3'-концу родственной тРНК с помощью специфической аминоацил-тРНК-синтетазы, второй – в специфическом связывании аминоацил-тРНК с соответствующим кодоном мРНК, находящейся в комплексе с рибосомой. Ключевой особенностью обеих реакций является их специфичность, поскольку сбои в образовании аминоацил-тРНК или связывании аминоацил-тРНК с соответствующим кодоном приведут к ошибкам в экспрессии генов. Поэтому очень важно понять природу такой специфичности, механизм ее обеспечения и последствия нарушений точности на этих двух этапах трансляции.
Основные особенности структуры тРНК. В любой клетке присутствует очень много разных тРНК. Молекула тРНК состоит обычно из 75–85 нуклеотидов и содержит уникальный тринуклеотид, который определяет, какую аминокислоту эта тРНК присоединяет и с каким кодоном она может спариться. На основании данных о нуклеотидной последовательности более чем 150 отдельных видов тРНК, выделенных из клеток про- и эукариот, были построены компьютерные модели внутримолекулярного комплементарного спаривания оснований в молекуле тРНК. Был сделан вывод, что практически все тРНК, независимо от их нуклеотидной последовательности, обладают характерной вторичной структурой, которую называют структурой «клеверного листа» из-за наличия в ней трех шпилек. Реальность предсказанной структуры была подтверждена данными о разной химической чувствительности оснований, одни из которых спарены, а другие нет.
Большинство молекул тРНК, имеющих форму клеверного листа, содержат четыре области, каждая из которых обладает инвариантными свойствами независимо от аминокислотной специфичности тРНК. 1. На 3'-конце молекулы всегда находятся четыре неспаренных нуклеотида, причем три из них–это обязательно ССА. 5'- и 3'-концы цепи РНК образуют акцепторный стебель. Цепи удерживаются вместе благодаря комплементарному спариванию семи нуклеотидов 5'-конца с семью нуклеотидами, находящимися вблизи 3'-конца. 2. У всех молекул имеется шпилька РфС, обозначаемая так потому, что она содержит два необычных остатка: риботимидин и псевдоуридин). Шпилька состоит из двухцепочечного стебля из пяти спаренных оснований, включая пару G-C, и петли длиной семь нуклеотидов. Тринуклеотид Т всегда расположен в одном и том же месте петли. В антикодоновой шпильке стебель всегда представлен семью спаренными основаниями. Триплет, комплементарный родственному кодону, – антикодон – находится в петле, состоящей из семи нуклеотидов. С 5'-конца антикодон фланкируют инвариантный остаток урацила и модифицированный цитозин, а к его 3'-концу примыкает модифицированный пурин, как правило аденин. 4. Еще одна шпилька состоит из стебля длиной три-четыре пары нуклеотидов и петли варьирующего размера, часто содержащей урацил в восстановленной форме – дигидроурацил.
Наиболее сильно варьируют нуклеотидные последовательности стеблей, число нуклеотидов между антикодоновым стеблем и стеблем ТфС, а также размер петли и локализация остатков дигидроурацила в DU-петле.
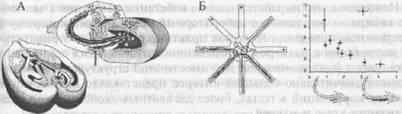
Рентгеноструктурный анализ некоторых молекул тРНК позволил выявить их характерную четвертичную структуру. Эта структура более компактна, чем структура «клеверного листа». Она образуется благодаря внутримолекулярным взаимодействиям, сближающим DU- и Т| С-шпильки. В результате молекула тРНК выглядит так, как будто она состоит из двух взаимно перпендикулярных частей – в одной из них находится акцепторный участок, в другой – антикодон. Из-за такого общего вида молекулы структура получила название L-конфигурации. L-структура представляется более адекватной, чем «клеверный лист», особенно если учесть, что тРНК играет роль адаптора при взаимодействии кодона и антикодона на рибосоме.
Обычно акцепторами для одной и той же аминокислоты служат несколько разных тРНК, имеющих разные антикодоны, что позволяет им спариваться с кодонами-синонимами. Отчасти этим объясняется и вырожденность кода, т.е. способность разных антикодонов детерминировать одну и ту же аминокислоту.
Этерификация молекул тРНК. Для выполнения функции адаптора в процессе трансляции мРНК тРНК должна связаться с аминокислотой, соответствующей своему антикодону. Это происходит в результате АТР-зависимой реакции, катализируемой специфическими ферментами аминоацил-тРНК-синтетазами. В ходе реакции АТР расщепляется на 5'-адениловую кислоту и неорганический фосфат, а высвобождаемая при этом энергия используется для присоединения карбоксильной группы аминокислоты к одной из гидроксильных групп рибозы на 3'-конце тРНК. На самом деле образование аминоацил-тРНК проходит в два этапа. На первом этапе карбоксильная группа аминокислоты присоединяется к а-фосфату АТР, что сопровождается высвобождением неорганического фосфата и образованием аминоацил-аденилата. Аминоацил-аденилат обладает очень высокой реакционной способностью и стабилизируется благодаря прочному связыванию с ферментом. Второй этап состоит в переносе аминоацильной группы от связанного с ферментом аминоацил-аденилата на 2'-или 3'-ОН-группу концевой рибозы тРНК. Потенциала переноса ацильной группы аминоацил-тРНК более чем достаточно для образования пептидной связи без дополнительного поступления энергии.
Ключевой особенностью реакции, приводящей к аминоацетилированию тРНК, является специфичность участвующих в ней ферментов. Присоединение к тРНК каждой из 20 аминокислот, встречающихся в белках, катализируется определенной аминоацил-тРНК-синтетазой. Фермент должен отличить одну аминокислоту от 19 других и перенести ее к одной или нескольким изоакцепторным тРНК из имеющихся примерно 75 других тРНК. Вспомним при этом, что многие аминокислоты очень сходны по структуре: лейцин, валин и изолейцин; валин и треонин; аспарагиновая и глутаминовая кислоты. Аминоацил-тРНК-синтетазы должны отличить «свои» тРНК от всех других, несмотря на удивительное сходство их вторичной и третичной структур. Поэтому необходимо, чтобы ферменты обладали очень высокой специфичностью, позволяющей им сделать правильный выбор из столь родственных структур и избежать ошибок при синтезе белка.
Комментарий по поводу структур аминоацил-тРНК-синтетаз и их способности к узнаванию аминокислот и родственных тРНК. Многие аминоацил-тРНК-синтетазы удалось очистить. Некоторые из них состоят из одной полипептидной цепи, другие – из двух или четырех идентичных цепей, каждая мол. массой от 35 до 115 кДа. Некоторые димерные и тетрамерные ферменты состоят из субъединиц двух типов. Четкой корреляции между размером молекулы фермента или характером его субъединичной структуры и специфичностью не существует.
Исследования взаимодействия между аминоацил-тРНК-синтетазами и родственными им тРНК не позволили выяснить природу их высокой специфичности. Большинство работ показало, что специфичность фермента определяется его прочным связыванием с акцепторным концом тРНК, DU-участком и вариабельной петлей. Некоторые ферменты, по-видимому, не распознают антикодоновый триплет и катализируют реакцию аминоацетилирования даже при измененном антикодоне. Однако отдельные ферменты проявляют пониженную активность по отношению к таким модифицированным тРНК и при замене антикодона присоединяют не ту аминокислоту. Следовательно, в некоторых случаях существенным оказывается и взаимодействие с антикодоновой петлей. В любом случае акцепторный конец тРНК должен быть ориентирован так, чтобы каталитический центр фермента смог перенести связанный аминоациладенилат к концевому нуклеотиду тРНК.
В какой-то степени способность фермента присоединять нужную аминокислоту к родственной тРНК зависит от специфического связывания аминокислоты. Однако, если безошибочное распознавание родственных аминокислот невозможно, синтетазы могут исправлять ошибки, происходящие при присоединении. Например, нельзя полностью исключить возможность связывания валина изолейцил-тРНК-синтетазой из-за сходства размера и структуры изолейцина и валина. Дефект в специфичности обнаруживается в первой же реакции: изолейцил-тРНК-синтетаза образует ферментсвязанный валил-аденилат, хотя и с меньшей эффективностью, чем изолейцил-аденилат, однако такой активированный валин не связывается ни с TPHK, ни с тРНК. Вместо этого ферментсвязанный валил-АМР быстро гидролизуется в присутствии тРНК, и образование валил-тРНК предотвращается. Подобный механизм позволяет валил-тРНК-синтетазе различать валин и треонин, а метионил-тРНК-синтетазе отличать треонин от метионина. Очевидно, что аминоацил-тРНК-синтетазы пользуются механизмом коррекции с целью предотвращения неизбежных ошибок в аминоацетилировании тРНК. И напротив, механизм, с помощью которого удалялась бы уже присоединенная к тРНК неправильная аминокислота, отсутствует. В таких случаях аминокислота занимает неправильную позицию в белке. Частота таких ошибок очень низка. В гемоглобине кролика, например, валин оказывается в местах, обычно занимаемых изолейцином, только в одном из 25000–50000 возможных случаев. Таким образом, точность первого шага на сложном пути считывания генетической информации обеспечивается четкой работой разных аминоацил-тРНК.
б. На рибосомах осуществляются спаривание аминоацил-тРНК с кодонами и сборка белковых цепей
Во всех клетках имеются рибосомы, играющие ключевую роль в синтезе белка; их число колеблется от 20000 до 50000 в зависимости от белоксинтезирующей активности клеток. Рибосомы индифферентны в отношении синтезируемых ими белков или тех клеточных мишеней, к которым они направляют синтезированные продукты. Тип синтезируемого рибосомой белка в каждом синтетическом цикле диктуется мРНК, с которой рибосома оказалась связанной. Внутри- или внеклеточная локализация белков определяется их структурными особенностями и – в зависимости от этих особенностей – характером взаимодействия со специализированными мембранами и органеллами.
Рибосомы про- и эукариот обладают в общем очень сходными структурой и функциями. Тем не менее из-за различий в структуре и организации про- и эукариотических мРНК и из-за того, что процессы транскрипции и трансляции у эукариот являются сопряженными во времени и в пространстве, тонкие различия между рибосомами про- и эукариот имеются. Типичными прокариотическими рибосомами являются рибосомы Е. coli, и поскольку их структура и функции изучены лучше остальных, мы используем эту модель в последующем обсуждении. Для сравнения мы остановимся на некоторых структурных особенностях рибосом эукариот.
Строение рибосомных частиц. Рибосомы прокариот состоят из малых и больших субчастиц. 30S-субчастицы состоят из единственной молекулы рРНК размером 1542 нуклеотида и 21 белка с разной мол. массой. 50S-субчастицы содержат две рРНК – большую, состоящую из 2904 нуклеотидов, и более мелкие, из 120 нуклеотидов; они связаны с 34 разными белками. Нуклеотидные и аминокислотные последовательности всех рРНК и белков известны. Электронно-микроскопические исследования 70S-рибосом и построения их трехмерных моделей показали, что малая и большая субчастицы соприкасаются в нескольких точках, но самой характерной особенностью является наличие бороздки между ними, необходимой, по-видимому, для размещения в ней мРНК на время трансляции.
И малая, и большая рибосомные субчастицы могут диссоциировать на составляющие молекулы РНК и белка. Более того, даже после отделения друг от друга молекулы всех РНК и белков способны восстанавливать исходную функционально активную рибосомную субчастицу, если их смешать в соответствующих условиях. Это означает, что вся информация о сборке мультимерного комплекса заключена в структуре его компонентов. Эксперименты по реконструированию рибосом позволяют лучше понять характер взаимодействия между этими компонентами и определить возможный порядок, в котором собираются белки и РНК in vivo. Кроме того, в подобных экспериментах можно проверить совместимость эквивалентных РНК или белковых субчастиц из различных источников. Далее, с помощью этого метода можно оценить способность мутантных РНК или белков к взаимодействию с восстановлением структуры рибосом и проявлению различных видов активности, присущих реконструированным рибосомам.
Рибосомы эукариот, находящиеся в цитозоле, также состоят из малых и больших субчастиц. Малые субчастицы содержат одну молекулу РНК размером 1900 нуклеотидов и 30–35 белков; большие – три цепи РНК длиной 120, 160 и 4800 нуклеотидов и 45–50 белков. Рибосомы митохондрий и хлоропластов отличаются от цитозольных рибосом. Как правило, они меньше и содержат меньшее количество белков и различных рРНК. Данные по физическому и химическому реконструированию более сложных эука-риотических хромосом значительно уступают аналогичным данным, полученным для Е. coli.
Необходимо выделить два важных в функциональном отношении участка, образующихся при ассоциации субчастиц в процессе формирования 70S-рибосомы. Это участки, в которых происходит связывание двух тРНК – одной, присоединенной к растущей белковой цепи, и другой, несущей следующую добавляемую к цепи аминокислоту.
Особые тРНК и некоторые вспомогательные белки, участвующие в трансляции. Как у про-, так и у эукариот имеются два вида тРНК, которые связывают метионин. У прокариот они обозначаются как тРНК и тРНК, а у эукариот – соответственно тРНК и тРНК. Каждая из обоих видов тРНК как у про-, так и у эукариот аминоацетилируется метионином с помощью соответствующих аминоацил-тРНК-синтетаз. тРНК прокариот и тРНК эукариот обладают необычными свойствами, позволяющими им функционировать в качестве адапторов при инициации синтеза полипептидной цепи в соответствующих инициаторных AUG-кодонах. тРНК про- и эукариот узнают AUG-кодоны в белок-кодирующих последовательностях.
У прокариот аминогруппа метионил-тРНК, но не метионил-тРНК формилируется особым ферментом до Fmet-TPHK с использованием в качестве донора формильной группы М10-формилтетрагидрофолата. Очевидно, трансформилаза отличает met-TPHKот met-TPHK. Fmet-TPHK используется исключительно для инициации белковых цепей, a met-TPHKMMet – только для декодирования внутренних метиониновых кодонов. Несмотря на то, что тРНК эукариот также используется только для инициации, ее метионильная группа не подвергается формилированию. Очевидно, некие особые свойства, присущие тРНК и необходимые для выполнения ею специальной инициаторной функции, связаны исключительно с ее нуклеотидной последовательностью и / или трехмерной структурой.
Известны белки, которые только временно, на период трансляции, связываются с рибосомами. Они играют важную роль при инициации, элонгации и терминации синтеза белковой цепи. Прежде чем подробно обсуждать эти процессы, мы познакомим читателя с такими белками и кратко опишем их свойства и роль в трансляции.
Эти белки, называемые факторами инициации и обозначаемые IF-1, IF-2 и IF-3, необходимы для инициации трансляции мРНК с образованием белков. IF-1 и IF-3 связываются с 3. Важным этапом терминации или отделения белковой цепи от мРНК является гидролиз GTP.
Похожие работы
... в отечественной теории и практике психологических измерений. Хотя концепт осмысленности измерения развивается с трансформацией идей Стивенса и разработкой проблем статистики и логики, его положения относительно шкалирования, по проблемам измерений в психологии и связанной с ними осмысленностью измерений требуют, на наш взгляд, критического анализа привычной практики использования психологического ...
... , вызванные динамическими му-тациями.-----------------------T-----------T-------T-----T------T------T----------------------¬ Болезнь, номер по ¦ Ген, лока-¦Триплет¦Норма¦Прему-¦Мута- ¦Литература ¦ МакКьюсику (MIM) ¦ лизация ¦ ¦ ¦тация ¦ция ¦ ¦ -----------------------+-----------+-------+-----+------+------+----------------------+ Синдром ломкой X-хро- ¦FMR1, FRAXA¦(CGG)n ...
... результаты были получены благодаря широкому использованию в лабораторных тестах генетически охарактеризованных животных, а также применению основных методов анализа генетических различий. В настоящее время исследование когнитивных способностей животных в этом тесте является одним из ведущих подходов в оценке особенностей поведения трансгенных животных и мышей-нокаутов. Детальнее с этими вопросами ...
... к основному тону, к тонике. Из обостренности интонации вводного тона среди полутонов развивается еще ряд важных для формы, как процесса интонирования, следствий: в отношении ладовом стирается тетрахордность, давнее наследие средиземноморской музыкальной культуры, и звукоряд европейский становится интонационным единством — гаммой; отношении эволюции гармонии возникает чувство доминантности, все ...

0 комментариев