Навигация
Фикобилины. Их структура, функции и физиологическая роль
4.3 Фикобилины. Их структура, функции и физиологическая роль
Синезеленые водоросли (цианобактерии), красные морские водоросли и некоторые морские криптомонады помимо хлорофилла а и каротиноидов содержат пигменты фикобилины. Наиболее известные представители фикобилинов — фикоэритробилины и фикоцианобилины. Первые преобладают у красных водорослей и определяют их цвет, вторые — у синезеленых.
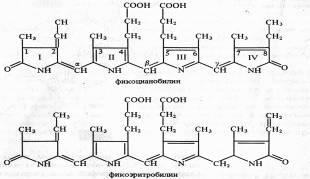
Структура и свойства фикобилинов. По структуре фикобилины. (от греч. «phycos» — водоросль и лат. bilis — желчь) относятся к группе желчных пигментов — билинов (у животных представитель этой группы — билирубин). Это тетрапирролы с открытой цепью, имеющие систему конъюгированных двойных и одинарных связей. В своем составе они не содержат атомов магния или других металлов, а также фитола.
У фикоцианобилина пиррольные кольца соединены между собой метиновыми мостиками. I и IV пирролы имеют по одной карбонильной группе. Пиррольные кольца содержат следующие боковые радикалы: четыре метильных (у C1,3,6,7), винильную (у С2), этильную (у С8) и два остатка пропионовой кислоты (у С4 и С5).
Фикобилины являются хромофорными группами фикобилипротеинов — глобулиновых белков, с которыми в отличие от хлорофиллов они связаны прочными ковалентными связями. Фикобилипротеины делятся на три основные группы; 1) фикоэритрины — белки красного цвета с максимумом поглощения от 498 до 568 нм, 2) фикоцианины — сине-голубые белки с максимумами поглощения от 585 до 630 нм, 3) аллофикоцианины — синие белки с максимумами поглощения от 585 до 650 нм. Все эти хромопротеины обладают флуоресценцией с максимумами 575 — 578, 635 — 647 и 660 нм соответственно.
Фикобилипротеины водорастворимы, в клетках водорослей они локализованы в фшобилисомах — гранулах, расположенных на наружной поверхности фотосинтетических ламелл.
Значение фикобилинов. Максимумы поглощения света у фикобилинов находятся между двумя максимумами поглощения у хлорофилла: в оранжевой, желтой и зеленой частях спектра (см. рис. 4.3). Значение такого распределения максимумов поглощения становится понятным, если вспомнить оптические свойства воды, которая поглощает прежде всего длинноволновые лучи. На глубине 34 м в морях и океанах полностью исчезают красные лучи, на глубине 177 м — желтые, на глубине 322 м — зеленые и, наконец, на глубину свыше 500 м не проникают даже синие и фиолетовые лучи. В связи с таким изменением качественного состава света в верхних слоях морей и океанов обитают преимущественно зеленые водоросли, глубже — сине-зеленые и еще глубже — водоросли с красной окраской. В. Т. Энгельман назвал это явление хроматической комплементарной адаптацией водорослей. По его наблюдениям (1881 — 1884), наиболее интенсивная ассимиляция С02 у водорослей с различной окраской соответствует максимумам поглощения света пигментными системами этих водорослей. Русский исследователь Н. М. Гайдуков (1903) экспериментально показал, что если культуру синезеленой водоросли Oscillaria sancta выращивать на свету разного спектрального состава, то у нее развивается дополнительная (комплементарная) окраска. При освещении зеленым светом водоросли становятся оранжево-красными, а при дейтвии красных лучей — зелеными. В настоящее время известно, что эти изменения цвета клеток связаны с изменениями в синтезе фикобилинов, принимающих участие в процессе фотосинтеза. Таким образом, у водорослей фикобилины — дополнительные пигменты, выполняющие вместо хлорофилла b функции светособирающего комплекса. Около 90% энергии света, поглощенного фикобилинами, передается на хлорофиллы а. Явление хроматической комплементарной адаптации обнаружено далеко не у всех видов синезеленых и красных водорослей. У многих из них адаптация к изменяющемуся спектральному составу света обеспечивается изменением количества и состава хлорофиллов а.
Экологическое значение спектрально-различных форм пигментов у фотосинтезирующих организмов.
Пигментные наборы фотосинтезирующих организмов позволяют им использовать весь диапазон длин волн падающей на Землю солнечной энергии. Обращает внимание большое различие в спектрах поглощения у представителей разных групп фотосинтезирующих организмов и прежде всего существенные сдвиги в максимумах поглощения хлорофиллов в красной области спектра. Несомненно экологическое значение этого явления, позволяющего избегать конкуренции за свет между разными группами фотосинтезирующих организмов. Что же касается эволюции спектров поглощения хлорофиллов, то очевидна тенденция к перемещению в более коротковолновую часть спектра с более высоким энергетическим уровнем.
5 Световая фаза фотосинтеза
5.1 Фотофизический этап. Электронно-возбужденное состояние пигментов. Представление о фотосинтетической единице. Антенные комплексы. Реакционные центры. Преобразование энергии в реакционном центре
На световой фазе фотосинтеза происходит поглощение света молекулами хлорофилла а с участием дополнительных пигментов (хлорофилла b, каротиноидов, фикобилинов) и трансформация энергии света в химическую энергию АТФ и восстановленного НАДФ. Все эти процессы осуществляются в фотохимически активных мембранах хлоропластов и представляют собой сложную систему фотофизических, фотохимических и химических реакций. В состав ламелл хлоропластов входят пять многокомпонентных белковых комплексов: светособирающий комплекс, фотосистемы I и II, цитохромный комплекс, включающий цитохромы b6 и f5 и АТФазный комплекс, участвующий в синтезе АТФ. Все они функционируют, взаимодействуя друг с другом.
Две фотосистемы. Впервые идею о существовании в хлоропластах двух фотосистем высказал Р. Эмерсон (1957), изучая влияние света на квантовый выход фотосинтеза у хлореллы. Под квантовым выходом фотосинтеза понимается количество выделившегося 02 или связанного С02 на 1 квант поглощенной энергии. Было показано, что квантовый выход высок при освещении хлореллы красными лучами с длиной волны 660-680 нм. Использование красного света с большей длиной волны приводило к снижению квантового выхода, а при 700 нм фотосинтез почти прекращался, хотя эта часть спектра еще поглощается хлорофиллом. Однако если хлореллу одновременно освещали коротковолновым (650 нм) и длинноволновым (700 нм) красным светом, то суммарный эффект (Y) был выше, чем при действии каждого красного света в отдельности.
Это явление получило название эффекта усиления Эмерсона. Отсюда возникло предположение, что в хлоропластах взаимодействуют две пигментные системы.
Предположение Эмерсона о двух пигментных системах подтвердилось в последующих работах, в которых из мембран хлоропластов с помощью детергентов (поверхностно-активных веществ, диссоциирующих гидрофобные связи) дифференциального центрифугирования в градиенте плотности сахарозы и других приемов удалось выделить и изучить белковые комплексы фотосистемы I (ФС I) и фотосистемы II (ФС II).
В состав ФС I в качестве реакционного центра входит димер пигмента П700 (хлорофилл а с максимумом поглощения 700 нм), а также хлорофиллы а675-695, играющие роль антенного компонента фотосистемы I. Первичным акцептором электронов в этой системе является мономерная форма хлорофилла а695 (Ах), вторичными акцепторами — А2 и Ав (железосерные белки — FeS). Комплекс ФС I под действием света восстанавливает водорастворимый FeS-белок ферредоксин (Фд) и окисляет медьсодержащий водорастворимый белок пластоцианин (Пц).
Белковый комплекс ФС II включает в себя реакционный центр содержащий хлорофилл а П680, а также антенные пигменты — хлорофиллы a670-673. Первичным акцептором электронов в этой фотосистеме выступает феофетин а (Фф), передающий электроны на первичный пластохинон, ассоциированный с FeS (QA) и дальше на вторичный пластохинон (Qb). В состав ФС II входят также белковый комплекс S-системы, окисляющий воду, и переносчик электронов Z, связанный с системой S и служащий донором е для П680. Этот комплекс функционирует с участием марганца, хлора и кальция. В ФС II локализован цитохром b559. ФС II восстанавливает пластохинон (PQ) и окисляет воду с выделением 02 и протонов.
Связующим звеном между ФС II и ФС I служат пул (фонд) пластохинонов, белковый цитохромный комплекс b6 — f5 и пластоцианин.
В ходе эволюции ФС I возникла раньше. Она функционирует у ныне существующих фотосинтезирующих бактерий, фотосинтез которых осуществляется без разложения воды и выделения 02 (фоторедукция). В этом случае функцию доноров электронов для световой фазы фотосинтеза выполняют легко окисляемые соединения, такие, как H2S, Н2, СН4 и др.
Антенные комплексы и миграция энергии в пигментных системах. Эмерсон и Арнольд показали, что в хлоропластах растений на каждый реакционный центр приходится от 200 до 400 молекул хлорофилла, функции которых связаны с поглощением света и передачей энергии возбужденного состояния на реакционные центры. Молекулы хлорофилла а и дополнительные пигменты — хлорофилл b, каротиноиды, фикобилины — входят в состав антенных или светособирающих комплексов (ССК). Из ламелл хлоропластов выделены светособирающий белковый комплекс с хлорофиллами а и b (ССКa-Ь ), тесно связанный с ФС II, и антенные комплексы, непосредственно входящие в фотосистемы I и II (фокусирующие антенные компоненты фотосистем).
В ССКa-Ь присутствуют хлорофилл а в двух или трех формах с максимумами поглощения между 660 и 675 нм, хлорофилл b с максимумом поглощения 650 нм и каротиноиды. В каждом ССКa-b содержится от 120 до 240 молекул хлорофиллов, причем отношение хлорофилла а к хлорофиллу b составляет 1,2—1,4. Половина белка тилакоидов и около 60% общего количества хлорофилла локализовано в ССК. У сине-зеленых и красных водорослей, у которых хлорофилл b отсутствует, роль ССК выполняют фикобилисомы, в состав которых входят фикобилины.
Антенный белковый комплекс ФС II содержит 40 молекул хлорофиллов а с максимумами поглощения 670 — 683 нм на один П680 и β-каротин.
Антенный белковый комплекс ФС I состоит из хромопротеинов, содержащих 110 молекул хлорофиллов а с максимумами поглощения 680 — 695 нм на один П700, из них 60 молекул — компоненты антенного комплекса самой фотосистемы, а 50 входят в состав комплекса, который можно рассматривать как ССК ФС I. Антенный комплекс ФС I также содержит β-каротин.
Хромопротеины антенных комплексов не обладают фотохимической и энзиматической активностью. Если бы каждая молекула хлорофилла преобразовывала поглощенную ею энергию кванта света в фотохимическую реакцию, то такая система была бы крайне нерентабельна. Продолжительность синглетного возбужденного состояния исчисляется 10-12 — 10-9 с, и даже на прямом солнечном свету 1 квант света поглощается молекулой хлорофилла не чаще одного раза за 0,1 с. Большую часть времени молекула хлорофилла «простаивает». Поэтому роль пигментов антенных комплексов состоит в том, чтобы собирать и передавать энергию квантов на небольшое количество молекул реакционных центров П680 и П700, которые и осуществляют фотохимические реакции. Аналогично отдельные капли дождя ударяют в крышу и, сливаясь, создают постоянный ток воды в водостоке.
Передача (миграция) энергии по пигментам антенных комплексов происходит по принципу индуктивного резонанса (без флуоресценции и переноса заряда). Природа индуктивного резонанса сострил в следующем. Каждая молекула хлорофилла, поглотившая квант света и перешедшая в синглетное возбужденное состояние, является молекулярным осциллятором. Возникающее вокруг возбужденной молекулы переменное электрическое поле с определенной частотой колебаний индуцирует осцилляцию диполя (электрон — ядро) соседней молекулы. При этом молекула-донор переходит в основное состояние, а молекула-акцептор — в возбужденное. Условиями для резонансного переноса энергии электронного возбуждения служат малые расстояния между молекулами, не превышающие 10 нм, и перекрытие частот колебаний у двух взаимодействующих молекул.
Флуоресценция каждой молекулы-донора имеет более длинноволновый максимум по сравнению с максимумом ее поглощения (в соответствии с правилом Стокса) и в большей или меньшей степени перекрывает зону поглощения акцепторной молекулы. Миграция энергии осуществляется от коротковолновых пигментов в сторону все более длинноволновых, т. е. пигментов с более низким уровнем синглетного возбужденного состояния.
В антенных комплексах перенос энергии осуществляется в ряду: каротин (400-550 нм)--► хлорофилл b (650 нм)--►хлорофиллы a (660-675 нм)---► П680 (ФС II). Скорость резонансного переноса энергии от молекулы к молекуле 10-10 — 10-9 с, причем эффективность переноса между молекулами хлорофилла достигает 100, а между молекулами каротина и хлорофилла — лишь 40%.
Реакционные центры. Белки, содержащие длинноволновые формы хлорофиллов (П680 в ФС II и П700 в ФС I) в количестве одна молекула на 200 — 400 молекул других хлорофиллов и способные к первичному фотохимическому разделению зарядов, называют реакционными центрами.
Первичное разделение зарядов в реакционных центрах происходит между молекулами хлорофилловой природы и связано с транспортом электронов. Функцию первичного донора электронов выполняет молекула хлорофилла, находящаяся в синглетном возбужденном состоянии. В реакционном центре ФС II, перешнуровывающем мембрану, первичным донором электронов служит П680, а первичным акцептором — феофетин. В реакционном центре ФС I первичный донор электронов— П700, а акцептор — мономерная форма хлорофилла а695 (А1).
Порядок реакций в реакционном центре ФС II определяется продолжительностью того или иного состояния молекул. Молекулы находятся в синглетном возбужденном состоянии 10-10 — 10-9 с. Первичные акцепторы (Фф или А1) получают электроны от своих доноров (П680 или П700 соответственно) за время около 10-12 с. Время обратных рекомбинаций от Фф- на П680+ и от A1- на П700+ во много раз больше (10-6 с). То же самое относится к последующим парам взаимодействующих молекул. Поэтому весь ход реакций резко сдвинут вправо. В реакционных центрах энергия возбужденного состояния хлорофилла преобразуется в энергию разделенных зарядов, т. е. превращается в химическую энергию.
5.2 Фотохимический этап. Электронно-транспортная цепь фотосинтеза. Представления о функционировании двух фотосистем. Фотофосфорилирование. Системы фотоокисления воды и выделения кислорода при фотосинтезе. Связь фотосинтетической ассимиляции С02 с фотохимическими реакциями
Нециклический и циклический транспорт электронов.
Для восстановления одной молекулы NADP+ в процессе фотосинтеза необходимы два электрона и два протона, причем донором электронов является вода. Фотоиндуцированное окисление воды осуществляет ФС II, восстановление NADP+ — фотосистема I. Следовательно, эти две фотосистемы должны функционировать во взаимодействии.
Исходя из данных о квантовом выходе фотосинтеза (необходимы 8 квантов света для выделения одной молекулы 02) из состава компонентов, входящих в ФС I и ФС II, и величин их окислительно-восстановительного потенциала была разработана схема последовательности реакций в световой фазе фотосинтеза.
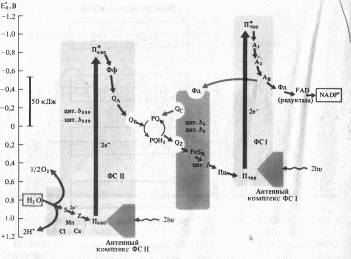
Из-за сходства с буквой Z эта схема, получила название Z-схемы. Впервые принцип Z-схемы был предложен Р. Хиллом и Ф. Бендаллом (1960) и экспериментально подтвержден работами Л. Дюйзенса (1961). В настоящее время Z-схема, или схема нециклического транспорта электронов при фотосинтезе является общепризнанной и непрерывно пополняется новыми деталями.
В ФС II димер П680, поглотив энергию, эквивалентную 2 квантам коротковолнового красного света, и перейдя в синглетное возбужденное состояние, отдает 2 электрона феофетину (Фф). От Фф электроны, теряя энергию, последовательно передаются на пластохиноны ФС 11 - QA и QB, на пул липидорастворимых молекул пластохинона (PQ), переносящих через липидную фазу мембраны электроны и протоны, на железосерный белок FeSK и цитохром цитохромного комплекса b6 — f, восстанавливая Cu-содержащий белок пластоцианин (Пц).
Вакантные места («дырки») в Пб80 заполняются двумя электронами из содержащего Мп переносчика электронов Z, который в свою очередь восстанавливается с участием системы S. Окисленный белковый комплекс S связывает воду и восстанавливается за счет электронов воды. Для осуществления этой реакции в белковом комплексе S необходимы Мп и С1-, а также Са2 + .
Однако описанная цепь реакций резко замедляется, если не возбуждена ФС I, так как в этом случае весь Пц переходит в восстановленное состояние. При возбуждении П700 в реакционном центре ФС I энергией, эквивалентной 2 квантам длинноволнового красного света, 2 электрона захватываются мономерной формой хлорофилла a (A1) и затем последовательно передаются переносчикам электронов А2 и Ав (железосерные белки FeS), ферредоксину (водорастворимый FeS-белок) и ферредоксин: NADP-оксидоредуктазе с FAD в качестве кофактора. Наконец, редуктаза восстанавливает NADP + .
На вакантные места в П700+ переходят электроны с Пц, и нециклическая цепь переноса электронов таким образом замыкается. Z-схема убедительно объясняет «эффект усиления Эмерсона», так как только при совместном использовании коротковолновых (ФС II) и длинноволновых (ФС I) лучей красного света интенсивность фотосинтеза будет оптимальной.
Энергия, освобождающаяся при движении электронов от П680 до П700, используется для синтеза АТФ из AДФ и неорганического фосфата (фотофосфорилирование).
Наряду с нециклическим в мембранах хлоропластов функционирует циклический транспорт электронов, включающий в себя только ФС I и комплекс цитохромов Ь6 — f. В этом случае возбужденные молекулы П700 последовательно отдают электроны на А1, А2, АB, Фд, PQ, цитохром b6, FeSR, цитохром f, Пц и, наконец, П700. При этом НAДФ+ не восстанавливается. Освобождающаяся энергия используется для фосфорилирования AДP.
Интересно отметить, что комплекс цитохромов Ь6 — f функционирует в системе транспорта электронов при фотосинтезе аналогично комплексу III (цит. Ь, C1) в митохондриях.
Разница в уровнях энергии между П680 и П700 (> 50 кДж) вполне достаточна для фосфорилирования AДФ, так как величина высокоэнергетической фосфатной связи АТФ равна 30,6 кДж/моль (7,3 ккал). Перепады энергии в ФС I еще значительнее. Однако само по себе освобождение энергии при нециклическом и циклическом транспорте электронов не объясняет, каким образом осуществляется фотофосфорилирование.
Механизм фосфорилирования AДФ, сопряженного с деятельностью ЭТЦ , объясняет хемиосмотическая теория, разработанная английским биохимиком П. Митчеллом (1961 — 1966). Для объяснения процессов фотофосфорилирования эта теория была впервые использована А. Ягендорфом (1967).
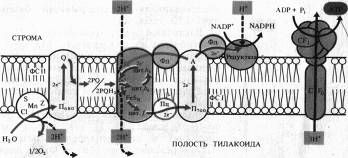
Сущность хемиосмотической теории состоит в следующем. Цепь переносчиков электронов и прогонов, действующая в соответствии с окислительно-восстановительным градиентом, перешнуровывает мембрану таким образом, что трансмембранный перенос е- и Н+ в одну сторону чередуется с переносом в обратную сторону только е-. В результате функционирования такого механизма (Н + -помпы) по одну сторону мембраны накапливается избыток Н+ и возникает электрохимический (т. е. электрический и концентрационный) потенциал ионов Н+, который служит формой запасания энергии. Обратный пассивный ток ионов Н+ через протонный канал Н+-АТФазы, получивший название сопрягающего фактор CF1, сопровождается образованием высокоэнергетической фосфатной связи АТФ.
На рис. 6.1 представлена упрощенная схема расположения переносчиков в мембране тилакоидов, объясняющая механизм фотофосфорилирования. На внутренней стороне мембраны тилакоида под действием света возбуждаются П680 и П700. Электроны от П680 захватываются акцепторами е- на наружной стороне и передаются на окисленную форму пластохинона (PQ) — липидорастворимого переносчика прогонов и электронов, выполняющего функцию челнока. Принимая два электрона, 2PQ диффундируют к цитохромному комплексу и захватывают из стромы 2Н + . Электроны с 2PQH2 поступают в цепь: F.eSR -> цит. f -> Пц,-> П700, а ионы Н + попадают в полость тилакоида. Вторая пара ионов Н+ освобождается там же при фотоокислении воды. В ФС I электроны П700 захватываются акцептором А, передаются ферредоксину и затем НAДФ+ на наружной стороне мембраны, причем 1Н+ используется на восстановление НAДФ.
Таким образом, из среды, окружающей тилакоид, при поглощении пигментами квантов света исчезают, а во внутренней полости тилакоида появляются протоны. В результате на мембране возникает электрохимический потенциал ионов Н + , который затем используется для фосфорилирования AДФ. Этот процесс называется нециклическим фотофосфорилированием.
При циклическом фотофосфорилировании, когда функционирует только ФС I, электроны от Фд поступают на цитохромный комплекс с использованием пула PQ, который действует как переносчик электронов и протонов. Затем электроны через цитохром f и Пц возвращаются на основной энергетический уровень в П700, а протоны поступают в полость тилакоида.
Белковые комплексы, участвующие в фотохимических реакциях фотосинтеза, в мембранах хлоропластов распределены неравномерно. Наибольшие различия наблюдаются между теми мембранами, которые плотно состыкованы друг с другом в гранах и теми участками мембран, которые контактируют со стромой (закругленные участки тилакоидов гран и мембраны тилакоидов стромы).
Светособирающий комплекс и пигмент-белковый комплекс ФС II находятся в основном в мембранах, плотно контактирующих друг с другом, причем ССК играет особую роль. В адгезии тилакоидных мембран.
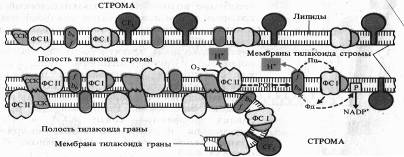
Показано, что у мутанта хламидомонады, лишенного белка, с которым связан хлорофилл Ь, граны не образуются. ФС I со своим светособирающим комплексом преимущественно, а АТФазный комплекс (CF1 + CF0), как правило, находятся на несостыкованных участках мембран. Комплекс цитохромов b6 — f равномерно распределен как в состыкованных, так и в не состыкованных мембранах. Такое распределение белковых комплексов, участвующих в световой фазе фотосинтеза, ставит вопрос о способе их взаимодействия. Показано, что это взаимодействие осуществляется с помощью легкоподвижного липофильного пластохинона PQ в липидной фазе и благодаря перемещению водорастворимого пластоцианина вдоль внутренних поверхностей ламелл и водорастворимого ферредоксина вдоль их наружных поверхностей.
К латеральным перемещениям вдоль мембраны способны и сами белковые комплексы. На это передвижение влияет величина их электрического заряда. Например, восстановление пластохинона PQ фотосистемой II приводит к активации киназы и фосфорилированию ССКа-ь. Фосфорилирование ССК увеличивает его отрицательный заряд, что способствует перемещению ССК в стромальную область мембраны и возрастанию миграции поглощенной энергии света к ФС I. Возросшая фотохимическая активность ФС I усиливает окисление PQ, что, в свою очередь, приводит к инактивации киназы, фосфатаза же дефосфорилирует ССК. Таким образом, обратимое фосфорилирование ССК представляет собой петлю обратной связи в системе взаимной регуляции активности ФС I и ФС II. Механизм такой регуляции включает латеральный транспорт белковых комплексов в мембранах хлоропластов.
Похожие работы
... в трофических цепях. Именно в круговоротах биогенных химических элементов, по мнению В.И. Вернадского, заключается геологическая роль живого вещества планеты. Живые организмы формируют не только биологический, но и геологический лик планеты. Важной идеей В.И. Вернадского была мысль о космической роли живого вещества, которая заключается в аккумулировании солнечной энергии и преобразовании ее в ...
... период многие страны приняли решение о полном или постепенном отказе от развития атомной энергетики. 1.3 Особенности альтернативной водородной энергетики Водородная энергетика включает следующие основные направления: Разработка эффективных методов и процессов крупномасштабного получения дешевого водорода из метана и сероводородсодержащего природного газа, а также на базе разложения воды; ...
... взаимодействия – зависимость организма от среды – была полно раскрыта от Ламарка до Мичурина. Но обратное явление – отражение жизни на среде – почти не привлекало внимание до В.И.Вернадского. Указывая, что связь живого и неживого в биосфере является взаимной, ученый писал: «Организм имеет дело со средой, к которой он не только приспособлен, но которая приспособлена и к нему». Конечно, здесь ...
... голоса, слушают пение птиц, плеск волн и шум ветра, дышат свежим воздухом. Воспользоваться таким транспортом захочет каждый, кто любит совершать водные путешествия. 6. РОССИЯ, УКРАИНА И СОЛНЕЧНАЯ ЭНЕРГЕТИКА В России в настоящее время имеется восемь предприятий, имеющих технологии и производственные мощности для изготовления 2 МВт солнечных элементов и модулей в год. В 1992 году на ...
0 комментариев