Навигация
Основные физико-химические свойства сырья и готовой продукции. Государственные стандарты на них
1.2 Основные физико-химические свойства сырья и готовой продукции. Государственные стандарты на них
1.2.1 Исходное сырье
Аммиак: в обычных условиях представляет собой бесцветный газ с резким запахом, хорошо растворим в воде и других растворителях, с воздухом и кислородом образует взрывоопасные смеси.
Химическая формула – NH3
Молекулярный вес – 17,03
Плотность, кг \ м3:
Жидкий аммиак – 681
Газообразный - 770
Температура самовоспламенения – 650 ˚С.
Температура затвердевания – 77,75 ˚С.
Без катализатора разлагается при температуре 1000 ˚С, с катализатором – при 300 ˚С.
| Массовая концентрация: | ||
| - | масла (после фильтров поз.2)- | не более 1,0 мг/м3 |
| - | железа (после фильтров поз.2) - | не более 1,0 мг/м3 |
| - | Инерты - | не более 0,5% |
| Массовая концентрация газообразного аммиака - | не менее 99,6% | |
Должен соответствовать ГОСТ 6221-90.
Воздух: сухой воздух должен содержать (% об.): N2 - 78.1; O2 – 21.0; Ar2 – 0.9; содержание водяных паров колеблется от 0,1 до 2,8 % (об.). В районе промышленных площадок воздух загрязнен пылью различного происхождения, а также разнообразными компонентами неорганических газовых выбросов. Количество пыли в воздухе составляет 0,5 – 1,0 мг\м3.
| Массовая концентрация пыли (после аппарата очистки воздуха)- | не более 7,0 мг/м3 |
Должен соответствовать ГОСТ 24484.
1.2.2 Вспомогательные материалы и катализаторы
Таблица 1 – Вспомогательные материалы и катализаторы
| Наименование сырья, материалов, полупродуктов, энергоресурсов | Показатели по стандарту, обязательные для проверки | Регламентируемые показатели | |||
| 1 | 2 | 3 | |||
| Деаэрированная вода (смесь частично-обессоленной воды с паровым конденсатом) для водогрейных котлов | Общая жесткость | не более 0,01 ммоль/дм3 | |||
| Прозрачность по шрифту | не менее 40 см | ||||
| Массовая концентрация: | |||||
| - | соединений железа (в пересчете на Fe++) | не более 0,1 мг/кг | |||
| - | растворимого кислорода (О2) | не более 0,03 мг/дм3 | |||
| - | массовая концентрация солей | не более 150 мг/дм3 | |||
| - | рН при 250С | 8,5 - 9,5 | |||
| Сетки катализаторные из платинового сплава | ГОСТ 3193-74 с изм. 5 сетки из платино-палладиевого сплава марки ПлПдРд -4 - 3,5 Кр.2875 мм с содержанием платины - 92,5% | Диаметр: | |||
| - - | Проволоки - 0,092 мм Сетки - 2875 мм | ||||
| Удостоверение качества продукции на устанавливаемую сетку должно соответствовать стандарту и марке | |||||
| Катализатор железохромовый среднетемпературный конверсии оксида углерода СТК-1 | ТУ 113-03-317-86 с изм. 3, марка CТК – 1 или CТК-1М | Диаметр - 7 мм Массовая концентрация: | |||
| железа в пересчете на Fe2О3 CТК-1 не менее 88% CТК - 1М не менее 86% | |||||
| Насыпная плотность н/б 1,3 кг/дм3 | |||||
| Паровой конденсат | Массовая концентрация солей | не менее 7,0% | |||
| рН | оксида железа (Fe2О3) | не менее 6,5% | |||
| Аммиак | оксида хрома (Сr2О3) | не нормир. | |||
| н/б 0,3% | 1,0-1,5% | ||||
Похожие работы
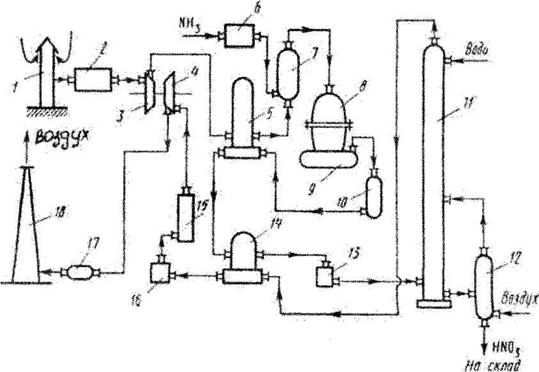
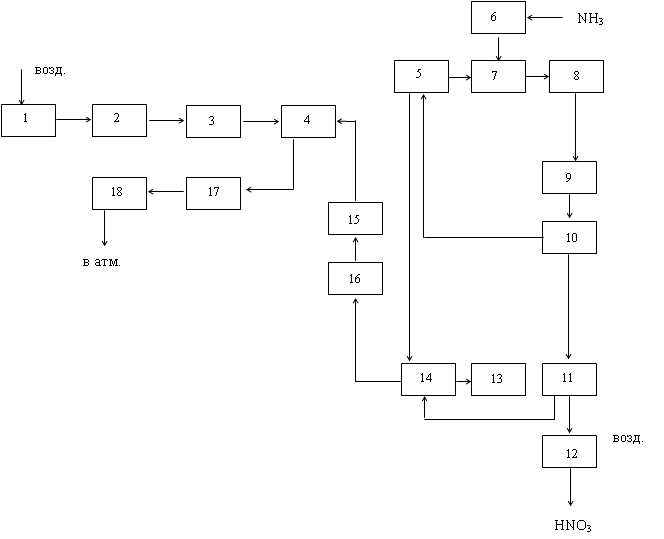
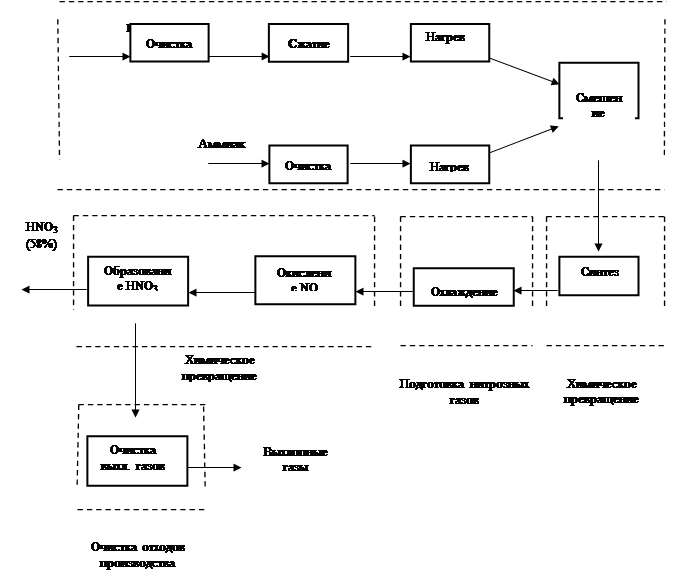
... + 50 2 = 4NO + 6Н2О 2NO+O2=2NO2 3NO2 + H2O = 2NО3 + N0 NH3 + 2О2 = HNO3 + Н2О + 421,2 Технологическая схема Рис. 3. Технологическая схема производства азотной кислоты 1-воздухозаборная труба; 2-воздухоочиститель; 3-газовый компрессор; 4-газовая турбина; 5-воздухоподогреватель; 6-испаритель аммиака; 7-смеситель с фильтром; 8-контактный аппарат; 9,17-котёл-утилизатор; 10-окислитель с ...
... в производстве концентрированной азотной кислоты по методу прямого синтеза. В отдельных случаях используется для обогащения АВС при получении неконцентрированной азотной кислоты. СОВРЕМЕННОЕ СОСТОЯНИЕ ТЕХНОЛОГИИ ПРОИЗВОДСТВА НЕКОНЦЕНТРИРОВАННОЙ АЗОТНОЙ КИСЛОТЫ. Азотная кислота и главным образом ее природная соль - натриевая селитра известны с давних времен. В 778 г. Арабский ученый Гебер ...
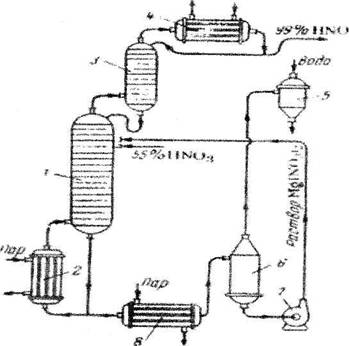
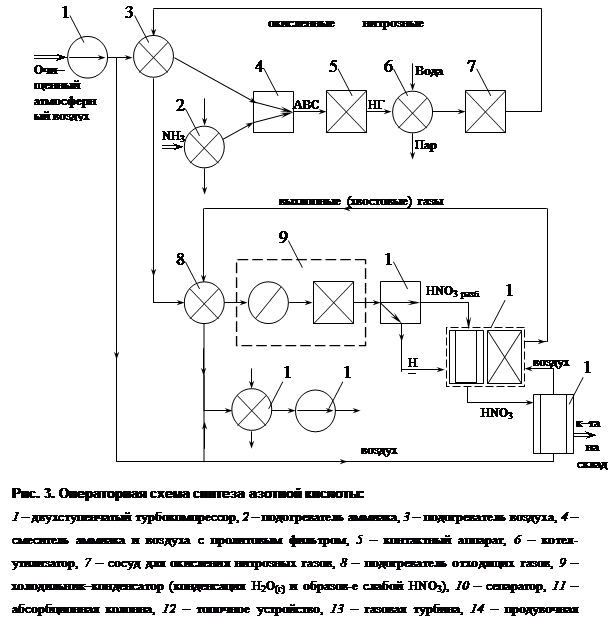
... очистки выхлопных газов, выпускающий продукцию в виде 53–58% -ной HNO3. Технологическая схема этого производства в упрощенном варианте представлена на рисунке 5. Подготовка сырья Рис.5 Схема производства азотной кислоты под давлением 0,716 МПа с приводом компрессора от газовой турбины: 1 – фильтр воздуха; 2 – реактор каталитической очистки; 3 – топочное устройство; 4 – ...
... способствует образованию NO2. При температурах до 100 ºС равновесие реакции практически полностью сдвинуто в правую сторону. Окисление диоксида азота – самая медленная стадия получения азотной кислоты. Она сильно зависит от концентрации реагентов, давления температуры. Применение воздуха, обогащенного кислородом (или чистого кислорода) позволяет получать НГ[2] с повышенным содержанием ...







0 комментариев