Навигация
Аппаратура для хроматографии
2.1 Аппаратура для хроматографии
Газоанализаторы.
1. Универсальный газоанализатор «ГАНК-4».
ГАНК-4 – серийная копия Первого универсального космического газоанализатора. ГАНК-4 отмечен высшими наградами на 5 международных выставках, имеет 7 патентов.
В газоанализаторе реализован экспрессный метод измерения максимально-разовых концентраций основных загрязнителей атмосферного воздуха и воздуха рабочей зоны (контролируемые вещества по выбору – до 130 (аммиак. ацетон, аэрозоль краски, бензин, водород, диоксид азота, диоксид углерода, кислород, кислота азотная, серная, уксусная, ксилол, марганец, масло минеральное, метанол, озон, окись этилена, пыль, сажа, сероводород, стирол, толуол, фенол, формальдегид. щелочь, этанол. этиленгликоль. этилцеллозольв и другие); диапазон измерений – от 0,001 мг/куб. м до 100 % об).
Достоинством газоанализатора является малый вес, автономное питание от встроенного аккумулятора, возможность легкого и быстрого использования различных датчиков (химических сенсоров) и химкассет на различные ингредиенты для анализа атмосферного воздуха и воздуха рабочей зоны. Он с успехом применяется как основное средство измерений при аттестации рабочих мест.
Широкая номенклатура анализируемых веществ дает возможность пользователю легко выбирать перечень загрязнителей и диапазоны их измерения, которые необходимы для работы на различных объектах.
Газоанализатор «ГАНК-4» удобен в эксплуатации, не требуется специальной перенастройки прибора при переходе с одного ингредиента на другой, имеется возможность производить измерения в любом месте, на любой высоте, не требуется выполнять усредненный расчет показаний – средний результат высвечивается на дисплее, одновременно производится отбор следующей пробы и обработка результата.
Газоанализатор является незаменимым средством измерения при различной загазованности объектов, ликвидации чрезвычайных ситуаций, для принятия срочных мер.
2. Портативный газовый хроматограф ФГХ-1.
ФГХ-1 является современным автоматизированным средством экспресс определения концентрации вредных веществ в воздухе. Благодаря высокой чувствительности и автоматизации, один и тот же прибор без какой-либо пробоподготовки позволяет анализировать содержание вредных веществ в воздухе в широком диапазоне концентраций: от ПДК в атмосфере до промышленных выбросов и при чрезвычайных ситуациях.
ФГХ - является уникальным средством эксресс-анализа, предназначенным для работы как в лабораторных, так и в «полевых» условиях непосредственно на исследуемом объекте, так как содержит собственные средства электро- и газового питания. Результаты анализа, комментарии к ним и сами хроматограммы автоматически документируются в памяти компьютера и могут быть немедленно предъявлены Заказчику или администрации контролируемого предприятия. Количество хранящихся хроматограмм – до 2000. Помимо определения концентрации веществ, ФГХ позволяет их автоматически идентифицировать.
Хроматограф содержит компьютер типа «Note-Book». Простое в использовании программное обеспечение позволяет проводить анализ в автоматическом режиме, а также работать с хроматограммой, воспроизводимой на экране компьютера. Для работы на ФГХ в автоматическом режиме не требуются специальные знания и опыт работы на хроматографах.
Анализируемые вещества – предельные и непредельные углеводороды, спирты, простые и сложные эфиры, ароматические углеводороды, кетоны, нефтепродукты, растворители, хлорпроизводные углеводородов, окись азота, сероуглерод и другие. Время анализа – менее 10 минут.
Некоторые примеры наиболее подходящих портативных (переносных) средств и их основные характеристики:
1. Хроматограф газовый полевой типа ЭХО-М (г. Новосибирск) масса 6 - 7 кг, электропитание 12 В, время непрерывной работы 8 ч. Детектор электронного захвата. Возможна замена детекторов (фотоионизационный детектор, пламенно-ионизационный детектор). Предел обнаружения с детектором электронного захвата составляет 5 10-13 кг (с возможным дополнением 1000 - кратного обогащения в выносном концентраторе). Цена - 12 000 - 14 000 $.
2. Хроматограф газовый переносной для анализа неорганических газов и продуктов сгорания топлива типа АХГ - 002. Предел обнаружения, г/см3: по Н2 - 8,4·10-10, по СО - 3,5·10-8, по СН4 - 6,6·10-9, по О2 - 8,7·10-9, по СО2 - 9,2·10-7 с детектором по теплопроводности. Цена ~ 2100 $.
3. Хроматограф газовый малогабаритный типа ХПМ - 5 для анализа сложных смесей веществ. Масса - 20 кг (аналитический блок) и 8 кг (блок питания), габариты, мм - 412х282х341 (аналитический блок) и 120х311х290 (блок питания). Пределы обнаружения: S - 1,0·10-10 (пламенно-фотометрический детектор), P - 1·10-11 - (пламенно-фотометрический детектор) и 2,0·10-12 (термоионный детектор), N-5·10-12 (термоионный детектор), пестициды - 4,0·10-13 (детектор электронного захвата), УВ - 2,0·10-8 (детектор по теплопроводности) и 2·10-11(пламенно-ионизационный детектор). Цена 3500 $.
4. Хроматографы жидкостные переносные типа «Цвет - 403». Масса - 16 кг, предел обнаружения, в мг/мл: 10-8 - 10-10 (электрохимический детектор) и 10-4 (ультрафиолетовый детектор). Цена 3000 - 3400 $.
5. Фотометр КФК-05 переносной малогабаритный (АООТ «Загорский оптико - механический завод», г. Сергиев-Посад). Габариты 190х170х83 мм, вес 1,2 кг, электропитание 220 и 12 В. Погрешность 1 %, среднеквадратичное отклонение 0,15 %.
6. Микрофотоколориметр полевой. МКМФ-02П (микропроцессорный аналог). Цена 455 - 520 $.
7. Спектрофотометр переносной DR/2010 VIS, =400-900 нм, погрешность 2 %, среднеквадратичное отклонение 0,15 %. Цена 3500 $.
Хроматографы
Вторым признанным лидером по числу реализуемых методик анализа веществ в объектах окружающей среды (20 - 40 %) в настоящее время являются приборы, основанные на хроматографии. Газовые (подвижная фаза - газ, неподвижная - твердый сорбент), газожидкостные (подвижная фаза - газ, неподвижная - тонкий слой жидкости на твердом носителе), жидкостные (подвижная фаза - жидкость, неподвижная фаза - твердый сорбент).
Среди отечественных хроматографических приборов больше всего отмечается газовых хроматографов (ряд серий и несколько десятков моделей). Наиболее известными в России являются газовые хроматографы серии «ЦВЕТ» Дзержинского завода (Московская область). Наиболее распространенная модель из этой серии - лабораторный газовый хроматограф «ЦВЕТ-800» с пламенно-ионизационным детектором. Цена базовой модели от 3700 $. Она может комплектоваться еще пятью детекторами (290 - 860 $).
ДТП - детектор по теплопроводности (для анализа летучих органических и неорганических соединений), неселективен,
ДЭЗ (ЭЗД) - детектор электронного захвата. Для высокочувствительного анализа Cl-, P- и N- содержащих соединений, в том числе ядохимикатов, селективен к Cl и O содержащим соединениям,
ПФД -пламенно - фотометрический детектор, селективен к P- и S-содержащим соединениям,
ТИД - термоионный детектор, селективный к P- и N- содержащим соединениям,
ФИД - фотоионизационный детектор (для анализа ароматических и алифатических углеводородов, фенолов, пестицидов и др. органических веществ с потенциалом ионизации ниже 12 эВ).
В зависимости от детектора и определяемого вещества чувствительность этого хроматографа может составлять 10-10 - 10-4 % об. Отличается высокой точностью (± 1-7 %) и воспроизводимостью анализа. Режимы задаются и управляются микропроцессором, а обработка выходной информации осуществляется компьютером или с выводом на самописец для ручной обработки.
Еще одна достаточно известная модель газовых хроматографов - «Кристалл». Наиболее современные и полностью автоматизированные отечественные лабораторные хроматографы - «Кристалл-200М», «Кристалл-4000».
Жидкостные хроматографы
Наиболее известны отечественные микроколоночные лабораторные жидкостные хромтаографы серии «МИЛИХРОМ», управляемые компьютером (5400 - 8400 $). Эти приборы позволяют с чувствительностью 10-9 - 10-11 г (10-3 - 10-5 г в пробе) определять пестициды, фенолы, тяжелые металлы, ПАУ, альдегиды, бензойную кислоту и другие органические вещества. Точность определения обычно составляет 1 - 3 %.
Отечественные ионные хроматографы: «ЦВЕТ - 3006М», «ЦВЕТ - 4000», «Стайер».
Остановимся более подробно на принципе работы детекторов, используемых в хромтаографии.
Детекторы газовых хроматографов
Детекторы обычно классифицируют на основании их селективности на универсальные, реагирующие на каждый компонент в подвижной фазе, селективные для определенной группы веществ, специфические для одного или ограниченного круга компонентов со сходными химическими характеристиками.
Пламенно-ионизационный детектор (ПИД). Проводимость газа -носителя, являющегося электрополяризатором, существенно возрастает благодаря ионам, образующимся при горении органических соединений в водородном пламени. Отклик ПИД пропорционален числу атомов углерода в молекуле, изменяется при переходе от одного класса органического соединений к другому незначительно.
Достоинства: простота в обращении, быстрый отклик, широкий линейный динамический диапазон, универсальность.
Недостатки: при проведении анализа определенного соединения в сложной матрице требуется более селективный детектор для уменьшения числа пиков мешающих компонентов. ПИД дает слабый отклик на вещества с малым содержанием углерода.
Электронно-захватный детектор (ЭЗД) используют для определения галогенсодержаищх соединений: хлорорганические пестициды, дибензафураны, тригалометаны и т.д. Принцип действия этого детектора основан на уменьшении проводимости, вызываемом захватом электронов специфическим анализируемым веществом. В состав детектора входит радиоактивный источник малой интенсивности (фольга с 63Ni), который испускает электроны высокой энергии. Ионизация молекул газа - носителя (азота или смеси аргона и метана) приводит к образованию ионов и тепловых электронов, которые и формируют электрический ток в ионизационной камере. Когда в нее попадают молекулы галогенсодержащих органических соединений, тепловые электроны захватываются атомами галогена и проводимость уменьшается, что приводит к формированию сигнала детектора.
ЭЗД хорошо зарекомендовал себя при анализе питьевых и подземных вод. В случае поверхностных и сточных вод, содержащих множество органических соединений различных классов, требуется предварительная очистка вод.
Сочетание фотоионизационного детектора и детектора электролитической проводимости. Для анализа летучих ароматических и галогенсодержащих соединений рекомендуется последовательное соединение неразрушающего фотоионизационного детектора (ФИД) и детектора по электролитической проводимости (ЭПД).
В фотоионизационном детекторе вещества возбуждаются фотонами, излучаемыми УФ-лампой, электрический ток, формируемый заряженными частицами, измеряется с помощью двух электродов. Селективность зависти от используемой лампы.
При детектировании галогенсодержащих компонентов посредством ЭПД входящее из колонок вещество восстанавливается водородом в никелевой реакционной трубке при 85 оС с образованием газообразного галогенводорода, который в свою очередь растворяется в н-пропаноле. Изменение проводимости растворителя преобразуется в сигнал детектора.
Атомно-эмиссионный детектор. АЭД позволяет различать галогенорганические соединения. В АЭД выходящее из колонки вещество атомизируется в высокоэнергетическом источнике, образовавшиеся возбужденные атомы излучают свет при возвращении в основное состояние. Излучаемый свет с различными длинами волн диспергируется в спектрометре и измеряется посредством фотодиодной матрицы. Каждый химический элемент имеет свой собственный типичный эмиссионный спектр, в котором эмиссионные линии обычно образуют кластеры с постоянным соотношением интенсивностей внутри кластера.
Комбинированные методы дают дополняющую друг друга информацию, позволяющую произвести правильную идентификации веществ, которые не могут быть опознаны с помощью какого- либо одного метода.[11-12]
Глава 3. Примеры применения хроматографии в анализе объектов окружающей среды
Анализ состояния водной среды с помощью метода газовой хроматографии[13-15]
Метод газовой хроматографии для анализа состояния водной среды все шире проникает из области научного эксперимента в сферы, непосредственно связанные со многими сторонами жизни человека.
В большинстве случаев термин "водная среда" относят к различным водным объектам, находящимся вне организма человека - к морским и речным водам, иным поверхностным водам суши, подземным водам, промышленным и бытовым стокам, атмосферным осадкам, наконец, к пищевым водам (схема 1). Все эти группы объектов было бы правильнее называть "внешней водной средой".
Схема 1
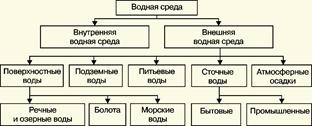
В связи с тем, что в организме человека, как и многих других живых существ, по крайней мере 80% приходится на долю воды, правомерно говорить о "внутренней водной среде" и о соответствующих объектах анализа. Эта категория объектов включает гомогенизаты и экстракты тканей различных органов и биологические жидкости, к числу которых относятся плазма крови, лимфа, слюна, моча, желчь, желудочный сок, спинно-мозговая жидкость и другие (схема 2). Как в первой, так и во второй группе объектов в анализируемых пробах могут присутствовать весьма разнообразные вещества, детальный анализ которых требует применения различных аналитических методов. Так, например, растворенные газы в морских и подземных водах, а также и в крови человека, определяют с помощью спектральных методов и в ряде случаев с помощью газовой хроматографии. Металлы, присутствующие в водных объектах, анализируют с помощью атомной абсорбционной спектроскопии или эмиссионной спектроскопии с индуктивно связанной плазмой. Очень малые следовые примеси многих элементов в водной среде определяют с помощью радиоактивационного анализа, а состав присутствующих в водной среде анионных составляющих анализируют методом ионной хроматографии.
Схема 2
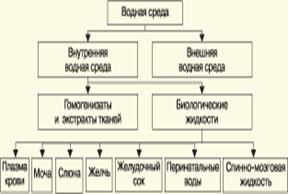
Высокомолекулярные полимерные вещества, присутствующие в водной пробе (гуминовые и фульвиновые кислоты во внешних природных водах, белковые компоненты и нуклеиновые кислоты в плазме крови), определяют методами жидкостной хроматографии - эксклюзионной, тонкослойной и высокоэффективной жидкостной хроматографии (схема 3).
Схема 3
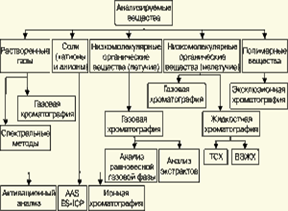
Однако очень большое число низкомолекулярных летучих органических соединений, способных переходить в парообразное состояние без разложения, анализируют и определяют количественно с помощью метода газовой хроматографии (схема 4). При этом собственно газохроматографическому определению может предшествовать операция извлечения анализируемых компонентов из водной пробы, их концентрирование и в ряде случаев перевод в их производные, обладающие более высокой летучестью либо меньшей полярностью, чем исходные соединения, и потому более пригодные для анализа с помощью газовой хроматографии (например, органические кислоты обычно переводят в их метиловые эфиры, аминокислоты - в алкиловые эфиры N-трифторацетильных производных и т.п.). Таким образом оказывается возможным использовать метод газовой хроматографии для определения тех органических веществ, которые в принципе не переходят в пар без разложения вследствие своей высокой полярности или малой термической устойчивости (например, углеводы).
Схема 4
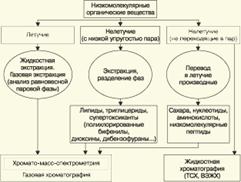
Метод газовой хроматографии уже в течение достаточно длительного времени является общепризнанным способом анализа летучих органических компонентов и следовых примесей водной среды. Опубликованы многочисленные монографии и оригинальные статьи, описывающие особенности применения метода газовой хроматографии к анализу тех или иных водных объектов.
Как и любой другой аналитический метод, газовая хроматография может дать корректную объективную информацию о составе водных объектов при условии достаточно правильного выполнения предварительных операций по отбору представительных проб анализируемых вод, извлечения и концентрирования подлежащих определению компонентов и их групп и ввода их в хроматографическую систему.
Объектами газохроматографического определения в водных средах могут быть растворенные газы и органические соединения с молекулярной массой от 16-30 (метан, этан) до 400-500 и более. Состав примесей может довольно быстро изменяться вследствие целого ряда причин. Поэтому время от момента отбора проб до выполнения анализа или предшествующих ему операций, обеспечивающих консервацию их состава, должно быть по возможности малым.
Причины изменения состава примесей водной среды, определяемых с помощью газовой хроматографии, могут включать следующие процессы:
а) потери растворенных газов и наиболее легколетучих органических компонентов вследствие изменений температуры и давления (например, при нагреве водной пробы от исходной температуры водоисточника до температуры лабораторного помещения);
б) исчезновение некоторых подлежащих определению примесных компонентов водных проб в результате химических и микробиологических процессов при хранении до проведения анализа (окисление альдегидов и тиолов, гидролиз ацеталей и галогенопроизводных, микробиологическое расщепление углеводородов нефти и др.);
в) загрязнение проб примесями, извлекаемыми из полимерной тары, используемой при отборе проб и их последующей транспортировке и хранении (пластификаторы, низкомолекулярные компоненты полимеров и т.п.);
г) загрязнение проб примесями, содержащимися в применяемых для экстракции растворителях;
д) изменение проб в испарителях и колонках применяемых хроматографических систем.
Правильно организованный газохроматографический анализ должен в возможно более полной степени исключить все перечисленные выше причины изменения состава анализируемых проб. Этой цели служат многочисленные методики анализа, опубликованные в оригинальных работах, а в ряде случаев и включенные в нормативные документы.
Для извлечения определяемых компонентов из водных матриц применяют методы экстракции малыми объемами органических растворителей с последующим концентрированием путем отгонки экстрагента (рис. 1); твердофазной экстракции с сорбцией определяемых компонентов на адсорбентах с привитой органической неподвижной фазой (углеводородными радикалами от С2H5 до С20Н41, либо функционально замещенными фрагментами с нитрильными, аминными или диольными группами). Разработаны методы микроэкстракции на единичном стеклянном или кварцевом волокне, покрытом пленкой полисилоксановой неподвижной фазы.
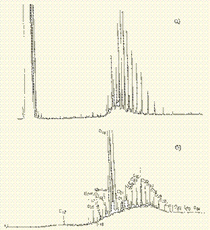
Рис. 1. Типичные хроматограммы нефтяных загрязнений, экстрагированных из воды Таганрогского залива: а) - август 1991 г.; б) - октябрь 1991 г.
В пробу анализируемой воды объемом около 100 мл (в конической колбе) помещают магнитную мешалку в форме стеклянной трубки длиной 30 мм и диаметром 2-3 мм с запаянными концами. Внутрь трубки помещают стальной стержень длиной 25 мм и диаметром 1-1,5 мм, а снаружи на трубку надевают отрезок трубки из силиконовой резины длиной 25-30 мм с внутренним диаметром 1 мм и толщиной стенок 0,5 мм. Согласно опубликованным данным перемешивание водной пробы такой мешалкой со скоростью несколько сотен оборотов в минуту в течение 10-15 мин при 20 °С приводит к тому, что более 90% всех липофильных примесей абсорбируется в силиконовой оболочке мешалки. После этого мешалку можно поместить в нагретый испаритель хроматографа для немедленного проведения анализа либо сохранить ее длительное время в закрытой пробирке для транспортировки в стационарную лабораторию.
Подобная техника извлечения и концентрирования малых примесей, названная авторами Stir Bar Sorptive Extraction, несомненно, имеет серьезные перспективы широкого применения. Возможно, что использование таких магнитных мешалок с полимерными покрытиями разных типов позволит избирательно извлекать из водных проб различные группы соединений, отличающиеся по своей полярности и прочим физико-химическим характеристикам.
Для определения состава легколетучих компонентов водных проб оказывается плодотворным метод газохроматографического анализа равновесного пара и газовой экстракции с улавливанием извлекаемых веществ в сорбционных концентраторах и последующим криогенным вводом в капиллярную колонку. Таким способом, например, подробно изучен состав хлорсодержащих микропримесей, образующихся при хлорировании питьевой воды (рис. 2). При извлечении микропримесей полярных веществ, хорошо растворимых в воде, применяют метод экстракции полярными водорастворимыми экстрагентами (спиртом, ацетоном) с предварительным насыщением водных проб неорганическими солями (высаливание хлоридом натрия или сульфатом аммония).
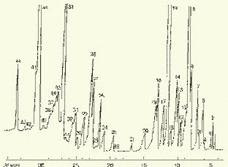
Рис. 2. Хроматограмма летучих органических соединений, содержащихся в пробе хлорированной питьевой воды. Капиллярная колонка длиной 50 м и диаметром 0,25 мм с силиконовой смазкой "Эдвардс" в качестве неподвижной фазы. Пики, обозначенные цифрами, идентифицированы. Пик 9 – хлороформ
Собственно газохроматографический анализ в большинстве случаев в настоящее время осуществляют с применением высокоэффективных капиллярных колонок в условиях программирования температуры от 50-100 °С до 300-350 °С (и даже до 400 °С и выше). Скорость нагрева колонок при этом может изменяться от 3-5 до 20-30 град/мин в зависимости от характера разделяемых компонентов.
Идентификацию пиков на хроматограммах выполняют с применением известных хроматографических зависимостей индексов удерживания от температур кипения и от молекулярной массы веществ. Для той же цели применяют селективные детекторы (например, электронно-захватный), термоионные хемилюминесцентные, атомно-абсорбционные, масс-селективные и др.
Наиболее полную информацию о молекулярном строении определяемых веществ позволяют получить методы хромато-масс-спектрометрии и газовой хроматографии с ИК-Фурье спектроскопическим детектором. Особенно плодотворным оказалось использование этих двух методов при определении пестицидов, полихлорированных бифенилов, диоксинов и им подобных веществ, продуктов распада токсичных ракетных топлив и боевых отравляющих веществ в объектах окружающей среды (рис. 3).
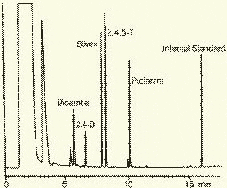
Рис. 3. Хроматограмма воды реки Оук Крик (США), содержащей пестициды: 1 - Дикамба (4,7 мкг/л); 2 - 2,4-D (7,0 мкг/л); 3 - Силвекс (4,5 мкг/л); 4 - 2,4,5-Т (5,2 мкг/л); 5 - Пиклорам (3,3 мкг/л); 6 - внутренний стандарт
В ряде случаев применение селективных детектирующих систем позволяет не только повысить чувствительность определения целевых компонентов, но и выявить источники загрязнения водной среды. Так, например, применение хемилюминесцентного озонового детектора с высокой специфической чувствительностью к веществам, содержащим серу, позволяет зафиксировать профиль серосодержащих соединений нефти и нефтяных топлив. Эти компоненты значительно более устойчивы в водной среде, чем углеводородные составляющие нефтепродуктов, поэтому совпадение таких профилей позволяет с большой степенью достоверности указать источник нефтяного загрязнения данного водного бассейна (рис. 4), .
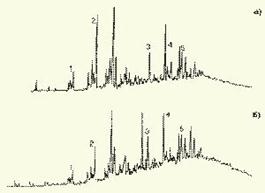
Рис. 4. Хроматограммы: а) - серосодержащих компонентов нефтяного загрязнения морской воды (район г. Таганрога); б) - судового дизельного топлива.
Кварцевая капиллярная колонка длиной 25 м и диаметром 0,25 мм с полидиметилсилоксаном SE-54 в качестве неподвижной фазы. Программирование температуры от 60 до 280 °C cо cкоростью нагрева 10 град/мин: 1 - метилбензотиофены; 2 - диметилбензотиофены; 3 - дибензотиофен; 4 - метилдибензотиофены; 5 – диметилдибензотиофены
Большие возможности газохроматографического анализа в настоящее время определенно позволяют осуществить достаточно полный анализ водных проб практически любого происхождения, в том числе питьевых, речных, озерных и морских вод, сточных вод коммунальных систем и промышленных предприятий.
В ряде случаев такие анализы могут быть проведены в полевых условиях непосредственно в местах отбора проб. Тем не менее, пока не существует методов, позволяющих провести полный анализ водных проб в единой системе без проведения предварительных лабораторных операций, часто трудоемких и длительных.
Перспективными для создания таких методов следует считать хроматографические системы с использованием в качестве подвижных фаз парообразных и сверхкритических сред (в том числе паров воды).
Широко используется газовая хроматография также и для анализа объектов внутренней водной среды. При этом применяется весь арсенал технических приемов, разработанных за 50 лет развития газовой хроматографии: высокоэффективные капиллярные колонки, высокочувствительные селективные детекторы, комбинированные аналитические системы, сочетающие газовую хроматографию с масс-спектрометрией и с ИК-спектроскопией с Фурье-преобразованием.
В этой области сложились два основных направления аналитических исследований. С одной стороны, это изучение состава естественных сред организма (плазмы крови, мочи, слюны, спинно-мозговой жидкости и др.) с целью выявления изменений этого состава в зависимости от физиологических особенностей организма, наличия патологических изменений и тому подобных факторов.
В настоящее время это направление газохроматографического анализа внутренней водной среды организма отражено в ряде руководств и монографий. Показано, что во многих случаях газохроматографический анализ позволяет выявить на ранней стадии целый ряд заболеваний и таким образом ускорить их лечение (рис. 5). При таких исследованиях широко используют экстракцию целевых компонентов растворителями, твердофазную экстракцию и метод анализа равновесного пара (рис. 6).
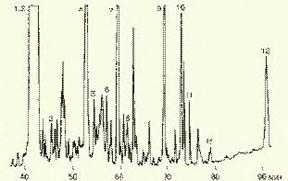
Рис. 5. Метаболический профиль стероидов из мочи пациента с опухолью яичника, секретирующей тестостерон. Идентифицированы все компоненты. Увеличенное содержание компонентов 1, 2, 4 и 7 указывает на наличие опухоли (1 - андростерон; 2 - этиохоланон; 4 - 11b-оксиандростерон; 7 - прегнантриол)

Рис 6. Хроматограмма летучих органических соединений мочи, полученная на капиллярной колонке с полисилоксановой неподвижной фазой БС-2 в условиях программирования температуры: 1 - ацетон; 3 - этанол; 6 - 2-пентанон; 7 - н-пропанол; 10 - диметилдисульфид;13 - 4-гептанон; 14 - н-бутанол; 15 - 2-гептанон; 29 - пиррол; 45 – карвон
Вторым важным направлением в анализе объектов внутренней водной среды является выявление чужеродных для организма соединений (фармацевтических препаратов, разного рода ядов, алкоголя, других наркотических веществ и т.п.). Так, применение высокочувствительного термоаэрозольного детектора, избирательно регистрирующего азотсодержащие соединения, позволило регистрировать противосудорожные лекарственные средства в крови детей, больных эпилепсией, даже через 3-5 дней после их применения (рис. 7). Аналогично, с помощью селективного термоионного детектора с высокой чувствительностью регистрировали в плазме крови наличие анестезирующего препарата кетамина, находящего, к сожалению, довольно широкое применение в качестве галлюциногенного наркотика (рис. 8).
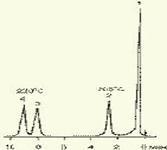
Рис. 7. Хроматограмма 0,1% раствора противоэпилептических лекарственных средств. Кварцевая капиллярная колонка длиной 10 м и диаметром 0,25 мм с полисилоксаном OV-17 в качестве неподвижной фазы: 1 - этанол; 2 - фенобарбитал; 3 - гексамидин; 4- дифенин

Рис. 8. Хроматограмма смеси компонентов плазмы крови, содержащей кетамин: а) - пламенно-ионизационный детектор; б) - термоионный детектор; 1 - кетамин; 2 - внутренний стандарт
Подобным же способом при газохроматографическом анализе проб плазмы крови, мочи или слюны могут быть определены несколько сотен других наркотиков, веществ, используемых в качестве допинга в спортивных соревнованиях, и анаболических стероидов, запрещенных к употреблению международными спортивными организациями.
Все перечисленные выше достижения газохроматографического метода в области анализа объектов водной среды все шире проникают из области научного эксперимента в сферы, непосредственно связанные с многими сторонами жизни современного общества. К таким областям можно отнести изучение состояния окружающей среды, контроль качества питьевой воды, сельскохозяйственной продукции и пищевых продуктов, клиническую медицину, криминалистику и ряд других.
Определение полиароматических углеводородов в объектах окружающей среды методами жидкостной и тонкослойной хроматографии[14]
Было определено содержание полиароматических углеводородов (ПАУ), в частности, бенз(а)пирена в снежном покрове. Пробоподготовку осуществляли экстракцией диэтиловым эфиром. Качественный анализ осуществляли методом тонкослойной хроматографии. Пробы наносили на пластину Silufol UV-254 и осуществляли хроматографический анализ в двух системах: система 1 - раствор кофеина в хлороформе; система 2 - смесь циклогексана и н-гексана. Использование системы 1 позволило снизить нижний предел обнаружения.
Количественный анализ осуществляли методом газожидкостной хроматографии (ГЖХ). Исследование проводили на хроматографе «Цвет-500» с пламенно-ионизационным детектором. В качестве сорбента использовали силиконовый каучук SE-54 с нанесенной на него неподвижной фазой OV-101. Анализ проводили в режиме программирования температуры от 200 до 310 С со скоростью 4 С /мин. В качестве газа-носителя использовали азот. Метод позволил определить ПАУ на уровне ПДК.
Глава 4. Современное аппаратурное оформление

Портативные хроматографы Agilent Micro-GC
Портативные газовые хроматографы (ГХ), занимая существенно меньше места по сравнению с лабораторными газовыми хроматографами, обеспечивают при этом сопоставимое качество анализов. Небольшие, размером с коробку из-под ботинок, Микро газовый хроматограф позволяют анализировать компоненты в концентрациях порядка одна часть на миллион (ррт) за несколько секунд - в десятки раз быстрее, чем обычные лабораторные газовые хроматографы. Микро газовые хроматографы предназначены для анализа газовых смесей или веществ с низкой температурой кипения (до 90 С) непосредственно в цехах, "у реактора". В корпус газового хроматографа с наибольшим размером 46 см помещаются до 4 хроматографических модулей. Микро газовый хроматограф характеризуется высокой производительностью его легко переносить, он быстро приводится в рабочее состояние. Это идеальный хроматограф, для получения быстрых результатов, например, при контролировании процессов в опытных установках, или, когда необходимо убедиться в однородности множества образцов газовых смесей. Использование модема позволяет передавать информацию, полученную от микро газового хроматографа по телефонным линиям на большие расстояния.
Революционное повышение производительности газового хроматографа
Миниатюризация инжекторов и детектора по теплопроводности обусловила использование в микро газовом хроматографе коротких и очень тонких капиллярных колонок, что более повысило эффективность процесса разделения. Это дает возможность проанализировать, например, природный газ (СГС10) за время не более 150 сек, смеси неорганических газов с серосодержащими газами - менее чем за 30 сек, смеси легколетучих соединений -за 50 сек, а сложную смесь нефтезаводских газов -за 160 сек. Наличие миниатюрной схемы разделения с обратной продувкой позволяет микро газовому хроматографу анализировать смеси, содержащие тяжелые компоненты, и быть готовым к началу следующего такого анализа уже через 2-3 минуты. Сокращение времени анализа в десятки раз приводит к революционному скачку в повышении производительности труда, помогает быстрее принимать правильные решения на производстве.
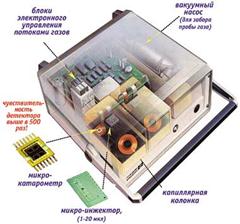
Микро-технология на монокристаллах кремния
Благодаря развитию микротехнологии в производстве газового хроматографа основные его узлы изготавливаются на основе монокристаллического кремния: инжектор с вентилями, система обратной продувки и универсальный детектор по теплопроводности. Эти основные узлы, а также колонка сравнения и рабочая колонка и термостат собраны в один механический прочный высокопроизводительный модуль.
Каждый газовый хроматограф может быть составлен из нескольких (до четырех) независимо управляемых модулей, сочетающих высокую скорость анализа с точностью результатов, требуемых в промышленности. Отсутствие подвижных частей в инжекторе делает всю систему исключительно надежной и долговечной.
Десять компонентов – менее чем за 120 сек!

Литература
1. Жуховицкий А.А., Туркельтауб Н.М. Газовая хроматография. М.: Гостоптехиздат, 1962, 240 с.
2. Сакодынский К.И., Киселев А.В., Иогансен А.В. и др. Физико-химическое применение газовой хроматографии. М.: Химия, 1973. - 254 с.
3. Жидкостная колоночная хроматография. В 3 т. / Под ред. З.Дейла, К.Мацека, Я.Янака. М.: Мир, 1972. – 439с.
4. Березкин В.Г., Алишоев В.Р., Немировская И.Б. Газовая хроматография в химии полимеров. М.: Наука, 1972. - 287 с.
5. Морозов А.А. Хроматография в неорганическом анализе. М.: Высш. шк., 1972. - 233 с.
6. Березкин В.Г., Бочков А.С. Количественная тонкослойная хроматография. М.: Наука, 1980. - 183 с.
7. Лабораторное руководство по хроматографическим и смежным методам. В 2 т. / Под ред. О.Микеш. М.: Мир, 1982, т. 1–2, 783 с.
8. Кирхнер Ю. Тонкослойная хроматография. В 2 т. М.: Мир, 1981, т. 1, 615 с.; т. 2. - 523 с.
9. Экстракционная хроматография. / Под ред. Т.Браун, Г.Герсини. - М.: Мир, 1978. - 627 с.
10. Скуг Д., Уэст Д. Основы аналитической химии / Пер. с англ. В 2 т. М.: Мир, 1979. – 324с.
11. Гольдберг К.А., Вигдергауз М.С. Введение в газовую хроматографию. М.: Химия, 1990. – 278с.
12. Хмельницкий Р.А., Бродский Е.С. Хромато-масс-спектрометрия. М.: Химия, 1983. – 280с.
13. Горелик Д.О., Конопелько Л.А., Панков Э.Д. Экологический мониторинг. В 2 т. СПб.: Крисмас, 2002. – 457с.
14. Назаркина С.Г. Определение полиароматических углеводородов в объектах окружающей среды методами жидкостной и тонкослойной хроматографии.
15. Хроматографический анализ окружающей среды. / Под ред. Р.Гроба. М.: Мир, 1979. - 606 с.
Похожие работы
... была определена концентрация 42 элементов в образцах биомониторов как из загрязненных, так и из фоновых районов [6-8]. Анализ объектов окружающей среды (мониторинг рабочих мест и здоровье персонала, занятого в производстве фосфорных удобрений) с помощью ядерно-физических методов - НАА в комбинации с атомной абсорбцией и рентгено-флюоресцентным анализом - проводится в рамках координационной ...
... Возможность проведения дифференцированного титрования смесей электролитов, что невозможно при титровании с визуальной индикацией конечной точки титрования.[1–3] 2. Примеры использования кондуктометрии в анализе объектов окружающей среды Экспресс методы контроля качества сырья, параметров технологических процессов и готовой продукции в сыроделии [4–8] В сыродельной промышленности, ...
... -аналитических исследованиях в органической химии, нефтехимии, биохимии, медицине, фармакологии, для охраны окружающей среды и др. [16] 3. Использование хромато – масс – спектрометрии в идентификации загрязнителей природных сред Возможности хромато-масс-спектрометрии по идентификации сточных вод и отходов накопителей промпредприятий были проверены на объектах г. Днепропетровска. С разной ...
... НДМГ (0,02– 10,0 мкг/мл) в растворе ацетата натрия требуется применение экстракционно-фотометрического метода (рис. 10). Рисунок 10 – Схема анализа воздуха на содержание НДМГ Определение несимметричного диметилгидразина методом инверсионной вольтамперометрии Одним из преимуществ электрохимических методов анализа в случае определения НДМГ является то, что из-за ионизации молекул данного вещества ...


0 комментариев