Навигация
Обоснование комплексонометрического метода
1.4.2 Обоснование комплексонометрического метода
Введение комплексонов в аналитическую практику расширило возможности химического анализа вообще и объемного метода в частности.
Наиболее ценным свойством комплексонов, широко используемым в анализе, является их способность давать внутрикомплексные соли с ионами щелочноземельных металлов: магнием, кальцием и барием, которые, как известно, трудно или невозможно перевести в комплексные соединения другими средствами.
Комплексы, образуемые комплексонами с большинством катионов металлов, весьма устойчивы, что вполне обеспечивает практически полное связывание определяемого металла в комплекс.
Объемно – аналитические методы анализа отличаются простотой, скоростью, что имеет решающее значение в практике промышленных лабораторий. Но до введения комплексонов объемно-аналитическими методами можно было определять лишь ограниченное число металлов. Комплексоны же позволяют определять объемными методами почти все металлы. Только ЭДТА образует комплексы с 44 катионами, из которых только Ag+, Нg2+, Ва2+ и катионы щелочных металлов обычно комплексонометрически не определяются.
Большим достоинством комплексонов является то, что в ряде случаев представляется возможность титровать одни катионы в присутствии других, не прибегая к предварительному их разделению.
Комплексоны, являясь кислотами или их кислыми солями, при взаимодействии с катионами независимо от их степени окисления образуют ионы водорода, например:
Са2+ + Н2Y2- → СаY2- + 2Н+
Поэтому титрование комплексонами можно проводить по методу нейтрализации, пользуясь кислотно-основными индикаторами.
Комплексонометрически можно определять не только катионы, но и анионы. Например, фосфат-ион в анализируемом растворе можно осадить солью магния, отделить осадок, растворить и в полученном растворе оттитровать магний рабочим раствором комплексона.
Комплексонометрия предъявляет высокие требования к чистоте применяемых реактивов и дистиллированной воды, в качестве которой лучше применять бидистиллят, полученный в аппарате из химически стойкого стекла.
Аналитические свойства комплексонов не исчерпываются применением их в объемном анализе. Они позволяют облегчить выполнение многих определений и в гравиметрическом анализе, так как могут связывать мешающие ионы в практически недиссоциированные комплексы, освобождая аналитика от отделения их осаждением.
В заключение обзора аналитических свойств комплексонов следует отметить их применимость и в физико-химических методах анализа – в фотометрии, потенциометрии, полярографии и др.
1.5 Теоретические основы комплексонометрического метода
В основе метода комплексонометрии лежит образование комплексных соединений анализируемых катионов с органическими реагентами – комплексонами.
В комплексонометрическом анализе в качестве рабочего вещества чаще всего используют трилон Б.
Трилон Б
![]()
![]() NaООССН2 СН2СООН
NaООССН2 СН2СООН
![]()
![]() N-СН2-СН2-N
N-СН2-СН2-N
НООССН2 СН2СООNa
С6Н12N2(СООН)2(СООNа)2 ·2Н2О
Трилоном Б называется двузамещенная натриевая соль органической этилендиаминотетрауксусной кислоты.
Трилон Б – это фирменное название вещества; его называют также хелатон, версен, комплексон III.
Сокращенное обозначение молекулы трилона Б: Na2Н2Тр.
Это соединение легко образует прочные внутрикомплексные соли со многими катионами. Соли образуются, с одной стороны, за счет замещения металлом водорода карбоксильных групп, с другой – за счет образования координационных связей между ионами металла и атомами азота.
При комплексонометрическом титровании к раствору, содержащему определяемые ионы, добавляют постепенно титрованный раствор комплексона. По мере титрования определяемые ионы связываются в комплекс, и в точке эквивалентности они практически отсутствуют в растворе. Реакцию в общем виде можно записать так:
Mg2+ + Na2H2Tp = Na2MgTp + 2H+
Чтобы реакция комплексообразования шла до конца, нужно связать выделяющиеся ионы водорода. Поэтому при титровании к анализируемому раствору добавляют смесь хлорида и гидроксида аммония – аммиачно-буферный раствор.
Для определения момента окончания титрования служат индикаторы – вещества, образующие окрашенные соединения с ионами кальция и магния или с одним из этих катионов. Такими индикаторами являются кислотный хром синий К, дающий переход от розовой к серо–голубой окраске при рН=10-11; магнезон и эриохром черный Т, называемый также хромом черным специальным ЕТ00, изменяющие окраску от вино–красной к синей; мурексид и др.
Индикаторы обладают различной чувствительностью, т.е. их окрашенные соединения с ионами кальция и магния возникают при различных, но определенных для данного индикатора и для выбранных условий концентрациях этих ионов (табл.1.1). Например, эриохром черный Т образует окрашенное соединение с кальцием при концентрации этого иона около 7 мкг – экв/л; по отношению к ионам магния этот индикатор более чувствителен, и окраска возникает уже при 4 – 5 мкг-экв/л.
Таблица 1.1.
Чувствительность индикатора при определении жесткости Трилоном Б
| Индикатор | Четкая окраска отмечается при концентрации, мкг-экв/л | Значение рН | |
| Са2+ | Мg2+ | ||
| Эриохром черный Т | 7 | 4 – 5 | 8 – 10 |
| Кислотный хром темно-синий | 2 | 1 | 9 – 10 |
| Кислотный хром синий К | 2 | 1 | 8 – 10 |
| Кислотный однохром синий | 4 | 1 | 9 – 10 |
| Мурексид | 1 | — | 10 |
В таблице 1.1 приведены концентрации ионов, при которых окраска изменяется достаточно четко и при титровании визуально хорошо отмечается.
В то же время, если взять ряд растворов с различной концентрацией магния, например 0; 0,2; 0,5; 0,7; 1,0; 1,5 мкг – экв/л, то при добавлении к таким растворам индикатора хром темно–синего или хром синего К визуально можно различить разницу в оттенках получающихся окрасок.
Таким способом можно определять визуальным колориметрированием малые величины жесткости. Для повышения чувствительности следует только предварительно превратить кальциевую жесткость в магниевую. Это можно выполнить, добавляя в анализируемую жидкость раствор трилоната магния. Поскольку комплекс с кальцием имеет большую прочность (табл.1.1), то будет протекать реакция:
Са2+ + Na2MgТр.→ Mg2+ + Na2СаТр.
и ионы кальция будут заменены в анализируемой воде ионами магния в эквивалентном отношении.
Устойчивость комплекса существенно зависит от рН раствора. Поэтому комплексонометрическое титрование ведут в заданном интервале рН, используя различные буферные растворы.
Методом комплексонометрии можно определить катионы магния, кальция, цинка, алюминия, бария, свинца и многие другие – более 40 различных катионов. Этот метод широко применяется для определения жесткости воды.
1.6 Методика определения жесткости воды комплексонометрическим методом
1.6.1 Сущность метода
Метод основан на образовании при рН=10±0,2 прочного бесцветного комплексного соединения трилона Б с ионами кальция и магния. В эквивалентной точке титрования все ионы кальция и магния связываются в комплексное соединение трилоном Б, в результате чего происходит изменение окраски индикатора от красной до голубой.
Чувствительность метода составляет 0,5 мг – экв/л при титровании 0,1н
Похожие работы
... красного окрашивания раствора не наблюдаем, следовательно анион NO2-действительно в данной смеси отсутствует. Качественные реакции на анионы третьей аналитической группы Подтвердим присутствие в анализируемом веществе аниона NO3-. Проведем следующую реакцию: к нескольким каплям раствора неизвестного вещества прибавим 2-3 капли дефениламина и 5 капель концентрированной серной кислоты. Наблюдается ...
... водорода. Именно так может диссоциировать и ион NH4: NH4+ NH3+H+ Реакция же -2e Mg0 + 2HCl=Mg+2Cl2+H02 2H++Mg Mg2++ H02 При нагревании магния в атмосфере галогенов происходит воспламенение и образование галоидных солей. -2e Mg + Cl20 Mg+2+Cl2- Причина воспламенения - очень большое тепловыделение, как и в ...
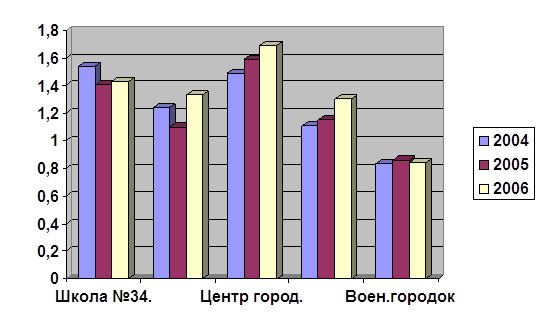
... 1 2 3 1 Очень чистая < 0,2 2 Чистая 0,2-1,0 3 Умеренно загрязненная 1,0-2,0 4 Загрязненная 2,0-4,0 5 Грязная 4,0-6,0 6 Очень грязная 6,0-10,0 7 Чрезвычайно грязная > 10 Глава 3 Определение некоторых показателей качества питьевой воды в различных районах г.Южно-Сахалинска и их сравнительный анализ 3.1 Показатели качества питьевой воды в различных районах г.Южно ...
... ;à НbО2- + ННb + СО2 Кислотно-основные свойства лигандов, связанных с комплексообразователем, часто выражены более ярко, чем кислотно-основные свойства свободных лигандов. 4. Комплексные соединения в аналитической химии 4.1 Качественный анализ катионов Первая группа катионов В первую аналитическую группу катионов входят ионов калия K+, натрия Na+, аммония NH4+ и магния Mg2+. ...
0 комментариев