Навигация
Обзор источников образования тяжелых металлов
Обзор ИСТОЧНИКов ОБРАЗОВАНИЯ ТЯЖЕЛЫХ МЕТАЛЛОВ
Содержание
ВВЕДЕНИЕ
1. ХАРАКТЕРИСТИКА ИСТОЧНИКОВ ЗАГРЯЗНЕНИЯ
2. ОСНОВНЫЕ СОЕДИНЕНИЯ ТЯЖЕЛЫХ МЕТАЛЛОВ В ПРОМЫШЛЕННОСТИ
2.1 ХРОМ
2.2 МАРГАНЕЦ
2.3 НИКЕЛЬ
2.4 КАДМИЙ
2.5 ЦИНК
2.6 ВОЛЬФРАМ
2.7 КОБАЛЬТ
2.8 ОЛОВО
2.9 РТУТЬ
2.10 СВИНЕЦ
2.11 СУРЬМА
2.12 МОЛИБДЕН
ЗАКЛЮЧЕНИЕ
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ
ВВЕДЕНИЕ
Тяжелые металлы применяются во многих отраслях промышленности, таких как металлургия, химическая технология, электрохимия, резиновая, текстильная, фарфоровая и другие. В производственных процессах с их использованием возможно образование сточных вод и твердых отходов с содержанием тяжелых металлов и соединений, а также выделение их в виде аэрозолей и летучих газообразных соединений превышающем допустимые нормативы. Следует учитывать и возможность загрязнения воздуха, воды водоемов, грунта и подземных вод вследствие накопления твердых отходов на свалках, шламонакопителях, а также при их уничтожении.
Практически все тяжелые металлы или их соединения ядовиты, токсичны, имеют низкие предельно допустимые показатели, поэтому разработки по переработке, утилизации и предотвращению образования токсичных отходов (безотходные технологии) имеют важное экологическое значение.
Существуют технологии и предложения по уменьшению содержания тяжелых металлов и их соединений в промышленных отходах. Так, например, для переработки свинецсодержащего сырья в основном применяют схему: спекание мелких свинцовых отходов, плавка агломерата совместно с аккумуляторным ломом и кусковыми отходами в шахтной печи. Такая технология обеспечивает применение высокопроизводительных металлургических агрегатов, переработку всех видов сырья и комплексное извлечение из него цветных металлов.[1]
Переработка никельсодержащих отходов является малоизученной и слаборазработанной, так электрохимические отходы ранее направляли на никелевые заводы, где их перерабатывали в конвертерах. В связи с тонкодисперсностью отходов и повышенным содержанием в них хлористого натрия извлечение никеля и кобальта не превышало 50 %. Это обстоятельство явилось основной причиной отказа никелевых предприятий от переработки таких отходов.
Вольфрамоникелевые катализаторы перерабатывают на электрометаллургическом комбинате путем подшихтовки их к основному сырью для получения ферровольфрама, при этом никель является вредной примесью и не извлекается.
Отходы луженой жести перерабатывают как в местах образования (на предприятиях мясомолочной, рыбной, пищевой промышленности), так и на предприятиях цветной металлургии. Последние для получения олова используют также луженый лом (банки, фляги). Регенерацию олова из луженых отходов и лома осуществляют методом электролиза в щелочном растворе по трем технологическим схемам — электролиз с растворимым анодом, электролиз с нерастворимым анодом и предварительным химическим снятием олова, электролиз по «совмещенной схеме».
Вторичное ртутьсодержащее сырье перерабатывают централизованно на одном из предприятий редкометалльной промышленности. По характеру переработки его подразделяют на три категории:
- сырье, перерабатываемое по существующей на предприятии технологической схеме для первичного сырья;
- материалы, требующие механического извлечения ртути;
- сырье, требующее специальной обработки.
Значительное количество отходов химической промышленности не используются из-за отсутствия специализированных мощностей для их переработки. При переработке цинксодержащих железных руд на ряде предприятий черной металлургии при очистке газов доменного и мартеновского производства образуются шламы, которые складируются на больших земельных площадях, что наносит урон не только плодородным почвам, но и окружающей среде в целом, а также является экономически не рентабельно.[2]
Таким образом, остро стоит проблема переработки и утилизации отходов содержащих соединения тяжелых металлов. Для разработки и внедрения технологий, решающих выше указанные проблемы, необходимы данные по содержанию тех или иных соединений в отходах, их количество и свойства, а также объемы образующихся отходов.
1. ХАРАКТЕРИСТИКА ИСТОЧНИКОВ ЗАГРЯЗНЕНИЯ
Как было сказано выше в различных производствах возможно образование твердых отходов и сточных вод, содержащих тяжелые металлы и их соединения, которые загрязняют окружающую среду. Некоторые твердые отходы могут быть использованы как вторичное сырье, а также возможна очистка сточных вод от солей тяжелых металлов.
1.1 Вторичное свинецсодержащее сырье состоит из лома свинцовых аккумуляторов (около 70%), лома деталей агрегатов и установок электротехнической, металлургической и химической отраслей промышленности (около 15 %) и прочих отходов (около 15 %). Заготавливаемое свинецсодержащее сырье в основном перерабатывают на специализированных заводах на сурьмянистый свинец, около 30 % сырья поступает на первичные свинцовые заводы и около 10 % — на подшихтовку при производстве баббитов и других сплавов.[3]
1.2 Для производства сурьмы и сурьмянистого свинца на специализированных заводах используют лом аккумуляторов (70—75 % свинца и до 4 % сурьмы), аккумуляторный шлам (50—80% свинца, 1,5—3 сурьмы), свинцовую изгарь (20—95% свинца, 0,3—3,5% сурьмы, 0,6—1,5% меди, 0,2—2 % цинка и 0,1—1 % олова), свинцовые пасты (30—70 % свинца). [1]
1.3 Лом и кусковые отходы цинка и гартцинка, незасоренного механическими примесями железа, в общем объеме заготовки цинксодержащего сырья занимают около 70 %, прочие цинксодержащие отходы (пыль, изгарь, шлаки, отходы химической промышленности) — около 30 %. Заготавливаемые цинксодержащие отходы в основном перерабатывают в химической промышленности, около 20 % поступает на переработку на заводы первичной и около 10 % — на заводы вторичной цветной металлургии.
Для производства цинковых белил и литопона в химической промышленности используют гартцинк (85—92 % цинка, около 3 % свинца), серую окись цинка (около 90% цинка и 4—5% углерода), изгарь (38—80 % цинка, 0,1—2 % свинца, 0,1—7,5 % меди, около 1,5 % олова) и частично нашатырные опады (до 28 % хлорида и до 38 % оксихлорида цинка).
Некоторые отходы химической промышленности — гидроокись (до 70 % цинка и около 1,5 % свинца) и углекислый цинк (20—35 % цинка, 35—40 % соды) — используют в других отраслях. Так, гидроокись применяют в качестве наполнителя изделий из асбеста, а углекислый цинк используют при производстве белой ситалловой плитки и фунгицида «Цирам». Часть гидроокиси используют для производства витерильных белил, а большое количество углекислого цинка направляют на предприятия цветной металлургии для переработки в вельц-печах.[2]
Значительное количество отходов химической промышленности — сернокислый цинк (до 85 % сульфата цинка), отработанные катализаторы (до 45—70 % цинка и 10—15 % меди), шламы вискозного производства (20—40 % цинка), нашатырные опады не используются из-за отсутствия специализированных мощностей для их переработки.
1.4 Основными видами никельсодержащего сырья являются: железоникелевые, кадмиево-никелевые аккумуляторы, электрохимические отходы, отработанные катализаторы, отходы сложнолегированных сталей на никелевой основе, лом и кусковые отходы чистого никеля.
Отходы сложнолегированных сталей заготавливают предприятия «Вторцветмет» и направляют на никелевые заводы, где из них извлекают никель и кобальт, а вольфрам, молибден и железо теряются в шлаках. Лом и кусковые отходы чистого никеля, а также отходы никелевых сплавов направляют для переработки на никелевые заводы.[1]
1.5 Вольфрамоникелевые катализаторы перерабатывают на электрометаллургическом комбинате путем подшихтовки их к основному сырью для получения ферровольфрама, при этом никель является вредной примесью и не извлекается.
Основными видами вольфрамсодержащего сырья являются отходы от производства и потребления проката, пылевидные отходы от заточки инструмента, стружка, путаная проволока, обрезь, лом шарошечных долот, быстрорежущего инструмента и т. п.
Отходы от производства и потребления проката и гнутых профилей, лом твердосплавного инструмента и прочих видов изделий, вольфрамовые катализаторы, лом, образующийся при проведении капитальных и текущих ремонтов на предприятиях автомобильной промышленности возвращают через управления Вторцветмета на соответствующие предприятия первичной металлургии.
1.6 Вторичное оловосодержащее сырье в основном (на 85 %) используют для производства сплавов, а остальное количество — для получения марочного олова. При изготовлении сплавов со свинцом применяют окисленные оловосодержащие отходы (изгарь, шламы, шлаки, скрап) и отходы свинцово-оловянных сплавов. Сплавы производят в электропечах. Для получения сплавов на медной основе используют паяные и луженые медные отходы, лом меди и медных сплавов, а также частично оловянные и свинцово-оловянные лом и отходы.
Масляный и флюсовый скрапы служат сырьем для получения олова и сплавов в местах образования — на предприятиях, производящих горячее лужение жести.
Отходы луженой жести перерабатывают как в местах образования (на предприятиях мясо-молочной, рыбной, пищевой промышленности), так и на предприятиях цветной металлургии. [4]
1.7 Вторичное ртутьсодержащее сырье перерабатывают централизованно на одном из предприятий редкометалльной промышленности. По характеру переработки его подразделяют на три категории:
- сырье, перерабатываемое по существующей на предприятии технологической схеме для первичного сырья;
- материалы, требующие механического извлечения ртути;
- сырье, требующее специальной обработки.
К сырью I категории относятся отработанные химические источники тока — ртутно-окисные элементы, шламы химических и фармацевтических заводов, черный сульфид ртути, закись и окись ртути, отходы производства ядохимикатов, содержащие диэтилртуть, этилмеркурхлорид, этилмеркурфосфат и другие ртутно-органические соединения. Батареи ртутно-окисных элементов дробят и подвергают обжигу в муфельных печах, в них же перерабатывают и другое вышеуказанное сырье, подшихтованное известью или огарком. При обжиге происходит отгонка ртути, отходящие газы очищают от пыли в циклонах и направляют в чугунные батареи конденсационной системы для конденсации паров ртути. Из конденсационной системы ртуть вместе с пылью и окалиной труб выпускают в пачуки или отстойники и перерабатывают по технологии, описанной в литературе [5].
К сырью II категории относится лом изделий электротехнической промышленности — ртутные выпрямители различных видов и другие приборы, содержащие металлическую ртуть. Основной частью этого вида сырья являются игнитроны марки ИВС-300/5. Игнитроны вскрывают на специальном станке, остальные приборы — автогенной резкой. Из вскрытых игнитронов и приборов металлическую ртуть сливают в емкости, а приборы после этого тщательно промывают водой и сдают как металлолом соответствующим организациям.
К III категории сырья относится отработанный активированный уголь производства поливинилхлорида. Уголь содержит металлическую ртуть, хлориды ртути (сулему и каломель) и хлористый водород, последний образует с водой соляную кислоту, которая разъедает чугунные конденсаторы. Поэтому уголь подвергают обесхлориванию путем его обработки щелочным раствором (расход едкого натра — 400—600 кг/т угля) при температуре до 100 °С в течение 2—3 ч. Обесхлоривание производят в емкостях, подогрев раствора — острым паром. Обработанный таким образом активированный уголь шихтуют с известью для нейтрализации оставшегося хлористого водорода и направляют на обжиг в муфельных печах.
1.8 Вторичным хромсодержащим сырьем являются хромовые катализаторы, сплавы, шлаки и хромсодержащие кеки. Имеються данные о большом количестве стоков хромовых производств, в которых содержание соединений хрома превышает предельнодопустимые концентрации. [6]
2. ОСНОВНЫЕ СОЕДИНЕНИЯ ТЯЖЕЛЫХ МЕТАЛЛОВ В ПРОМЫШЛЕННОСТИ 2.1 ХРОМ
Содержание в земной коре 0,035%, наиболее распространенным видом сырья являются хромитовые руды, феррохром (60-70% получаемого хрома), известно около 40 минералов. Применяется хром в качестве легирующей добавки к сталям. Входит в состав некоторых огнеупоров. Получается восстановлением Cr2O3 алюминием или кремнием либо электролитическим восстановлением растворов соединений Cr; феррохромом (60 – 85 % Cr) – прямым восстановлением хромовой руды.[7]
Физические и химические свойства. Твердый блестящий металл, Тпл. 1890ºС, Ткип. 2480ºС, плотность 6,92, химически мало активен, при обычных условиях устойчив к кислороду и влаге. Царская водка и HNO3 пассивируется.
Металлический хром малотоксичен, ПДК (в пересчете на CrO3) – 0,01мг/м3, Cr6+ - 0,0015мг/м3. [8]
2.1.1 Cr2O3 (окись хрома (III), зеленый крон, хромовая зелень) – применяется как сырье для получения Cr алюмотермическим методом, карбида хрома, шлифовальных паст и красок для стекла и керамики; входит в состав хромовых катализаторов. Получается восстановлением хроматов или бихроматов серой, углем, SO2, и др.; термическим разложением хромового ангидрида.
Физические и химические свойства. Темно-зеленые кристаллы. Тпл. 2235ºС, плотность 5,21, амфотерна.
2.1.2 CrO3 (окись хрома (VI), трехокись хрома, хромовый ангидрид) – встречается при хромировании, при выплавке легированных сталей, при добавлении феррохрома в шихту (выделяется в виде тумана). Применяется для электролитического хромирования; для получения Cr2O3 и др. Получается действием концентрированной H2SO4 на Na2Cr2O7 (реже на K2Cr2O7).
Физические и химические свойства. Темно-красные гигроскопические кристаллы. Тпл. 197ºС, плотность 2,8, растворимость в воде 62,58%(20ºС), 65,47%(80ºС). Сильный окислитель. При действии кислот отдает кислород и образует соли хрома.
2.1.3 Na2CrO4 (хромат натрия), K2CrO4 (хромат калия), (NH4)2CrO4 (хромат аммония) – применяются в производстве пигментов; как протрава при крашении; как окислитель в органическом синтезе, в фотографии и др. Получаются: Na2CrO4 – продукт переработки хромистого железняка на соединения хрома; K2CrO4 – действием щелочи на K2Cr2O7.
Физические и химические свойства.
Na2CrO4 желтые кристаллы. Тпл. 790ºС, плотность 2,72, растворимость в воде 80,18г/100г(19,5ºС), сильный окислитель.
K2CrO4 – желтые кристаллы. Тпл. 984ºС, плотность 2,74, растворимость в воде 63,0г/100г(20ºС), 79,2г/100г(100ºС), при действии кислот превращается в K2Cr2O7, сильный окислитель.
(NH4)2CrO4– желтые кристаллы, растворимость в воде 40,5г/100г (30ºС), 70,1г/100г(75ºС), сильный окислитель.
2.1.4 Na2Cr2O7×2H2O (бихромат натрия, хромпик натриевый), K2Cr2O7 (бихромат калия, хромпик калиевый), (NH4)2Cr2O7 (бихромат аммония) – применяются в металлообрабатывающей, кожевенной, текстильной, химической, лакокрасочной, фармацевтической, керамической, спичечной промышленности; в фотографии; для протравливания семян и др. Наиболее широкое применение имеет Na2Cr2O7×2H2O. Получаются: Na2Cr2O7 и K2Cr2O7 – окислительным обжигом хромистого железняка с содой (или поташом) и известью и обработкой полученных при этом Na2CrO4 и K2CrO4 серной кислотой или двуокисью углерода; K2Cr2O7 и (NH4)2Cr2O7 – обменным разложением Na2Cr2O7 с KCl или K2SO4 и с (NH4)2SO4.
Физические и химические свойства.
(NH4)2Cr2O7 оранжево-красные расплывающиеся кристаллы. Тпл. 356ºС, плотность 2,525, растворимость в воде 180,8г/100г (20ºС), 435,0г/100г(100ºС), при нагревании теряет воду, сильный окислитель.
K2Cr2O7 оранжево-красные кристаллы. Тпл. 185ºС, плотность 2,15, растворимость в воде 30,8г/100г (15ºС), 155,6г/100г(100ºС), при нагревании теряет воду, сильный окислитель.
2.1.5 KCr(SO4)2×12H2O(хромокалиевые квасцы), NH4Cr(SO4)2×2H2O (хромоаммониевые квасцы) – применяются для дубления кож; в текстильной промышленности; при производстве кинопленки. Получаются при смешивании горячих водных растворов сульфатов хрома и калия (или аммония); восстановлением соответствующих бихроматов сернистым газом, древесными опилками или каменноугольной смолой.
Физические и химические свойства. Фиолетовые кристаллы.
KCr(SO4)2 Тпл. 89ºС, плотность 1,83, растворимость в воде 18,3г/100г (20ºС).
NH4Cr(SO4)2×2H2O Тпл. 94ºС, плотность 1,72, растворимость в воде 2,1г/100г (20ºС), 15,7г/100г (40ºС), при обычных условиях устойчивы.
2.1.6 CrCl3(хлорид хрома (III)) – применяется для получения хрома. Получается хлорированием феррохрома или хромовой руды в присутствии угля; при действии Cl2 и Cr или на Cr2O3 с углем при 600°С.
Физические и химические свойства. Розово-фиолетовые кристаллы, плотность 3,03, раствор. в воде в присутствии восстановителей, образует многочисленные продукты с аминами, аммиаком и др.
2.1.7 CrO2Cl2 (оксохлорид хрома, хлорангидрид хромовой кислоты, хлороокись хрома) – получается действием сухого HCl на безводный CrO3 или H2SO4 на смесь K2Cr2O7 и NaCl.
Физические и химические свойства. Красная дымящая на воздухе жидкость. Тпл. –96,5ºС, Ткип. 116,7ºС, плотность 1,91(25ºС), растворяется в спирте, эфире, сильный окислитель. [7]
2.2 МАРГАНЕЦMn – применяется в металлургии (90%) для обессеривания и раскисления сталей, как легирующая добавка при производстве чугуна повышенной прочности и твердых сталей, в сплавах с цветными металлами; для создания антикоррозионных защитных покрытий на металлах. Получается восстановлением окислов Mn алюминием; электролизом водных растворов солей Mn.[9]
Физические и химические свойства. Серебристо-белый металл, на воздухе покрывается оксидной пленкой, Тпл. 1244ºС, Ткип. 2095ºС, плотность 7,44, растворяется в кислотах, взаимодействует с кислотами.[7]
2.2.1 MnO (окись марганца (II)) – встречается в природе в составе магнезита и других руд. Применяется в производстве ферритов и красок. Получается восстановлением высших окислов марганца водородом, СО.
Физические и химические свойства. Серо-зеленые кристаллы, Тпл. 1650ºС, плотность 5,18, основной оксид.
Похожие работы
... Листов Пров. 1 2 Консульт. БГТУ 7140607 2004 Н. контр. Утв. Целью данной дипломной работы является изучение сорбционных свойств мха по отношению к микроорганизмам и тяжелым металлам, а также изучение сорбционной способности системы «мох-микроорганизмы» и выявление доли участия каждого компонента этой ...
... коробки противогаза на 45 г, после чего она уже непригодна. В случае резко повышенных концентрации применяют шланговые противогазы. Применяют также специальную одежду и перчатки. 2 Гигиеническое нормирование содержания тяжелых металлов в объектах окружающей среды Ниже приведены основные сведения по нормированию содержания тяжелых металлов в воздухе, воде, почве, пищевых продуктах и кормах ...
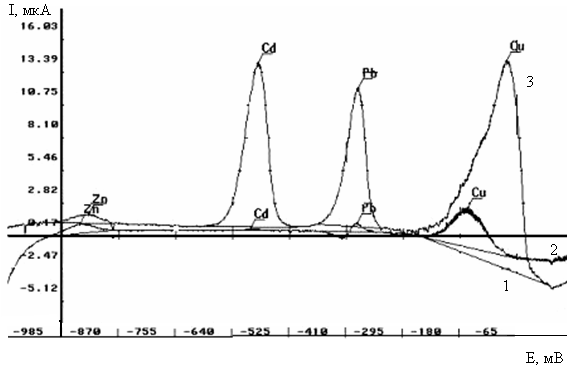
... повышения чувствительности определения мышьяка методом инверсионной вольамперометрии его обычно концентрируют на золотых и золото-графитовых электродах [28]. Работа посвящена разработке методики анализа воды на содержание мышьяка методом инверсионной вольтамперометрии с использованием золото-стеклоуглеродного электрода(ЗСУЭ), полученного методом «in situ»,что удешевляет анализ. Определены условия ...
... малая произрастает в большинстве стоячих водоемах по всей стране с разным уровнем загрязнения. Цель нашей работы следующая: Возможность использования ряски малой в качестве фиторемедиатора водоемов загрязнённых тяжелыми металлами и другими токсичными веществами. В работе были поставлены следующие задачи: 1. Возможность использование ряски малой для определения токсичности сточных вод и их ...






0 комментариев