Навигация
Г жира в день. Во многом это обусловлено сформированной в последние
150 г жира в день. Во многом это обусловлено сформированной в последние
несколько десятилетий культурой питания в сети закусочных быстрой еды - так
называемая "кафетерий-культура". Гамбургеры, чисбургеры, мороженое, жареные
пирожки, картофель фри - основные блюда таких закусочных. Все это блюда с
очень высоким содержанием жира.
Мы уже отмечали выше, что при прогрессировании ожирения наблюдается
увеличение способности организма к окислению жира. Этот феномен обусловлен
тем, что увеличенные адипоциты легче выделяют триглицериды в кровь, а при
увеличении их концентрации в крови, ткани начинают отдавать им предпочтение
в выборе субстратов для окисления. Подсчитано, что увеличение массы тела на
10 кг сопровождается усилением окисления жира на 15 - 20 г в день. Усиление
окисления жира у больных с ожирением предохраняет их от дальнейшего
нарастания массы тела делая избыток веса стабильным даже в условиях
продолжающегося чрезмерного потребления жира [Astrup et al.,. 1994].
Снижение веса в ходе диетотерапии, наоборот, сопровождается снижением
способности организма к окислению жира. Установлено, что уменьшение массы
жира на 10 кг сопровождается снижением способности к окислению жира в
среднем на 14 - 22 г в сутки [Astrup et al., 1994]. То есть, пациент,
похудевший на 20 кг для того чтобы удержать полученный результат стабильным,
должен уменьшить суточное потребление жира в среднем на 30-40 г. Так как
обычно эта величина не учитывается, ожирение рецидивирует по крайней мере в
9 случаях из 10.
Роль наследственности в развитии ожирения
Само по себе участие генетических факторов в развитии ожирения можно
считать твердо доказанным. В этом нас убеждает и существование линий
лабораторных животных с высокой частотой встречаемости ожирения, и
существование семей, частота встречаемости ожирения в которых значительно
превосходит среднюю, и наличие популяций (например, индейцы племени Пима) с
очень высокой частотой ожирения. В наследственной природе ожирения у
человека убеждает нас и близнецовый метод анализа. Частота встречаемости
ожирения в парах гомозиготных близнецов значимо выше, чем в парах
гетерозиготных [Hakala P., et al, 1999].
К наследственным по своей природе следует относить и различия в
склонности к ожирению, имеющиеся у представителей различных рас [Chitwood
L.F. et al, 1996; Albu J. B., et al, 1999]. Chitwood L.F. и соавторы [1996]
исследовали этот вопрос и обнаружили, что у черных женщин по сравнению с
белыми снижена способность к окислению жиров, более выражено участие
углеводов в окислительных процессах и более высокий уровень инсулина. Это по
мнению авторов, делает черных женщин более склонными к развитию ожирения.
Согласно современным представлениям, человека можно признать
наследственно склонным к полноте, если один из его родителей имеет
избыточный вес. Действительно, вероятность иметь ожирение в этом случае
приближается к 70-80%, тогда как в основной популяции она не превышает
25-30% [Hakala P., et al, 1999].
Несомненно участие генетических факторов в развитии ожирения в некоторых
линиях лабораторных животных. И, кажется, исследования последних лет
приближают нас к пониманию природы и интимных механизмов их участия в
патогенезе нарастания массы тела.
Так, в частности, было установлено, что ожирение у мышей линии оb/ob
определяется мутацией в ob гене. В норме этот ген кодирует белок лептин,
состоящий из 167 аминокислотных остатка, который продуцируется адипоцитами
[Панков Ю. А., 1996]. Оказалось, что лептин определенным образом влияет на
запасы жира в организме [Brunner L., Levens N., 1998]. Во всяком случае, у
мышей линии ob/ob с ожирением его содержание в крови снижено по сравнению с
нормальными животными, а при введении лептина мышам этой линии последние
теряют вес. Кстати, свое название лептин получил от греческого слова
"лептос", что означает тонкий или стройный [Панков Ю. А., 1996; Brunner L.,
Levens N., 1998].
Как было установлено далее, лептин влияет на пищевое поведение животных.
При его введении в организм мышам линии ob/ob потребление пищи уменьшается и
именно в силу этого животные теряют вес [Schwartz M.W. et al., 1996; Brunner
L., Levens N., 1998]. Полагают, что регуляторный эффект этого белка
реализуется на уровне пищевых центров гипоталамуса. Это позволяет
рассматривать лептин как специфический гормон, регулирующий запасы энергии в
организме [Casanueva F. F., Dieguez C., 1999].
Естественно, было предпринято изучение содержания лептина и у других
линий животных с большой частотой ожирения. И здесь была обнаружена
ситуация, принципиально отличная от таковой у мышей ob/ob. Оказалось, что у
мышей линии db/db и у крыс линии fa/fa содержание лептина в крови
значительно больше, чем у нормальных животных [Hardie L.J. et al., 1996].
Дополнительное введение этого белка больным животным не влияло на их пищевое
поведение и не приводило к уменьшению массы тела [Schwartz M.W. et al.,
1996]. Тогда было высказано предположение, что ожирение в этом случае
развивается вследствие снижения чувствительности к лептину [Hardie L.J. et
al., 1996].
Белок, аналогичный мышиному лептину обнаруживается и у людей. Однако, до
настоящего времени не установлена его точная роль в развитии ожирения у
человека. Как следует из большого числа исследований, концентрация лептина в
крови больных с избыточной массой тела в 2-7 раз выше, чем в норме. Это
касается как взрослых [Caro J. F. et al., 1996; Segal K. R. et al., 1996;
McGregor G. et al., 1996, Liu J., et al, 1999], так и детей [Hassink S. G.
et al., 1996]. Концентрация лептина у человека прямо и значимо коррелирует
со степенью выраженности ожирения и массой жира. В специальных исследованиях
было показано, что увеличение содержания этого белка в крови у больных с
ожирением связано именно с увеличением его продукции, а не с возможным
замедлением элиминации из крови [Klein S. et al., 1996; Liu J., et al,
1999].
Здесь абсолютно логичной оказалась гипотеза, что больные ожирением в силу
каких-то еще не выясненных причин, утрачивают чувствительность к действию
лептина. Так, в частности J.J. Holst [1996] была предложена липостатическая
гипотеза контроля массы тела, основные положения которой могут быть сведены
к следующему. В норме жировые клетки продуцируют лептин, обладающий
свойствами белкового гормона, основное назначение которого сигнализировать в
специальные центры гипоталамуса о состоянии запасов жира в организме. Данный
сигнал воспринимается с помощью соответствующих рецепторов и реализуется
через систему регуляции аппетита и потребления пищи. Ожирение может
развиться если имеется хотя бы одна из двух мутаций - либо мутация,
нарушающая синтез лептина, либо мутация, нарушающая синтез рецепторов к
нему.
О том, что лептин влияет на нейрохимические процессы в гипоталамусе,
говорят и данные Glaum S.R. et al. [1996]. Причем авторы установили, что
лептин усиливает синаптическую передачу импульсов в аркуатном ядре
гипоталамуса у крыс линии Zuker с нормальной массой тела, но не влияет на
данные процессы у крыс с ожирением. Это, по мнению авторов связано с
мутацией рецептора лептина у последних.
Предпринимались также попытки обнаружить мутации в гипоталамических
рецепторах лептина у людей, больных ожирением. Так, в исследовании Considine
R.V. et al. [1995] сравнивались рецепторы к лептину, выделенные из
гипоталамусов людей, больных ожирением, и людей с нормальной массой тела.
При этом авторам не удалось обнаружить каких либо отличий. В рецепторах,
выделенных от людей с ожирением, не удалось обнаружить и мутаций,
свойственных таковым в рецепторах у мышей линии db/db или крыс линии fa/fa.
В этой связи авторами было высказано предположение, что резистентность к
действию лептина если и имеется, то реализуется она не на уровне
гипоталамического рецептора.
По данным Caro J. F. et al. [1996] хотя концентрация лептина в плазме у
лиц, страдающих ожирением действительно в несколько раз выше, содержание
этого белка в спиномозговой жидкости у них выше всего на 30%. Соотношение
концентраций лептина в спиномозговой жидкости и в плазме у худых людей было
в 4 раза выше, чем таковое у полных пациентов. По мнению авторов, у лиц с
ожирением в результате мутации нарушается продукция переносчика лептина
через гематоэнцефалический барьер и как следствие, снижается
чувствительность к его регуляторному действию.
Головной мозг не единственное место, где обнаруживаются рецепторы к
лептину. Так, сравнительно недавно были обнаружены рецепторы к этому белку и
в (-клетках поджелудочной железы [Kieffer T. J. et al., 1996]. В этой связи
возникло предположение, что лептин каким-то образом влияет на продукцию
инсулина. Исходя из сдерживающего действия лептина на развитие ожирения
(липогенез) полагают, что в норме, в ответ на увеличение концентрации
инсулина увеличивается и продукция лептина, который по принципу
отрицательной обратной связи тормозит дальнейшую продукцию и выброс
инсулина. О том, что инсулин стимулирует продукцию лептина в культурах
адипоцитов продемонстрировано и в исследовании Nolan J.J. et al. [1996].
Причем этот эффект наблюдается только при длительной, но не кратковременной
инкубации культур с повышеной концентрацией инсулина в культуральной среде.
Подводя итог нашего краткого обзора, посвященного лептину, укажем, что
все, что связано с этим белком, как минимум, очень интересно. Однако, все
это еще очень далеко от окончательной ясности. Вроде бы лептин участвует в
поддержании нормальной массы тела и защищает организм от нарастания веса. Но
почему эта защита не срабатывает практически у каждого второго человека?
Возможно в дальнейшем мы будем иметь или препарат лептина или препарат
рецептора к лептину или препарат специфически улучшающий связь лептина с
рецептором или действующий еще как-то, но защищающий организм от развития
ожирения или вызывающий снижение веса [Heymsfield S. B., et al, 1999]. Пока
же мы имеем новую область исследований и говорить о возможном практическом
использовании результатов этих исследований преждевременно.
Механизмы развития заболеваний, причинно связанных с ожирением. Концепция
метаболического синдрома
Не вызывает сомнения, что гипертоническая болезнь, дислипидемия,
атеросклероз и инсулиннезависимый сахарный диабет имеют причинную связь с
ожирением. Или, другими словами, определенные изменения в регуляции
метаболизма и в самом метаболизме, закономерно возникающие при ожирении,
закономерно ведут к развитию этих заболеваний. В этом убеждают нас и
эпидемиологические исследования, показывающие, что у людей с избыточным
весом риск развития перечисленных выше заболеваний значительно превосходит
таковой у лиц с нормальной массой тела. [Bray G. A, 1998; Lean M. E. J.,
1998]. Известно так же, что если эти заболевания уже имеются, то успешное
снижение избыточной массы тела позволяет уменьшить их проявления, улучшить
контроль, или добиться ремиссии [Lean M. E. J., 1998].
Определенным прогрессом в наших представлениях о механизмах, ведущих к
развитию этих заболеваний при ожирении явилась разработка концепции
метаболического синдрома (синдрома инсулинрезистентности или синдрома-Х).
Согласно современным представлениям, к метаболическому синдрому можно
отнести артериальную гипертензию (АГ), дислипидемию, атеросклероз и
ишемическую болезнь сердца (ИБС), а так же инсулиннезависимый сахарный
диабет (ИНСД) [DeFronzo R.A., Ferrannini E, 1991; Mikhail N., et al, 1999,
Kortelainen M. L., Sarkioja T. 1999]. Такое объединение подчеркивает наличие
общих закономерностей в развитии этих заболеваний и открывает для нас новые
возможности в их профилактике и лечении.
Концепция метаболического синдрома постулирует, что в качестве основных
причин и механизмов развития перечисленных выше заболеваний являются такие
метаболические нарушения, как снижение чувствительности тканей к инсулину
(инсулинрезистентность) и компенсаторная гиперпродукция этого гормона
клетками островков Лангенгарса (гиперинсулинизм) [Buzzigoli G., 1987;
Weinsier R.L. et al., 1986; DeFronzo R.A., Ferrannini E., 1991; Aeicao?a М.
М. и Козупица Г. С., 1996].
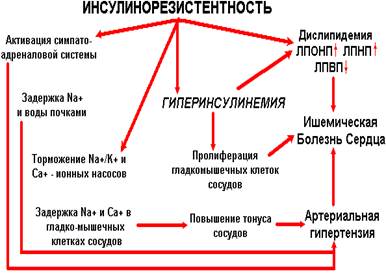
Устанавливаются и механизмы участия гиперинсулинизма и
инсулинрезистентности в патогенезе этих заболеванеий. Известно, что на фоне
гиперинсулинизма усиливается обратное всасывание натрия в канальцах почек. А
увеличение уровня натрия в крови прямо ведет к гиперволемии, увеличению
объема циркулирующей крови и повышению артериального давления. Кроме того,
на фоне гиперинсулинизма повышается активность симпатоадреналовой системы,
что усиливает сосудистый тонус, повышает переферическое сосудистое
сопротивление, что далее, так же ведет к повышению артериального давления
[DeFronzo R.A., Ferrannini E., 1991; Mikhail N., et al, 1999].
На фоне гиперинсулинизма и инсулинрезистентности нарушается метаболизм
липидов в печени. Это приводит к увеличению уровня триглицеридов, а так же
холестерина, связанного с липопротеидами низкой плотности, что в свою
очередь ведет к повышению атерогенности плазмы и прогрессированию
атеросклероза [DeFronzo R.A., Ferrannini E, 1991; Kortelainen M. L.,
Sarkioja T. 1999; Howard B. V., 1999].
Патогенез сахарного диабета второго типа определяется снижением
чувствительности тканей к инсулину, наблюдаемом при ожирении. Для
преодоления инсулинрезистентности клеткам поджелудочной железы приходится
увеличивать продукцию инсулина. Через какое-то время может наступить
истощение резерва их функции и повышение уровня глюкозы в крови [Felber J.
P., 1992; Kopelman P., Formiguera X., 1999].
К инсулинрезистентности и гиперинсулинизму могут привести следующие
причины - избыток жира в организме, избыток жира в пище и малоподвижный
образ жизни (гиподинамия). Впрочем, очень часто эти причины выступают в
сочетании или сочетание гиподинамии и жирного питания ведет сначала к
развитию ожирения, которое в свою очередь приводит к развитию
метаболического синдрома. Мы указываем на возможность самостоятельного
действия данных причин с целью подчеркнуть, что метаболический синдром может
возникать не обязательно на фоне ожирения. Он может возникать и на фоне
нормальной массы тела.
Известно, что избыточный вес и ожирение закономерно сопровождаются
снижением чувствительности тканей к инсулину и гиперинсулинизмом [Bonadonna
R. C. et al., 1990].
О повышении уровня инсулина в крови у пациентов с ожирением говорят и
наши данные (таблица 3).
Таблица 3
Базальный и стимулированный глюкозой уровень иммунореактивного инсулина
(ИРИ) у женщин, больных ожирением [Aeicao?a e a?., 1996]
Показатели
Группы обследуемых
Контроль (n=25)
Ожирение (n=36)
Ожирение 1-2 степени (n=14)
Ожирение
3-4 степени (n=22)
Возраст, годы
28,1+1,1
30,0(1,7
26,8(2,0
32,6(2,5
ИМТ, кг/м2
21,5+0,44
36,6+1,2*
31,6(0,5*
43,6(1,8*+
ИРИ баз., пмоль/л
32,4+4,8
82,4+9,6*
78,0(9,9*
114,2(22,4*
ИРИ стим.- 60 мин, пмоль/л
163,9+19,0
404,3+63,9*
396,7+97,3*
454,7+80,0*
ИРИ стим.-120 мин, пмоль/л
66,0+7,4
255,3+41,8*
225,9+68,4*
299,4+55,9*
Глюкоза баз., пмоль/л
4,32+0,14
4,05+0,11
4,09(0,20
4,14(0,22
* - показатели достоверно отличаются от контроля
+ - показатели достоверно отличаются в группах ожирения
Как видно из приведенных данных, у больных ожирением достоверно выше, чем
у лиц с нормальной массой тела как базальный уровень инсулина, так и уровень
инсулина после стандартной нагрузки глюкозой. Данное увеличение, однако, не
сопровождается значимым снижением базальной концентрации глюкозы. Это может
быть объяснено тем, что у больных с ожирением снижена чувствительность к инсулину. Кстати, как отмечают некоторые авторы, коэффициент отношения
базальных концентраций инсулина и глюкозы может быть принят, как показатель,
количественно характеризующий степень выраженности инсулинрезистентности*
[DeFronzo R.A., Ferrannini E].
Сценарий развития гиперинсулинизма и инсулинрезистентности при ожирении
следующий. По мере увеличения массы жира в организме увеличиваются размеры
жировых клеток. Чем больше адипоцит, тем менее он чувствителен к инсулину.
Соответственно меньше и сдерживаюшее влияние этого гормона на процессы
липолиза. Как результат - повышение уровня триглицеридов и
неэстрифицированных жирных кислот в крови. согласно закономерностям
глюкозожирнокислотного цикла (цикла Рендла), мышечные клетки и клетки
печени, усиливают захват и окисление этих метаболитов и соответственно,
снижают инсулинзависимый транспорт глюкозы - развивается
инсулинрезистентность. Что бы скомпенсировать данные нарушения, а именно
блокировать триглицериды в жировых клетках и предотвратить развитие
гипергликемии, инсулярному аппарату поджелудочной железы приходится
увеличивать продукцию инсулина - развивается гиперинсулинизм.
Как было установлено в недавних исследованиях степень выраженности
гиперинсулинизма и инсулинрезистентности зависит не только от массы
избыточного жира, но и от его распределения [Гинзбург М. М. и соавт., 1996;
Hodge A. M. et al., 1996]. Осложнения более вероятны при так называемом
абдоминальном ожирении, когда основная масса жира расположена в брюшной
полости и на туловище, и менее вероятны при глютеофеморальном, когда жировые
отложения более выражены на ягодицах и бедрах. Причем вероятность развития
осложнений тем выше, чем более выражен абдоминальный характер распределения
жира. Известно, что у лиц с абдоминальным ожирением осложнения появляются в
более молодом возрасте и при меньшем избытке массы тела. Некоторые авторы не
без оснований называют абдоминальное ожирение злокачественным.
Наиболее простыми и надежными критериями, характеризующими распределение
жира являются размер окружности талии и отношение окружностей талии и бедер
(Т/Б[Ѓ.©.9]). У женщин об абдоминальном распределении жира говорят при
величине отношения Т/Б больше 0,81 (по некоторым данным - больше 0,84). У
мужчин абдоминальное распределение жира устанавливается при отношении талия
- бедра больше единицы. Достаточно точно ситуацию с абдоминальным
накоплением жира характеризует и размер окружности талии. При этом
желательно, чтобы окружность талии у мужчины была меньше 94 см, а у женщин
она не превышала 80 см [Hodge AM et al., 1996].
В качестве комментария более злокачественного течения абдоминального
ожирения у женщин приведем собственные данные [Гинзбург М. М. и соавт.
1997], согласно которым при разделение группы больных по признаку
распределения жира у пациентов с абдоминальным ожирением как систолическое,
так и диастолическое АД достоверно повышено по сравнению с контролем, тогда
как при глютеофеморальном ожирении величина АД значимо не отличается от
контроля (таблица 4). Таблица 4
Зависимость уровня артериального давления у больных ожирением от
распределения жира (n - количество больных)
Показатели
Группы обследуемых
Контрольная,
n=33
Больные ожирением,
n=48
Глютеофеморальн. распределение жира, n=17
Абдоминальн. Распределение жира, n=31
Возраст, годы
29,8(1,1
33,3(1,2
32,3(2,0
34,6(1,5
Индекс массы тела, кг/см2
21,5(0,4
35,0(0,7*
33,2(1,0*
35,8(0,8*
Т/Б, усл. ед.
0,70(0,02
0,85(0,01*
0,78(0,01*
0,88(0,01*+
Сист. АД, мм рт. ст.
117,5(2,5
134,7(16,2*
122,5(11,4
141,8(18,3*+
Диаст. АД, мм рт. ст.
75,0(2,9
90,3(12,3*
80,0(8,1
94,8(11,0*+
Глюкоза, ммоль/л
4,32(0,14
4,03(0,09
3,82(0,11
4,12(0,11
Инсулин, пмоль/л
32,4(4,8
83,2(7,4*
57,5(8,8*
101,7(8,8*+
* - различия достоверны по сравнению с контролем
+- различия достоверны между группами больных
У больных с ожирением уровень АД значимо коррелирует с отношением Т/Б
(таблица 5). Эта зависимость носит линейный характер (рис. 6) и описывается
следующимит регрессионными уравнениями:
у1 = 133,4х + 21,7; R2=0,24
y2 = 120,1x - 11,3; R2=0,34
где у1 и у2 - соответственно уровень систолического и диастолического АД,
а х - величина отношения талии и бедер. Таблица 5
Связь АД с характеристиками распределения жира и концентрацией инсулина
Показатели
Коэффициенты корреляции
Систол. АД
Диастол. АД
Т/Б
0,55*
0,58*
Концентрация инсулина
0,59*
0,58*
* значение коэффициента корреляции r достоверно
Механизм более злокачественного течения абдоминального ожирения
определяется тем, что при этой форме распределения жира гиперинсулинизм и
инсулинрезистентность более выражены, чем при глютеофеморальном [Hodge AM et
al., 1996]. Это подтверждается и нашими данными, согласно которым содержание
инсулина в плазме у больных с ожирением достоверно выше при абдоминальном
распределении жира, чем при глютеофеморальном (таблица 4). В то же время
уровень глюкозы крови у больных обеих групп практически не отличается от
контроля. Мы уже отмечали, что более высокий уровень инсулина на фоне
нормального содержания глюкозы позволяет утверждать, что гиперинсулинизм,
наблюдающийся при ожирении, связан с состоянием инсулинрезистентности
тканей.
О связи гиперинсулинизма с распределением жира говорит и обнаруженная
прямая корреляция между концентрацией инсулина и величиной отношения
Т/Б (r=0,51; p<0,05). Нами не выявлено значимой корреляции между индексом
массы тела и уровнем инсулина (r=0,21; p>0,05). Это позволяет заключить, что
у женщин больных ожирением гиперинсулинизм не нарастает линейно с
увеличением индекса массы тела и больше зависит от распределения жира, чем
от степени выраженности ожирения.
Кстати, имеются интересные данные, показывающие, что артериальная
гипертензия у лиц со статистически нормальной массой тела более вероятна при
преимущественно абдоминальном накоплении жира [DeFronzo R.A., Ferrannini E.
1991].
Необходимо учитывать, что возникновение или не возникновение какого либо
заболевания, связанного с метаболическим синдромом зависит от многих
факторов и в частности от систем, регулирующих жировой и углеводный обмен.
Нарушение этой регуляции может возникать и при слишком большой массе жира и
при слишком выраженном абдоминальном его распределении.
Имеется также отчетливая зависимость развития метаболического синдрома от
возраста. Известно, что с возрастом как у мужчин, так и у женщин усиливается
абдоминальное накопление жира, а так же ухудшается чувствительность тканей к
инсулину [Kotani K., et. al. 1994]. В этой связи нет ничего удивительного,
что в некоторых случаях проявления метаболического синдрома могут
наблюдаться и при нормальном весе, но при преимущественном абдоминальном
накоплении жира. Более того, осознавая эту связь, в плане этиотропного
лечения, мы можем предложить пациенту немного уменьшить массу тела (даже
учитывая, что она не превышает статистическую норму) и настоять на этом пути
лечения.
Как полагают, более высокий уровень инсулинрезистентности при
абдоминальном ожирении объясняется тем, что интраабдоминальная клетчатка по
природе своей более чувствительна к липолитическому действию катехоламинов
и, наоборот, менее чувствительна к антилиполитическому действию инсулина
[DeFronzo R.A., Ferrannini E. 1991; Albu J. B. et al, 1999]. То есть, при
абдоминальном ожирении уровень триглицеридов и неэстрифицированных жирных
кислот в крови обычно значимо выше, чем при глютеофеморальном той же степени
выраженности [DeFronzo R.A., Ferrannini E. 1991; Albu J. B. et al, 1999].
Как мы уже отмечали выше, повышение уровня триглицеридов и
неэстрифицированных жирных кислот в крови можно признать пусковым в развитии
метаболического синдрома. Далее события развиваются по уже описанному нами
сценарию. В соответствии с закономерностями глюкозо-жирнокислотного цикла
клетки тканей мишеней (мышечные и печеночные) уменьшают инсулинзависимый
транспорт глюкозы - развивается инсулинрезистентность, которая
компенсируется увеличением продукции инсулина и гиперинсулинизмом.
Не следует думать, что глютеофеморальное ожирение, в отличие от
абдоминального, никогда не сопровождается осложнениями. В плане развития
инсулинрезистентности опасен любой избыток жира, просто при преимущественно
абдоминальном его накоплении осложнения развиваются при меньшей степени
выраженности ожирения и в более молодом возрасте.
Наличие или отсутствие осложнений при ожирении зависит и от состояния
компенсаторных механизмов. Например, сахарный диабет клинически не проявит
себя пока островковый аппарат в состоянии продуцировать инсулин в
количествах, уравновешивающих инсулинрезистентность. Уровень артериального
давления даже при наличии всех предпосылок к его повышению может
поддерживаться в норме благодаря хорошей функциональной активности
депрессорной системы. Атеросклероз может длительное время не проявлять себя
при хорошей способности к росту коллатералей. Причем у разных больных
резервы компенсации тех или иных проявлений ожирения могут быть выражены по
разному. И, возможно, поэтому у одних больных осложнения ожирения могут быть
представлены нарушением толерантности к углеводам, у других - артериальной гипертензией, у третьих - ишемической болезнью сердца, или ИНСД, у четвертых
- сочетанием перечисленных выше заболеваний, а пятые, имея и достаточно
выраженный избыток массы тела и абдоминальное накопление жира и преклонный
возраст могут оставаться относительно здоровыми.
В общем понятен и механизм развития гиперинсулинизма и
инсулинрезистентности при питании с большим количеством жира. Избыток жира в
пище может прямо вести к его избытку в крови и, опять же, по закономерностям
глюкозожирнокислотного цикла может переключать метаболизм основных
тканей-мишеней на преимущественное потребление и окисление жирных кислот
[Lichtenstein A. H., et al 1998]. В этом случае тормозится инсулинзависимый
транспорт глюкозы, возникает инсулинрезистентность, для компенсации которой
развивается гиперинсулинизм.
При гиподинамии механизмы развития метаболического синдрома заключаются в
следующем. На фоне малоподвижности существенно снижается захват мышцами
жирных кеислот а так же инсулинзависимый транспорт глюкозы -
инсулинрезистентность, которая далее компенсируется гиперинсулинизмом [Weyer
C., et al, 1999].
Итак, гипертоническая болезнь, атеросклероз и сахарный диабет второго
типа в настоящее время рассматриваются как естественные и закономерные
осложнения ожирения. Установлено, что в основе их патогенеза лежит явление
снижения чувствительности тканей к инсулину (инсулинрезистентность) и
компенсирующая это состояние гиперпродукция инсулина клетками поджелудочной
железы (гиперинсулинизм) [Гинзбург М. М., Козупица Г. С. 1997].
Инсулинрезистентность и гиперинсулинизм обычно наблюдаются при ожирении и
патогенетически связаны со степенью выраженности избытка массы тела
[Bonadonna R. C. et al., 1990].
Наличие осложнений более тесно связано с абдоминальным накоплением жира,
чем со степенью выраженности избытка массы тела. Объясняется это особенной
ролью абдоминального жира в обмене веществ, изначально меньшей его
чувствительностью к инсулину и как следствие более выраженной
инсулинрезистентностью, наблюдаемой при абдоминальном ожирении.
Разработка концепции метаболического синдрома весьма перспективна для
современной медицины. Появилась возможность большую группу болезней,
существенно влияющих на структуру заболеваемости, смертности и
продолжительность жизни, причинно связать с нарушением жирового обмена и
ожирением. Эта концепция определяет и патогенетически обосновывает меры
профилактики и лечения заболеваний, объединяющихся в метаболический синдром.
Их профилактика и лечение в обязательном порядке должна включать меры,
направленные на повышение чувствительности тканей к инсулину, а именно,
нормализацию питания с уменьшением доли жира в пище, более активные
двигательные режимы и комплекс воздействий, направленных на снижение
избыточной массы тела. Действительно, в большом количестве исследований
установлено, что снижение массы тела ведет к снижению артериального давления
у гипертоников, к уменьшению показателя атерогенности плазмы и к уменьшению
частоты приступов стенокардии у больных с ИБС, а так же к улучшению контроля
уровня гликемии у больных с ИНСД [Гинзбург М. М., Козупица Г. С. 1997].
Необходимо учитывать, что гиперинсулинизм и инсулинрезистентность могут
развиваться и у лиц, имеющих нормальный вес. Обычно это происходит на фоне
гиподинамии, или при чрезмерном потреблении жиров, особенно животных, при
абдоминальном распределении жира, а так же в преклонном возрасте. При этом
так же может наблюдаться весь спектр осложнений, характерных для ожирения.
Некоторые исследователи определяют метаболизм, наблюдаемый у таких больных,
как метаболизм, подобный таковому при ожирении (like obesity metabolism).
Вместе с тем, очень большой круг вопросов оста„тся до конца не
выясненными. В частности не определено, следует ли относить к
метаболическому синдрому все случаи ожирения, можно ли всякий случай
эсенциальной артериальной гипертензии или ишемической болезни сердца
рассматривать как проявлекния метаболического синдрома, при каких
концентрациях инсулина и показателях инсулинрезистентности можно говорить о
наличии метаболического синдрома и можно ли говорить об этом синдроме, если
у пациента не выявляется ни одно из его клинических проявлений, но имеется
гиперинсулинизм?
Наверное, многие вопросы разрешатся, когда будет уточнена концепция
синдрома и разработана его классификация. Например, определив пороговые
концентрации инсулина, можно было бы выделить скрытые формы метаболического
синдрома, когда гиперинсулинизм является единственным его проявлением. В
этих случаях наши усилия были бы направлены на профилактику развития его клинических проявлений. Если же окажется, что метаболический синдром
является основной причиной развития эсенциальной гипертонии или
дислипидемии, то будет существенно повышена роль диет и физических
упражнений в лечении этих заболеваний. Согласимся, что сейчас врачи уделяют
мало внимания этим, действительно этиотропным методам лечения.
Поскольку пусковым в развитии метаболического синдрома является повышение
базального уровня триглицеридов и ненасыщенных жирных кислот в крови, можно
было бы придать этим показателям диагностическое значение, аналогичное,
например, значению гипергликемии натощак при сахарном диабете.
Классификация ожирения
К ожирению следует относить ситуации, когда избыток жировой массы на 15%
превышает идеальный вес* или на 10% - максимально допустимый вес** тела.
Меньший избыток веса определяется как избыточная масса тела и
рассматривается как предболезнь [Шурыгин Д. Я. и соавторы, 1980].
В Западной литературе избыток веса чаще оценивают по индексу массы тела
или по индексу Кеттле. Он определяется путем деления массы тела в
килограммах на величину роста в метрах, возведенную в квадрат. Индекс Кеттле
достаточно надежно характеризует избыток массы тела у взрослых мужчин и
женщин, имеющих рост в пределах средних значений (150-185 см). При
нормальной массе тела индекс Кеттле меньше 25,0. Если он больше 25, но
меньше 27 - это избыточная масса тела, но еще не ожирение, если больше 27 -
это ожирение. Причем, если индекс Кетле меньше 28,5, говорят о легком
ожирении, если меньше 35, то это ожирение средней степени тяжести, если
индекс Кеттле меньше 40, это тяжелое ожирение, наконец, если он больше 40 -
это ожирение очень тяжелое.
Этиопатогенетическая классификация ожирения подразделяет ожирение на
первичные и вторичные формы. Вторичное или симптоматическое ожирение
включает в себя эндокрино-метаболическое ожирение, рассмотренное выше
(ожирение при синдроме Кушинга, при гипотиреозе, при акромегалии и при
инсуломе), и церебральное ожирение, связанное с заболеваниями и поражением
головного мозга. Отличительным свойством вторичных форм ожирения является
уменьшение массы тела при успешном лечении основного заболевания [Шурыгин Д.
Я. и соавторы, 1980].
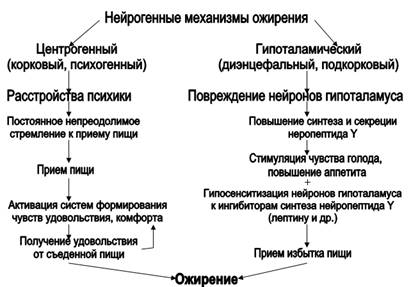
Первичное ожирение, на долю которого приходится 90-95% всех случаев
заболевания, в свою очередь подразделяется на алиментарно-конституциональную
и нейроэндокринную (гипоталамическую) формы.
Необходимо отметить, что абсолютно надежных и четких критериев
дифференциированного диагноза этих форм не существует. В руководствах,
посвященных этому вопросу, указывается, что алиментарно-конституциональное
ожирение - доброкачественная медленно-прогрессирующая форма, довольно редко
приводящая к развитию осложнений. Отложение жира обычно пропорциональное и
соответствующее полу. Нейро-эндокринное - наоборот, быстро прогрессирует,
часто имеет осложнения (гипертензия, дислипидемия, сахарный диабет), могут
наблюдаться симптомы гипоталамической дисфункции - головные боли, нарушения
сна, расстройства вигетатики и др., отложение жира непропорциональное
(выражено абдоминальное по типу синдрома Кушинга или глютеофеморальное по
типу синдрома Барракера-Сименса).
Отметим, в медицине Запада разделение ожирения на алиментарное и
гипоталамическое отсутствует. Что касается отечественной медицины, то далеко
не все авторы поддерживают подобное подразделение [Терещенко И. В., 1991].
Действительно, при любом ожирении могут наблюдаться периоды быстрого набора
массы, которые сменяются длительными периодами стабилизации. Наличие или
отсутствие осложнений скорее определяются степенью ожирения, формой
распределения жира, возрастом и продолжительностью заболевания. Форма
распределения жира (абдоминальная или глютеофеморальная), как было
установлено в недавних исследованиях, определяется генетическими и
эндокринными механизмами [Гинзбург М. М., Козупица Г. С. 1996], но никак не
гипоталамической дисфункцией. Да и сама гипоталамическая дисфункция
(гипоталамический синдром) может развиваться уже вторично на фоне
существующего ожирения. Другими словами, при анализе конкретных случаев
заболевания, бывает довольно трудно выделить несомненно нейроэндокринные
формы, развитие которых связано с первичной гипоталамической дисфункцией.
В последние годы наметилась тенденция подразделять ожирение по признаку
распределения жира на абдоминальное, когда основная масса жира расположена в брюшной полости, на передней брюшной стенке, туловище, шее и лице (мужской
или андроидальный тип ожирения) и глютеофеморальное с преимущественным
отложением жира на ягодицах и бедрах (женский или гиноидальный тип ожирения)
[Гинзбург М. М., Козупица Г. С. 1996]. Обусловлено это тем, что при
абдоминальном ожирении значительно чаще чем при глютеофеморальном
наблюдаются осложнения. Установлено, что осложнения при абдоминальном
ожирении наблюдаются в более молодом возрасте и при сравнительно меньшем
избытке массы тела. Как мы уже указывали, наиболее простой и достаточно
надежный критерий подразделения ожирения по признаку распределения жира -
это отношение размеров талии и бедер. При преимущественном
глютнеофеморальном распределении жира у женщин это отношение меньше 0,81,
соответственно, при абдоминальном - больше 0,81. У мужчин граница
подразделения на абдоминальное и глютеофеморальное ожирение составляет 1,0.
В зависимости от того, нарастает в данный момент масса тела, остается
стабильным или снижается, оправдано подразделение ожирения на
прогрессирующее, стабильное или регрессирующее. Однако, до настоящего
времени нет точных критериев, сколько килограммов и за какой период следует
набрать или потерять, что бы данное ожирение было отнесено к
прогрессирующему или регрессирующему. Мы полагаем, что колебания массы тела
порядка 2-3 кг в год можно отнести к стабильному ожирению, а вот если масса
тела увеличивается на 5 кг в год и более, то такой случай есть все основания
отнести к прогрессирующему ожирению.
В зависимости от наличия или отсутствия осложнений ожирение может быть
подразделено на осложненное или не осложненное. Напомним, что в качестве
типичных и наиболее частых осложнений ожирения можно рассматривать
гипертоническую болезнь, атеросклероз и ишемическую болезнь сердца а так же
инсулиннезависимый сахарный диабет.
Принципы профилактики ожирения
С учетом закономерностей нарастания избыточного веса можно выделить
следующие группы лиц вероятность развития ожирения у которых значимо
превосходит среднюю:
* лица, у которых хотя бы один из родителей имеет избыточный вес;
* женщины в период беременности и в течение 2-3 лет после родов;
* спортсмены, прекратившие тренировки, лица, уволенные в запас из армии,
лица, по каким либо причинам, сократившие объем физических нагрузок;
* больные, перенесшие тяжелые операции или травмы и вынужденные
длительное время проводить на постельном или ограниченном двигательном
режиме;
* люди, отказавшиеся от курения;
* люди, вынужденные длительное время принимать препараты раувольфии или
(-блокаторы;
* лица с привычно большим потреблением жира;
* лица среднего и пожилого возраста;
Как видим, в группу риска по заболеванию ожирением можно без особых
усилий включить большинство из взрослых людей. Поэтому еще раз отметим, что
профилактика ожирения очень важна и должна быть направлена на все общество.
К сожалению, до настоящего времени ни одно из государств, не смотря на
высокую социальную значимость проблемы ожирения и внушительные суммы
экономических потерь, связанных с этой проблемой не может похвалиться
наличием серьезной общегосударственной программы профилактики ожирения. Чаще всего дело ограничивается врачебной профилактической работой, а та, в свою
очередь, ограничивается пожеланиями вести более активный образ жизни и более
рационально питаться. Иногда советы подобного рода доходят до нас и из
средств массовой информации. Причем, как и в лечение ожирения, наряду с
советами более или менее серьезными есть и советы, научная обоснованность
которых весьма сомнительна. Более того, периодически в средствах массовой
информации в том или ином виде встречаются и пожелания прямо
противоположные. А именно, что избыточный вес лечить не следует, что полный
человек по своему красив и по своему здоров, что организм сам знает сколько
ему есть и сколько ему весить, и так далее. Не трудно себе представить как
полные люди, зачастую уже измученные многочисленными безуспешными попытками
похудеть, воспринимают подобного рода советы.
Не лишне напомнить, что профилактика ожирения, как и профилактика любого
другого заболевания, должна строиться на точном знании причин и механизмов
его развития. В этой связи идеи, рекомендующие в качестве основ профилактики
интенсивные физические нагрузки, низкую калорийность питание и чрезвычайно
жесткое ограничение углеводов, следует признать устаревшими. Во-первых,
соблюдать их могут лишь единицы, а во-вторых, благодаря научным достижениям
последнего времени могут быть предложены иные пути профилактики, как более
приемлемые в плане длительной и массовой воспроизводимости, так и более Речь идет об открытом недавно явлении, суть которого заключается в
следующем. При низкой доле жира в питании масса тела остается стабильной
даже если потребление других нутриентов и прежде всего, углеводов не
лимитируется [Katan M. B. 1998]. Такой режим питания с полным на то
основанием можно было бы определить как нежирогенный. В профилактической
работе необходимо стремиться ограничить потребление жира на столько, на
сколько это возможно при сохранении удовлетворительного качества жизни. Для
того чтобы уменьшить потребление жира человек должен хотя бы примерно
представлять его количество в тех или иных продуктах. Можно было бы
предложить людям небольшие таблицы по его содержанию в наиболее популярных
продуктах.
Что касается двигательного режима, то и здесь обнаруживается, что
вероятность развития ожирения обратно пропорциональна физическим нагрузкам,
совершаемым человеком. Врач в своей работе должен стремиться поддержать у
человека ценность физических нагрузок, вызвать желание их исполнять. Однако
и здесь предстоит еще очень большая работа, что бы определить принципы
дозирования нагрузок и определения оптимальных режимов тренировок и
двигательных режимов для предупреждения развития ожирения в тех или иных
возрастных группах.
Несмотря на то, что в здравоохранении России данная диета в настоящее
время применяется как основная в лечении ожирения, в доступной литературе мы
не смогли найти сведений, характеризующих ее эффективность. Ориентируясь на
собственные данные по применению диеты у больных ожирением, укажем, что
она эффективна лишь у 70% пациентов и у 70% из них лишь в течение первого
месяца лечения. Средний результат снижения веса за первый месяц лечения
составляет 2,3-3,5 кг. Далее в большинстве случаев несмотря на продолжение
диеты снижение веса прекращается или пациенты прекращают лечение не выдержав
жестких условий монотонной диеты. Диета не приводит к формированию
навыков рационального питания, поэтому после прекращения лечения
рецидивирование избыточного веса наблюдается с частотой 90-95%.
Уменьшение гиперинсулинизма и инсулинрезистентности в ходе диетотерапии
может быть обусловлено питанием с низким содержанием жиров в пище,
уменьшением у пациенток как общей жировой массы, так и массы абдоминального
жира, о чем свидетельствует уменьшение размеров талии Заметим, что если при снижении жировой массы можно ожидать улучшения
контроля таких грозных заболеваний, как артериальная гипертензия, сахарный
диабет, атеросклероз и ишемическая болезнь сердца, то лечение ожирения
несомненно можно рассматривать в качестве эффективного метода лечения этих
заболеваний. А поскольку ожирение, согласно современным представлениям, есть
причина названных заболеваний, то такое лечение можно с полным основанием
называть этиотропным.
Основные принципы лечения ожирения при наличии у больного артериальной
гипертензии, ишемической болезни сердца или сахарного диабета могут
оставаться такими же как и при неосложненном ожирении. Однако, наличие
осложнений заставляет врача несколько изменить тактику лечения. Естественно,
что при этом следует избегать назначений, ухудшающих контроль того или иного
осложнения. Врач должен настаивать на более медленном и мягком снижении
веса, памятуя, что резкие диетические ограничения могут повлечь за собой
стресс и, как следствие, обострение течения того или иного осложнения.
Следует с большей осторожностью подходить и к назначению индивидуальных
двигательных режимов. Лечебное действие физических тренировок при
дислипидемиях, артериальной гипертензии и ИНСД хорошо известно. Однако
применение чрезмерных нагрузок может обострить течение этих заболеваний.
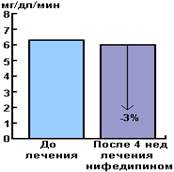
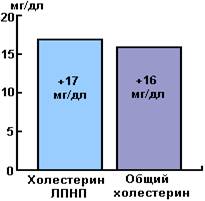
При сопутствующей артериальной гипертензии следует уделить определенное
внимание назначению гипотензивной фармакотерапии. Известно, что (-блокаторы
и тиазидовые диуретики, усиливая инсулинрезистентность, тем самым замыкают
порочный круг, приводящий как к развитию самого ожирения так и к повышению
артериального давления [Крутикова Е. В., Преображенский Д. В., 1995].
Отношение к этим средствам должно быть пересмотрено. Предпочтение следует
отдавать препаратам, появившимся сравнительно недавно - ингибиторам
ангиотензинпревращающего фермента и антагонистам ангиотензина. У таких
больных следует с определенной осторожностью назначать биостимуляторы и
другие средства, способные повышать или потенцировать артериальное давление.
Эта рекомендация относится и к больным, у которых ожирение осложнено
ишемической болезнью сердца.
Следует еще раз подчеркнуть, что вопрос о назначении гипотензивных
средств должен возникать только в том случае, если применение диетических
мероприятий (маложирное, разгрузочное питание с ограничением поваренной
соли) не позволяет достичь контроля артериальной гипертензии. Врач должен
настаивать на уменьшении избытка жировой массы. Он должен быть готов к
уменьшению дозы и даже к полной отмене лекарственных средств в процессе
уменьшения избыточного веса, поскольку это тоже может сопровождаться
улучшением контроля артериальной гипертензии.
При сопутствующем сахарном диабете, особенно при среднетяжелой и тяжелой
формах, когда компенсация достигается соответственно назначением сахароснижающих препаратов или инсулина, следует корректировать дозу этих
средств, так как гипокалорийная диета, резко уменьшая потребность тканей в
инсулине может способствовать развитию гипогликемических состояний. Мы
рекомендовали бы начинать лечение таких больных в условиях терапевтического
или эндокринологического отделения, где можно обеспечить контроль уровня
глюкозы в крови. После отработки дозы сахароснижающих средств и/или инсулина
на фоне гипокалорийной диеты лечение может быть продолжено в амбулаторных
условиях. У таких пациентов следует воздержаться и от применения жестких
диетических режимов с выраженным дефицитом калорий. Нам представляется, что
методом выбора у них могла бы стать изокалорийная диета - диета с
односторонним уменьшением жира до 35-45 граммов в день и менее. Нужно быть
осторожным и в рекомендации двигательных режимов у больных сахарным
диабетом. Известно, что на фоне интенсивных тренировок уровень сахара крови
может понижаться, что в условиях применения инсулина или сахароснижающих
средств резко повышает риск развития гипогликемических состояний.
В последние годы вновь повысился интерес к сахароснижающему препарату
бигуанидной природы метформину. Как было показано в ряде исследований, этот
препарат специфически повышает чувствительность тканей к инсулину,
способствует уменьшению гиперинсулинизма. Метформин не вызывает повышения
массы тела у больных [Zimmet P., Collier G., 1999; Pugeat M., Ducluzeau P.
H. 1999; Yki-Jarvinen H., et al., 1999]. В настоящее время основным
показанием к применению метформина является сахарный диабет у пациентова с
ожирением. Вместе с тем, имеются отдельные сообщения о применении этого
препарата в плане коррекции метаболических сдвигов (гиперинсулинизма и
инсулинрезистентности) у пациентов с сохраненной толерантностью к углеводам
[Pugeat M., Ducluzeau P. H. 1999]
При лечении ожирения, осложненного ишемической болезнью сердца весьма
желательно включать в комплекс препаратов полиненасыщеннве жирные кислоты
из-за их выраженного противосклеротического действия. Здесь так же уместны
замечания, высказанные нами в связи с артериальной гипертензией или сахарным
диабетом. Не желательны чрезмерные диетические ограничения и чрезмерные
физические нагрузки. Нам представляется не совсем уместным и применение у
таких пациентов (-блокаторов.
Психотерапия
В соответствии с современными представлениями об этиологии и патогенезе
ожирения, психотерапия, конечно же, не является ведущим методом лечения
этого заболевания, однако с помощью психотерапевтических методов лечения у
пациента может быть выработан новый стереотип питания и новый стереотип
образа жизни, выработано конструктивное отношение к своей проблеме, усилена
ценность задачи снижения массы тела, что, несомненно, в дальнейшем усилит и
закрепит эффект лечения.
Мы полагаем, что любой врач, занимающийся лечением ожирения, применяет те
или иные методы психотерапии, зачастую даже не подозревая об этом.
Действительно, пациента необходимо убедить, что дальше все будет хорошо, что
все те трудности, с которыми он встретится в ходе лечения, он сможет
преодолеть и что в конце лечения его ждет приз - хорошая внешность и хорошее
здоровье. И от того, на сколько врачу удастся проконтролировать мысли и
чувства своего пациента, во многом зависит эффект лечения. Здесь же нам
хотелось бы рассмотреть именно методы и возможности профессиональной
психотерапии, а так же роль и место практикующих психотерапевтов в лечении
больных с ожирением.
Наиболее часто врачами используется так называемая рациональная
психотерапии в виде терапии поведением. Пациента обучают навыкам безопасного
обхождения с пищей, учат умерять свои пищевые пристрастия и есть в конечном
счете ровно столько, сколько необходимо чтобы не потолстеть. Обычно такие
методы позволяют закрепить полученный результат, увеличить срок ремиссии и уменьшить количество рецидивов ожирения. В работе D. B. Allison и M. S.
Faith [1996] авторы сочетали терапию поведением с гипнозом, направленным на
более глубокое усвоение навыков образа питания и образа жизни. При анализе
результатов оказалось, что гипноз сам по себе не усиливает эффекта диеты и
бихивиористической терапии.
В некоторых лечебных центрах Запада наряду с индивидуальной работой (врач
- пациент) практикуется метод лечебного коллектива, в котором пациенты
обмениваются опытом решения трудностей, возникающих при соблюдении диеты и
режима физических нагрузок, сообща находят выходы из тех или иных жизненных
ситуаций, препятствующих снижению массы тела. В этом плане демонстративны
результаты исследования J. Balle и T. P. Almdal [1996] где авторы в группе
больных преподавали только принципы рационального питания и образа жизни, не
усиливая их назначением гипокалорийной диеты. Через 4 месяца наблюдения
отмечалось уменьшение массы тела в среднем на 5,2 кг, что, кстати, было
несколько больше, чем при индивидуальной работе с пациентами.
В России применение психотерапии в лечении ожирения только-только
начинает развиваться. Следует отметить, что "кодирование", столь популярное
в последнее время, имеет очень мало общего с серьезной психотерапией.
Опыт оперативного лечения ожирения
Традиционно ожирение относилось к заболеваниям терапевтическим
(эндокринологическим), а основной метод лечения был консервативный - диета,
лечебная физкультура, психотерапия, и так далее. Однако, видимо из-за
удручающих результатов такого лечения, на протяжение последних 25 - 30 лет
более или менее пристально изучалась и возможность хирургического лечения
ожирения [Husemann B., 1995] Отметим, что интерес к хирургическим методам
лечения, судя по публикациям в зарубежной литературе, значительно усилился.
Появились исследования катамнестического характера, охватывающие довольно
длительный срок наблюдения и большое число больных. К сожалению, мы не
смогли найти отечественных публикаций, посвященных оперативному лечению
ожирения. С учетом этого мы посчитали целесообразным предложить читателю
небольшой обзор проблемы [Desaive C., 1995]
В основном оперативное лечение проводится у пациентов с выраженным
ожирением (ИМТ не менее 40 кг/м2), имеющих, как правило, те или иные
метаболические осложнения.
Основные методы операции - еюноколоностомия, операция на выключение
желудка и вертикальная бандажная гастропластика (ВБГ). Последняя
осуществляется с помощью кольца из инертных полимерных материалов, диаметром
45-50 мм, фиксирующемся на теле желудка. Укажем, что в последние годы
наиболее часто используется именно ВБГ.
В работе Frering V., et al. [1996] исследовались отдаленные результаты
ВБГ, выполненной в период с 1987 по 1993 год у 62 больных, 7 мужчин и 55
женщин в возрасте от 20 до 68 лет. Перед операцией средний вес пациентов
составлял 123+27 кг, ИМТ - 47,3+9,8 кг/м2. Среди метаболических осложнений у
больных отмечались сахарный диабет в 31 случае, артериальная гипертензия в
Похожие работы
... клиники и установления диагноза СД 2 типа. Ряд исследований свидетельствует о развитии МС вследствие длительного течения АГ, которая приводит к снижению периферического кровотока и развитию ИР. Артериальная гипертензия и метаболический синдром АГ часто является одним из первых клинических проявлений МС. В основе патогенеза АГ при МС лежит ИР и вызванная ею компенсаторная ГИ в сочетании с ...
... диабета 2-го типы составляет в Европе 40-60 миллионов человек. В индустриальных странах распространённость МС среди населения старше 30 лет составляет 10-20 %, в США — 25 %. Ранее считалось, что метаболический синдром – это удел людей среднего возраста и, преимущественно, женщин, обычно его частота возрастает в менопаузальном периоде. Однако проведённые под эгидой Американской Ассоциации Диабета ...
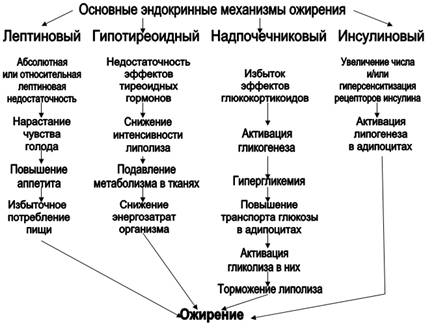
... , скорость обменных процессов в тканях и энергетические затраты организма. В результате нарастает масса тела. [1] 3.2.3 Надпочечниковый механизм Надпочечниковый (глюкокортикоидный, кортизоловый) механизм ожирения включается вследствие гиперпродукции глюкокортикоидов в коре надпочечников (например, при болезни или синдроме Иценко-Кушинга). Под влиянием избытка глюкокортикоидов активизируется ...
... основе выявлялся отек, значительное полнокровие сосудов, т.е. преобладают микроциркуляторные нарушения. Выводы Таким образом, наличие МС: – является основой полиморбидности в гастроэнтерологии; – характеризуется системными однотипными изменениями органов пищеварения, обусловленными преимущественно микроциркуляторными нарушениями; – характеризуется отсутствием четкой клинической симптоматики, а ...


0 комментариев