Навигация
Гордон А., Форд Р.. “Спутник химика”. М.: Мир, 1976
39 Гордон А., Форд Р.. “Спутник химика”. М.: Мир, 1976.
40Мартин В. В., Володарский Л. Б., Щукин Г. И., Вишневецкая Л. А., Григорьев И. А. // Известия АН СССР, Сер. хим. 1985. С. 161 -169.
41Репинская И. Б., Шварцберг М. С.. Избранные методы синтеза органических соединений. Новосибирск.: Из-во НГУ. 2000. С. 243.
42Brown R. F. S., Clark V. M., Lamchen M., Todd A. // J. Chem. Soc. 1959. № 6. Р. 2116 - 2122.
43Voinov M. A., Grigor'ev I. A., Volodarsky L. B. // Heterocyclic Communications 1998. Vol. 4. № 3. P. 261.
44Кошин А. Н., Хуторянский В. А., Могорская О. И., Белецкая И П., Реутов О.А. // ЖОРХ. 1978. Том 14, №1, 231 - 233.
45Milstein D., J.K. Stille. // J. Am. Chem. Soc. 1979. Vol. 101. № 17. P. 4992 - 4998.
46Stille J.K. // Angew. Chem., Int.Ed. 1986. № 25. P. 508-524.
47Godschalk J., J.K. Stille // Tetrahedron Lett. 1980. Vol. 21. № 27. P. 2599 - 2602.
48Stanforth S.P. // Tetrahedron 1998. Vol. 54. № 3 – 4. P. 263-304.
49Kikukawa K., Kono K., Wada F., Matsuda T. // J. Org. Chem. 1983. Vol. 48. №8. 1333 - 1336.
50Кашин А.Н., Бумагина И. Г., Бумагин Н .А., Белецкая И. П. // ЖорХ. 1981. Том 17, №1. С. 21.
51Farina V., Krishnan B., Marshall D. R., Roth G. P. // J. Org. Chem. 1993. Vol. 58. P. 5434 - 5444.
52Bailey T.R. // Tetrahedron Lett. 1986. Vol. 27. № 37. Р. 4407 - 4410.
53Yamamoto Y., Seko T., Nemoto H. // J. Org. Chem. 1989 Vol. 54. № 20. Р. 4734 – 4736.
54Roth G. P., Farina V., Liebeskind L. S., Pena-Carbera E. // Tetrahedron Lett. 1995. Vol 36. № 13. Р. 2191 - 2195.
55Rochin A. I., Bumagin N. A., Beletskaya I. P. // Tetrahedron Lett. 1995. Vol. 36. № 1. Р. 125 – 129.
56Сколдинов А.П., Кочешков К.А. // ЖОХ. 1942. Том 12. Вып. 7- 8. С. 398.
57Logue M.W., Teng K. // J. Org. Chem. 1982. Vol. 47. № 13. P. 2549 – 2533.
58Yamamoto Y., Yanagi A. // Chem. Parm. Bull. 1982 Vol. 30. P. 2003
59Labadie J.W., Stille J.K., Tuefing D. // J. Org. Chem. 1983. Vol. 48. № 24. P. 4634 - 4642
60Reutov O. A. // Pure Appl. Chem. 1968. Vol. 17. P. 79.
61Белецкая И. П., Карпов В. И., Москаленко В. А., Реутов О. А. // Докл. АН СССР 1965. Том 162. с. 414.
62Julia M., Colomer E. // Compt. Rend. Acad. Sci. 1970. C 270. P. 1305.
63Hoye T. R., Kurth M. J. // J. Org. Chem. 1979. V. 44. P. 3461.
64Larock R.C. // Tetrahedron 1982. Vol. 38. № 12. P. 1713 - 1754.
65Белецкая И. П., Максименко О. А., Реутов О. А. // ЖOpХ. 1996. № 2. С. 1124.
66Takagi К., Okamoto Т., Sakakibara Y., Ohno A., Oka S., Hayama N. // Chem. Lett. 1969. p.911.
67Bundel Yu. G., Rozenberg V. I., Kurts A. L., Antonova N. D., Reutov O. A. // J. Orgnometal. Chem. 1969. Vol. 18. p. 209.
68Warshaw J. A., Gallis D. E., Acken B. J., Gonzales O. J., Crist D. R. // J. Org. Chem. 1989. Vol. 54. № 7. P. 1736 - 1743.
69Lub J., de Boer Th. J. // Rec. trav. chim. 1984. B. 103. S. 328.
70Janzen E. G., Zhang Y.-K. // J. Org. Chem. 1995. Vol. 60. № 17. P. 5441 - 5445.
71Щукин Г. И., Григорьев И. А., Вишневецкая Л. А.,Володарский Л. Б. // Изв. АН СССР. Сер. хим. 1988. Том 8. № 1. С. 1944.
72Coates R. M., Firsan S. J.// J. Org. Chem. 1998. Vol. 51. Р. 5198 - 5209.
73Григорьев И. А, Щукин Г. И., Мартин В. В.,. Маматюк В. И. // ХГС. 1985. Том 2. С. 252 - 259.
74Мажукин Д. Г., Тихонов А. Я, Петренко О. П., Володарский Л. Б. // ХГС. 1997. № 3. с. 403 - 405.
75Хмельницкий Л. И., Новиков С. С., Годовикова Т. И. // Химия фуроксанов. Строение и синтез. М.: Наука, 1981.
76Kцbrich G. // Chem. Ber. 1959. B. 92. № 11. S. 2981 - 2985.
77Rheingold A. L., Lable-Sands L. M., Trofimenko S. // Angew. Chem., Int. Ed. 2000. Vol. 39. № 18. Р. 3321 - 3324.
78Щукин Г. И., Григорьев И. А., Володарский Л. Б. // ХГС. 1990, № 4, С. 478 - 482.
79Kalinowski H.-O., Berger S., Braun, S. In book. Carbon-13 NMR Spectroscopy. Brisbane, Toronto, Singapore, N.Y.: John Wiley & Sons 1988. Chapter 3, P. 250.
80 Reich H.J., Sikorski W.H., Gudmundsson B.O., Dykstra B.O., Triplr R.R. // // J. Am. Chem. Soc. 1998. Vol. 120. Р. 4035 - 4036.
81 Voinov M. A., Salnikov G. E., Genaev A. M., Mamatyuk V. I., Shakirov M. M., Grigor’ev I. A.// Magn. Reson. Chem. 2001 Vol. 39. P. 681 – 683.
82Митасов М. М., Григорьев И. А., Щукин Г. И., Коробейничева И. К., Володарский Л. Б. // Изв. СО АН СССР. Сер. хим. 1978. Том 2. № 1. С. 112.
83Wulfsberg G., West R., Mallikarjuna Rao V. N. // J. Am. Chem. Soc. 1973. Vol. 95. № 26. Р. 8658 - 8665.
84Шорыгин П. П., Петухов В. A., Столярова Л. Г. // Докл. АН СССР. 1964. № 154. С. 441.
85Slutsky J., Kwart H. // J. Am. Chem. Soc. 1973. Vol. 95. № 26. Р. 8678 - 8685.
86Chenard B. L., Zyl C. M Van. // J. Org. Chem. 1986. Vol. 51. № 19. Р. 3561 - 3566.
87Шорыгин П. П., Петухов В. A., Столярова Л. Г. // Докл. АН СССР 1964. Том. 154. С. 441.
88Meyers A. I., Edwards P. D., Rieker W. F., Bailey T. R. // J. Am. Chem. Soc. 1984. Vol. 106. № 11. Р. 3270 - 3276.
89Толалаева Т. В., Несмеянов А. Н. В: Методы элементоорганической химии. Литий. Натрий. Калий. Рубидий. Цезий. Ред. Несмеянов А. Н., Кочешков К. А. Книга первая. М.: Наука, 1963. С. 749-840.
90Watson T. J. N. // J. Org. Chem. 1998. Vol. 63. № 2. Р. 406 - 407.
Приложение.
Таблица 3. Синтезированные соединения их характеристики.
№ | Структурная формула | Выход, % | Т. пл., °С | ИК (KBr) n, см-1 | УФ (C2H5OH) lmaxнм.,(lge) | Найдено/Вычислено, % C H N | Брутто- формула |
| 63 | | 92 | масло | 1575 (С=N) 1672 (С=С) | 236 (3.91) | 63.6 9.5 11.0 63.6 9.8 12.4 | C12H22N2O2 |
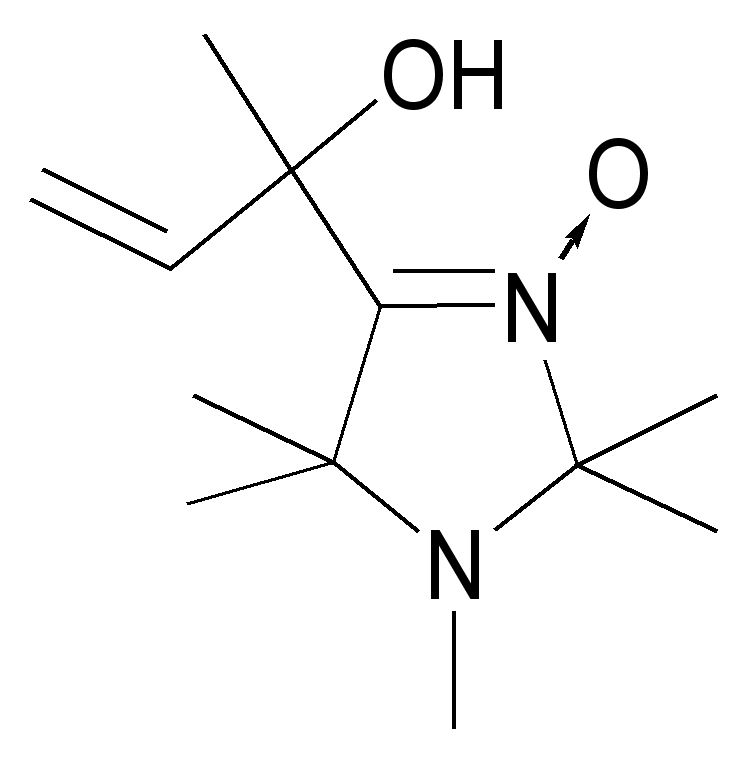
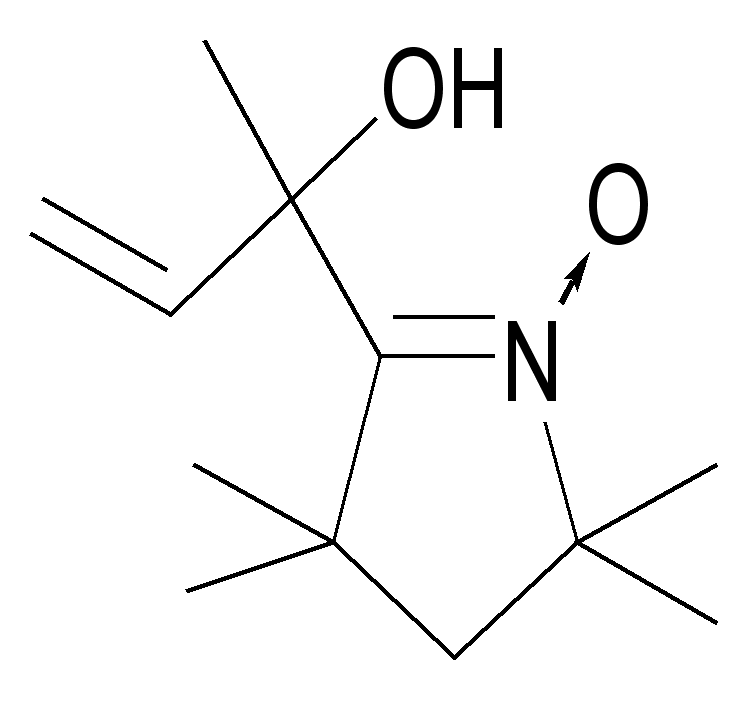
| 64 | | 83 | масло | 1556 (С=N) 1673 (С=С) | 238 (3.97) | 68.3 9.9 6.8 68.2 10.0 6.6 | C12H21NO2 |
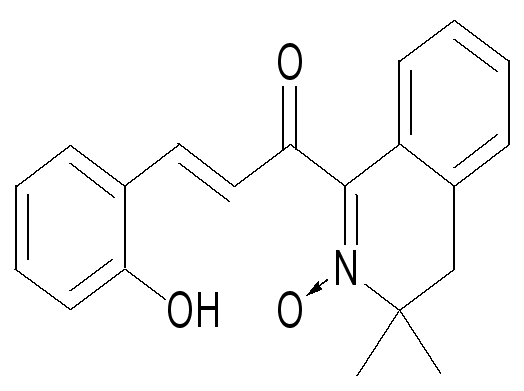
| 65 | | 71 | 164 (CCl4- бензол, 1:1) | 1640 (С=О), 3254 (Ar-OH) 751 (, Ar-H) 1600 (С=N) | 264 (3.76) 265 (3.97) 382 (4.08) | 67,9 8,2 8,8 67,7 8,1 8,9 | C18H26N2O3 |
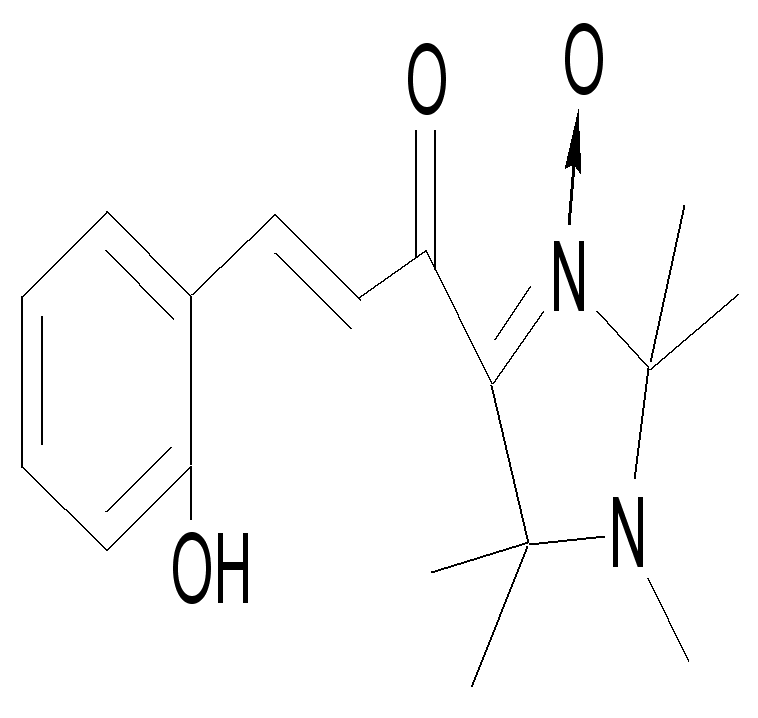
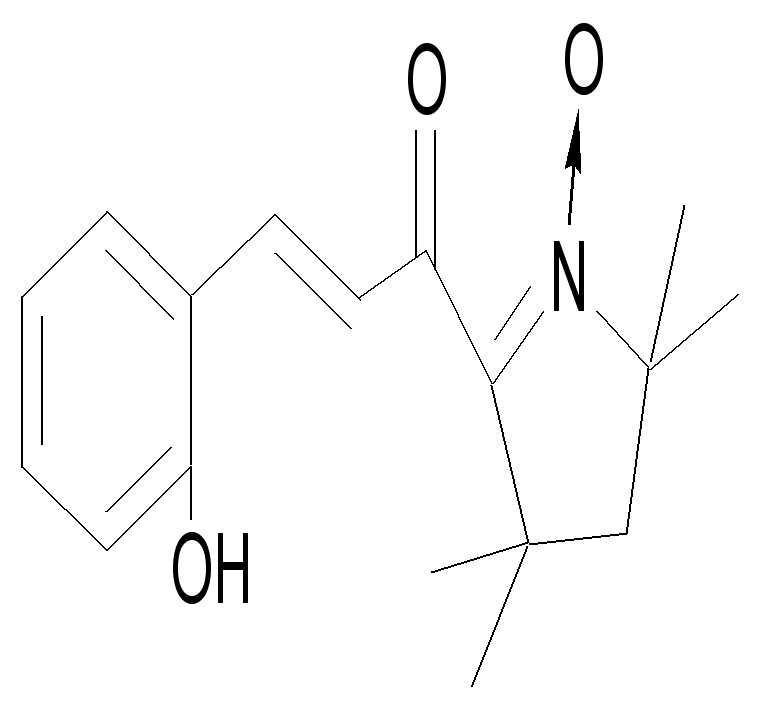
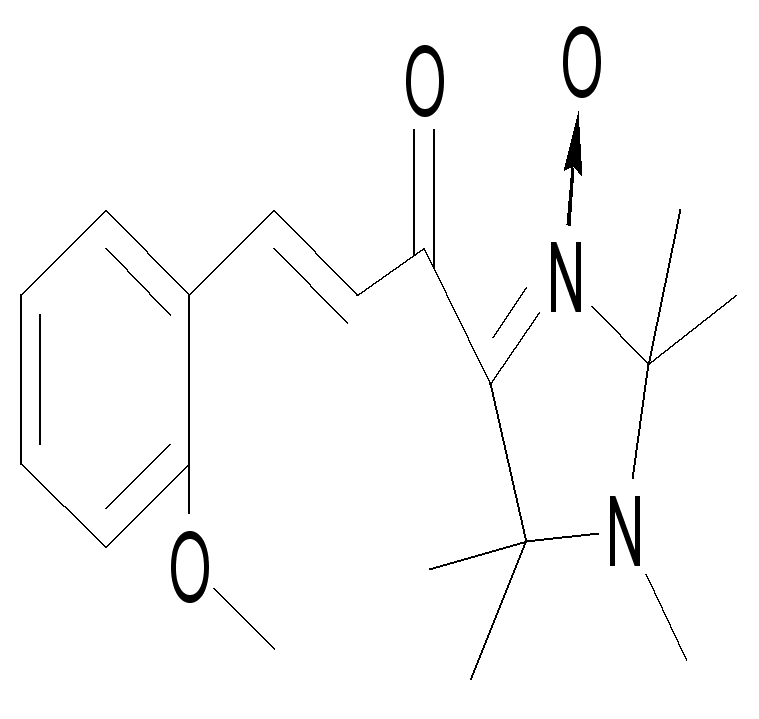
| 65а | | 63 | 176-177ОС (этилацетат-гексан, 4:1) | 1642 (С=О) 3400-3200 (Ar-OH) 753 (, ArH), 1593 (С=N ) | 313 (4,04), 375 (4,13) | 71,1 7,5 4,7 71,1 7,4 4,9 | C17H21NO3 |
| 65б | | 25 | 197-198 гексан-этилацетат 3:1 | 1640, 1610 (C=C-C=O) | 221 (4,22) 231 (4,21) 302 (4,43) 354 (4,13) | 74,6 5,9 4,2 74,7 5,9 4,3 | C20H19NO3 |
| 67 | | 95 | 144-145 гексан-этилацетат 1:1 | 1642, 1586 (C=C-C=O) 1522 | 262 (2,88) 323 (3,06) 373 (3,18) | 68,4 7,7 8,9 68,3 7,6 8,8 | C20H19NO3 |
| 69 | | 60 | 70-74 | 1574 (C=N) | 243 (3.6) | 69.1 9.1 11,9 69,5 9,0 12,1 | C20H31N3O2 |
| 69а | | 75 | 63-65 | 1554 (C=N) | 246 (2.85) | 72.6 9.3 8.4 69,5 9,0 12,1 | C20H31N3O2 |
| 71 | | 83 | 56-60 | 1557 (С=N) 1651 (C=O) | 259 (3.97) | 69.1 7.8 10.9 69.2 7.7 10.8 | C15H20N2O2 |
| 73 | | 50 | 92-94 | 1601 (С=N) | 242 (4.0) | 70,8 7,9 6,45 71,2 7,8 6,4 | C13H17NO2 |
| 73а | | 15 | 104-106 | 1584 (C=N) | 240 (4.03). | 67,6 8,0 11,5 67,7 8,1 11,3 | C14H20N2O2 |
| 74 | | 47 | 145 EtOAc-гексан, 1:1 | 1584 (С=N), 3333 (Н2О крист.) | 235 (3,94) | 59,1 10,7 17,1 59,8 10,3 17,4 | C16H32N4O2 1/2 Н2О |
| 100 | | 90 | 82-83 (гексан) | 1578 (C=N) | 260 (3,78) | Сl 50,4 8,2 14,7 17,6 50,4 7,9 14,7 17,9 | C8H15N2OCl |
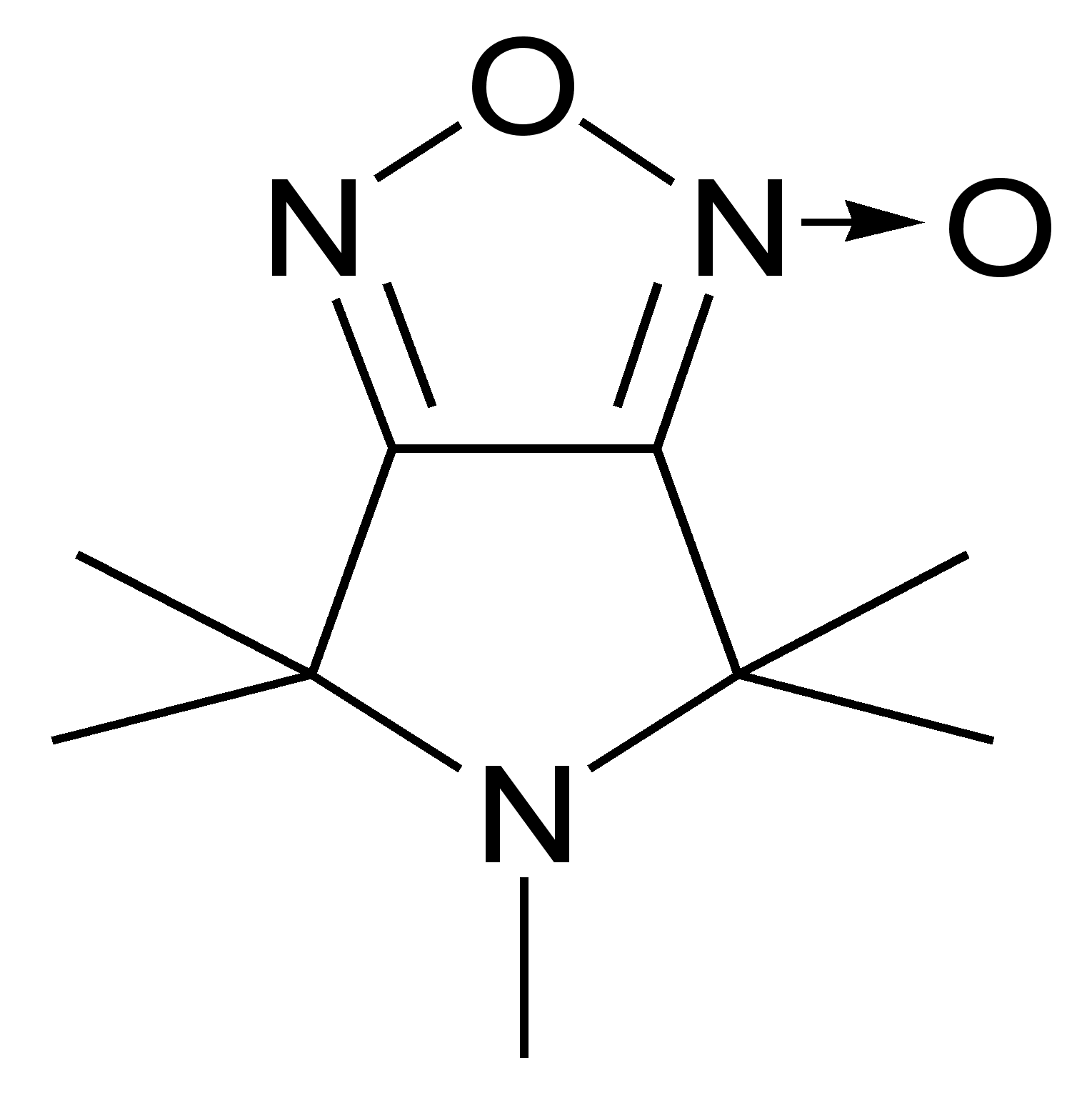
| 102 | | 80 | 89-92 | 1661 (C=N(O)-O-N=C) | 263 (3.67) | 52,9 6,8 23,2 52,7 6,6 23,1 | С9Н15N3O2 |
| 104 | | 30 | 193-194 | 1595 (C=N). | 203 (4,18) 231 (4,06) 267 (3,97) | S 58,1 7,3 9,1 11,8 58,0 7,1 9,0 10,3 | C15H22N2O3S |
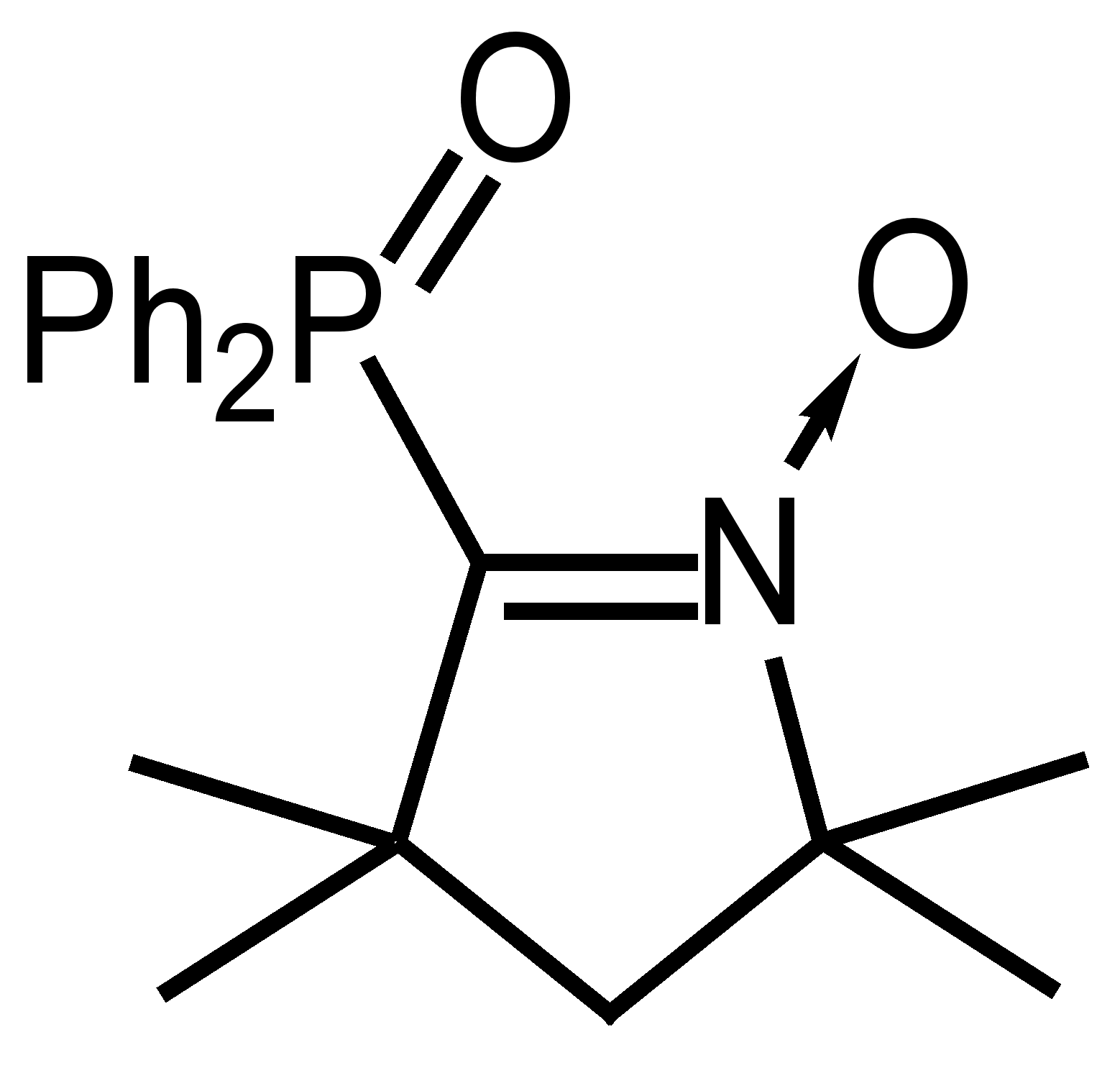
| 105 | | 60 | 131-133 | 1543 (C=N) | 261 (3,89) | Р 67,5 7,0 7,5 8,8 67,4 7,0 7,9 8,7 | C20H25N2PO2 |
| 105a | | 95 | 177-178 гексан-бензол, 1:1 | 1533 (С=N). | 223 (4,47) 266 (3,90) | P 70,3 7,2 4,1 8,7 69,0 6,4 4,5 9,9 | C20H24NO2P |
| 105б | | 60 | 111 гексан | 1533 (С=N) | 225 (4,45) 265 (4,16) | P 69,1 6,3 4,6 9,7 69,0 6,4 4,5 9,9 | C18H20NO2P |
| 106 | | 85 | 110 (гексан-бензол 2:1) | 1562 (С=N). | 259 (3,99) | 54,0 6,5 9,0 54,6 6,2 8,5 | C14H20N2OSe |
| 106а | | 73 | 98-100 (гексан) | 1562 (C=N) | 259 (3,99) | 57,3 6,2 4,7 56,7 6,5 4,7 | C14H19NOSe |
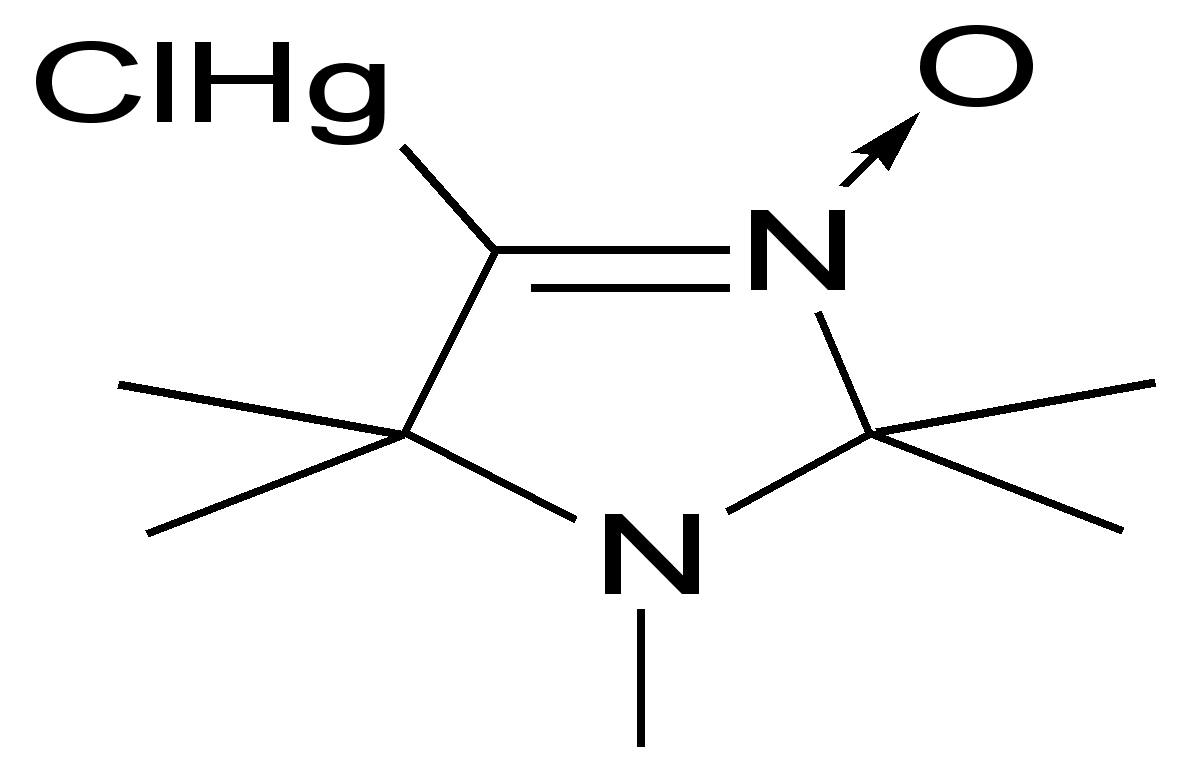
| 107 | | 80 | 201-203 EtOAc-CHCl3, 1:2 | 1576 (C=N) | 265 (3,62) | - | C8H15ClHgN2O |
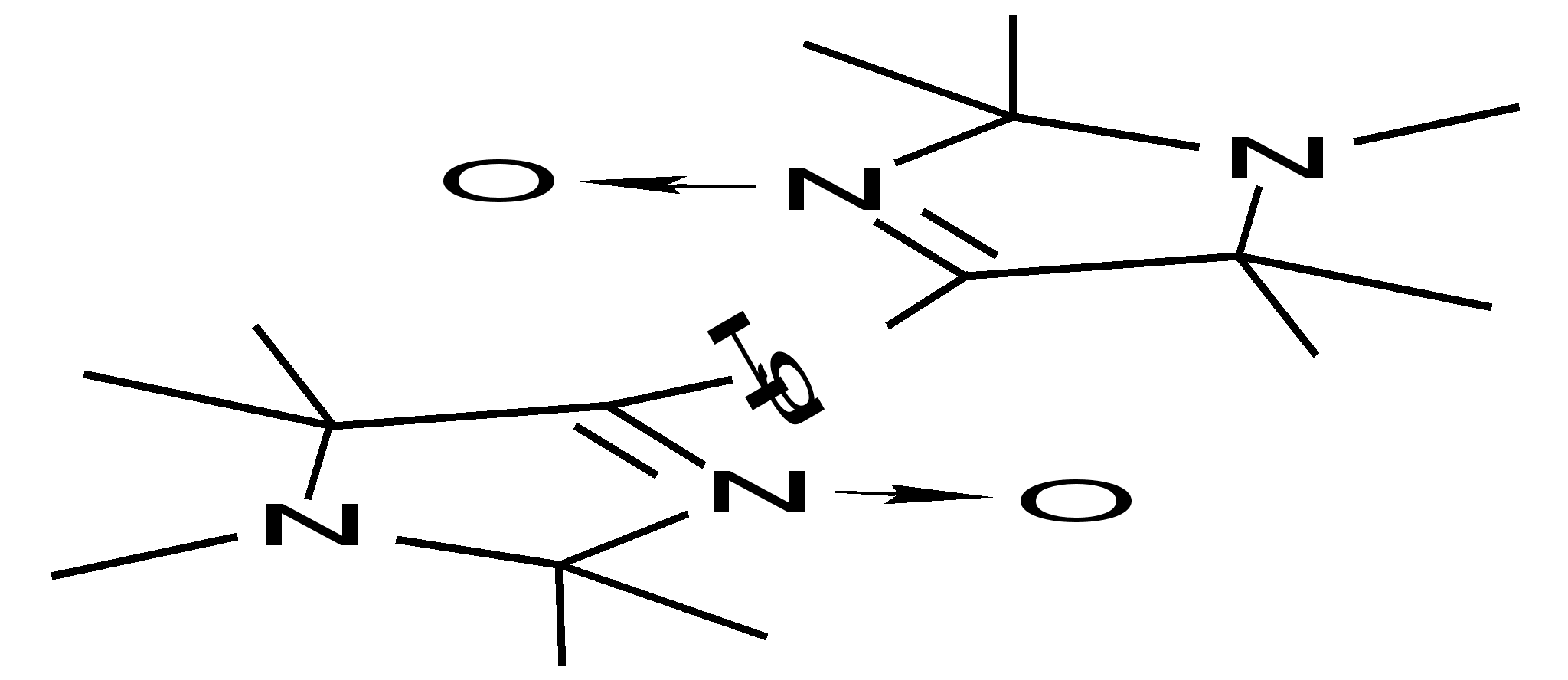
| 108 | | 30 | 185-188 (гексан) | 1558(С=N), 2808(N-CH3) | 263 (3,95). | - | C16H30HgN4O2 |
| 109 | | 25 | 200-204 (гексан) | 1544, 1533 (С=N) | 266 (3,80) | - | C16H28HgN2O2 |
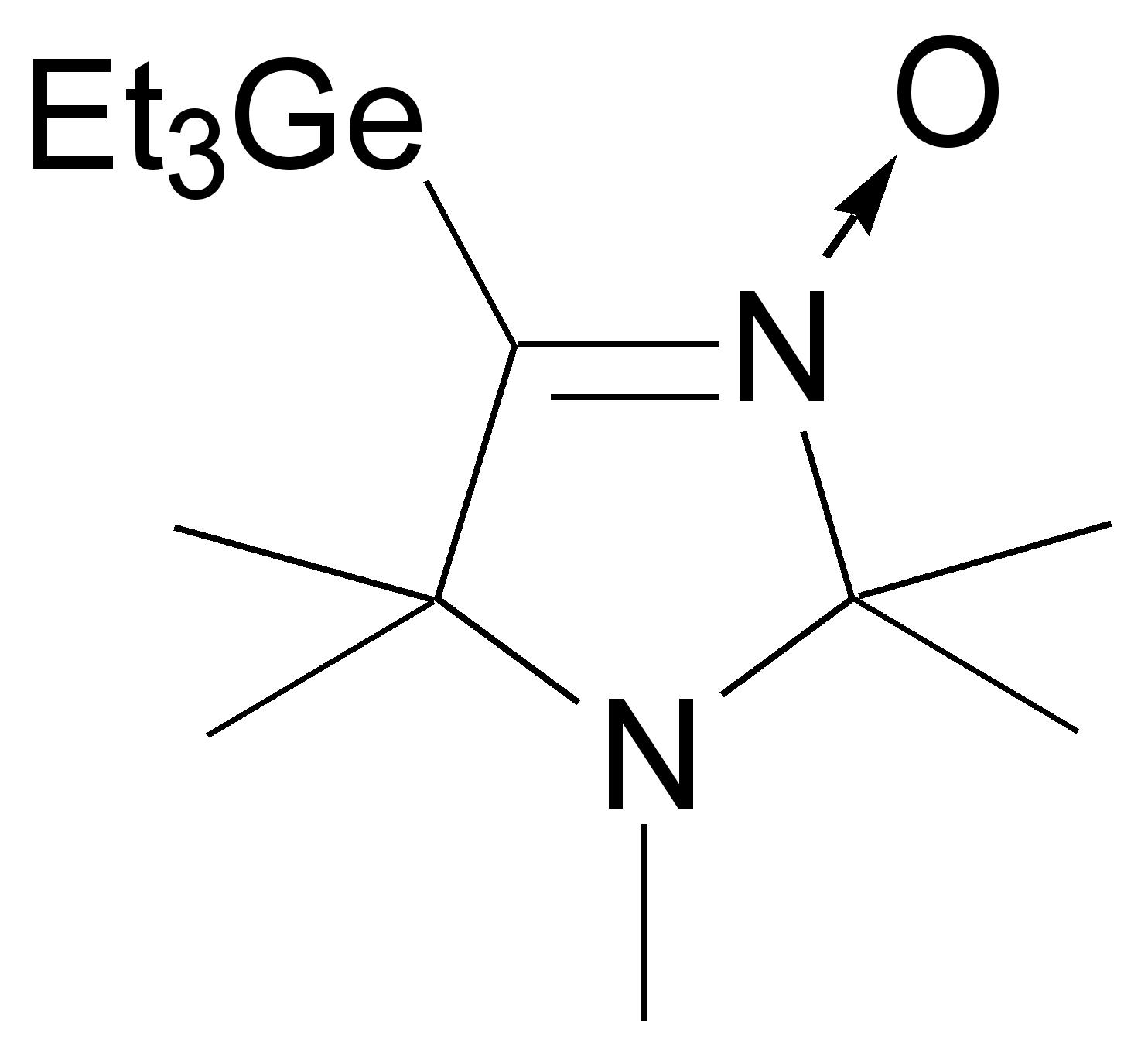
| 110 | | 60 | масло | 1523 (С=N) | 259 (3,67) | 56,5 9,9 4,3 56,0 9,7 4,7 | C14H29GeNO |
| 110a | | 87 | масло | 1533 (C=N) | 257 (3,90) | 53,1 9,9 8,6 52,9 9,5 8,9 | C14H30N2OGe |
| 110б | | 30 | масло | 1527 (C=N) | 249 (3.89). | 53,5 9,7 8,7 53,4 9,6 8,9 | C13H28GeN2O |
Таблица 4. Данные рентгеноструктурного анализа соединения 106.
| Атомы | Длины и углы | Атомы | Длины и углы |
| Se(1)-C(4) | 1.896(4) | N(3)-C(2)-C(8) | 109.4(5) |
| Se(1)-C(11) | 1.928(5) | N(1)-C(2)-C(7) | 117.8(6) |
| O(1)-N(3) | 1.301(5) | N(3)-C(2)-C(7) | 106.9(5) |
| N(1)-C(6) | 1.445(8) | C(8)-C(2)-C(7) | 111.2(7) |
| N(1)-C(2) | 1.455(8) | C(4)-N(3)-O(1) | 126.3(5) |
| N(1)-C(5) | 1.482(7) | C(4)-N(3)-C(2) | 112.8(4) |
| C(2)-N(3) | 1.511(7) | O(1)-N(3)-C(2) | 120.8(4) |
| C(2)-C(8) | 1.512(8) | N(3)-C(4)-C(5) | 111.5(4) |
| C(2)-C(7) | 1.519(11) | N(3)-C(4)-Se(1) | 112.4(3) |
| N(3)-C(4) | 1.288(6) | C(5)-C(4)-Se(1) | 136.0(3) |
| C(4)-C(5) | 1.495(7) | N(1)-C(5)-C(4) | 100.5(4) |
| C(5)-C(10) | 1.520(8) | N(1)-C(5)-C(10) | 107.9(5) |
| C(5)-C(9) | 1.530(7) | C(4)-C(5)-C(10) | 112.1(4) |
| C(11)-C(16) | 1.378(7) | N(1)-C(5)-C(9) | 114.2(5) |
| C(11)-C(12) | 1.390(7) | C(4)-C(5)-C(9) | 111.9(5) |
| C(12)-C(13) | 1.371(9) | C(10)-C(5)-C(9) | 109.8(6) |
| C(13)-C(14) | 1.368(9) | C(16)-C(11)-C(12) | 119.8(5) |
| C(14)-C(15) | 1.396(10) | C(16)-C(11)-Se(1) | 120.0(4) |
| C(15)-C(16) | 1.382(8) | C(12)-C(11)-Se(1) | 119.8(4) |
| C(4)-Se(1)-C(11) | 102.2(2) | C(13)-C(12)-C(11) | 119.5(5) |
| C(6)-N(1)-C(2) | 116.2(4) | C(14)-C(13)-C(12) | 120.8(5) |
| C(6)-N(1)-C(5) | 117.6(4) | C(13)-C(14)-C(15) | 120.3(6) |
| C(2)-N(1)-C(5) | 111.1(4) | C(16)-C(15)-C(14) | 118.8(7) |
| N(1)-C(2)-N(3) | 99.8(4) | C(11)-C(16)-C(15) | 120.7(6) |
| N(1)-C(2)-C(8) | 110.8(5) |
Кристаллы соединения 106 ромбической сингонии:
a = 23.007(2), b = 6.2670(6), c = 10.0814(12) Е, V = 1453.6(3) Е3. Пространственная группа Pna21.
Z = 4, Dc = 1.422 г/см3, R = 0.0302 для 1245 I > 2(I).
Таблица 5. Данные рентгеноструктурного анализа соединения 105.
| Атомы | Длины и углы | Атомы | Длины и углы |
| P(1)-O(2) | 1.4806(14) | N(1B)-C(2)-C(7) | 86.9(6) |
| P(1)-C(17) | 1.792(2) | N(1)-C(2)-C(7) | 120.2(3) |
| P(1)-C(11) | 1.802(2) | N(3)-C(2)-C(7) | 107.8(2) |
| P(1)-C(4) | 1.806(2) | N(1B)-C(2)-C(8) | 138.3(6) |
| O(1)-N(3) | 1.281(2) | N(1)-C(2)-C(8) | 107.6(3) |
| N(1)-C(6) | 1.450(10) | N(3)-C(2)-C(8) | 109.3(2) |
| N(1)-C(5) | 1.473(3) | C(7)-C(2)-C(8) | 111.1(3) |
| N(1)-C(2) | 1.477(3) | O(1)-N(3)-C(4) | 127.78(19) |
| N(1B)-C(2) | 1.440(10) | O(1)-N(3)-C(2) | 118.97(17) |
| N(1B)-C(6B) | 1.51(3) | C(4)-N(3)-C(2) | 113.18(17) |
| N(1B)-C(5) | 1.605(11) | N(3)-C(4)-C(5) | 110.90(18) |
| C(2)-N(3) | 1.497(3) | N(3)-C(4)-P(1) | 122.87(16) |
| C(2)-C(7) | 1.503(4) | C(5)-C(4)-P(1) | 125.87(15) |
| C(2)-C(8) | 1.508(4) | N(1)-C(5)-C(4) | 100.81(17) |
| N(3)-C(4) | 1.298(3) | N(1)-C(5)-C(9) | 118.6(2) |
| C(4)-C(5) | 1.504(3) | C(4)-C(5)-C(9) | 109.83(19) |
| C(5)-C(9) | 1.521(3) | N(1)-C(5)-C(10) | 105.6(2) |
| C(5)-C(10) | 1.523(4) | C(4)-C(5)-C(10) | 113.1(2) |
| C(11)-C(16) | 1.385(3) | C(9)-C(5)-C(10) | 108.9(2) |
| C(11)-C(12) | 1.392(3) | N(1)-C(5)-N(1B) | 33.8(4) |
| C(12)-C(13) | 1.376(4) | C(4)-C(5)-N(1B) | 96.6(4) |
| C(13)-C(14) | 1.371(4) | C(9)-C(5)-N(1B) | 89.6(5) |
| C(14)-C(15) | 1.368(4) | C(10)-C(5)-N(1B) | 135.6(5) |
| C(15)-C(16) | 1.378(4) | C(16)-C(11)-C(12) | 118.5(2) |
| C(17)-C(22) | 1.375(3) | C(16)-C(11)-P(1) | 116.63(17) |
| C(17)-C(18) | 1.383(4) | C(12)-C(11)-P(1) | 124.84(19) |
| C(18)-C(19) | 1.376(4) | C(13)-C(12)-C(11) | 119.8(3) |
| C(19)-C(20) | 1.365(5) | C(14)-C(13)-C(12) | 121.1(3) |
| C(20)-C(21) | 1.359(6) | C(15)-C(14)-C(13) | 119.5(3) |
| C(21)-C(22) | 1.396(4) | C(14)-C(15)-C(16) | 120.3(3) |
| O(2)-P(1)-C(17) | 112.76(10) | C(15)-C(16)-C(11) | 120.8(2) |
| O(2)-P(1)-C(11) | 111.75(10) | C(22)-C(17)-C(18) | 118.8(2) |
| C(17)-P(1)-C(11) | 110.40(10) | C(22)-C(17)-P(1) | 123.1(2) |
| O(2)-P(1)-C(4) | 109.68(9) | C(18)-C(17)-P(1) | 117.69(19) |
| C(17)-P(1)-C(4) | 106.49(10) | C(19)-C(18)-C(17) | 121.5(3) |
| C(11)-P(1)-C(4) | 105.35(10) | C(20)-C(19)-C(18) | 119.1(4) |
| C(6)-N(1)-C(5) | 118.3(5) | C(21)-C(20)-C(19) | 120.7(3) |
| C(6)-N(1)-C(2) | 114.3(5) | C(20)-C(21)-C(22) | 120.5(3) |
| C(5)-N(1)-C(2) | 110.5(2) | C(17)-C(22)-C(21) | 119.5(3) |
| C(2)-N(1B)-C(6B) | 114.9(12) | N(1B)-C(2)-N(1) | 36.0(5) |
| C(2)-N(1B)-C(5) | 105.4(7) | N(1B)-C(2)-N(3) | 99.5(4) |
| C(6B)-N(1B)-C(5) | 106.5(13) | N(1)-C(2)-N(3) | 99.93(17) |
Кристаллы соединения 105 моноклинной сингонии:
a = 12.4029(8), b = 8.9187(5), c = 17.7928(12) Е, V = 1967.9(2) Е3.
Пространственная группа P21/с, Z = 4.
Dc = 1.203 г/см3, R = 0.0456 для 2653 I > 2(I
Похожие работы
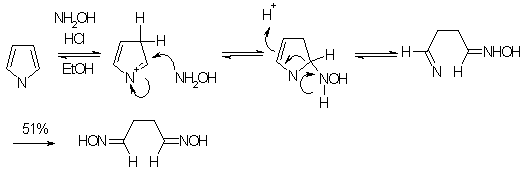
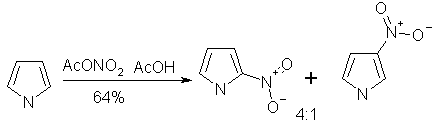
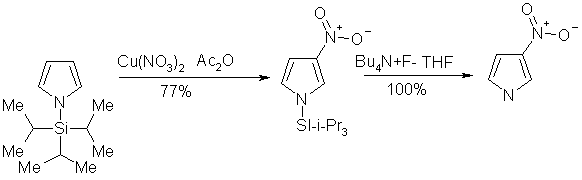
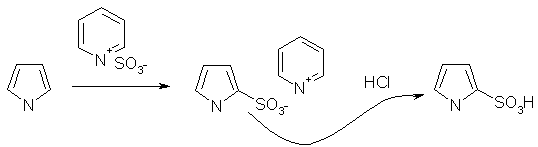
... продуктами олигомеризации и полимеризации. Наиболее гладко пиррол моноалкилируется сопряженными енонами, содержащими уходящую группу в β-положении. 1.2.2 Электрофильное замещение тиофена Как и следовало ожидать, для тиофена характерны реакции, свойственные ароматическим соединениям типа бензола. Тиофен галогенируется, нитруется, сульфируется и ацилируется аналогично фурану и пирролу ...












0 комментариев