Навигация
Растворимые в воде (щелочи) — гидроксиды металлов главных подгрупп I и II групп
1. Растворимые в воде (щелочи) — гидроксиды металлов главных подгрупп I и II групп.
![]()
2. Нерастворимые в воде — гидроксиды остальных металлов.
![]()
Химические свойства. Щелочи изменяют окраску индикаторов (лакмус становится синим, фенолфталеин – малиновым).
Взаимодействие с кислотами:

Взаимодействие с кислотными оксидами:
![]()
Растворы щелочей вступают в реакции ионного обмена с растворами солей, если образующийся при этом гидроксид нерастворим в воде:
![]()
При нагревании слабые основания разлагаются на оксиды металлов и воду:
![]()
Получение оснований. Щелочи получают электролизом растворов солей.
Электролиз раствора хлорида натрия. Процессы на катоде и аноде:
![]()
Уравнение реакции:
![]()
Нерастворимые в воде основания получают реакцией обмена со щелочами:
![]()
Средние соли, их состав, названия, химические свойства (взаимодействие с металлами, кислотами, щелочами, друг с другом с учетом особенностей реакций окисления-восстановления и ионного обмена).
Соли — электролиты, в растворах которых есть катионы металлов или ион аммония и анионы кислотных остатков.
Названия: название аниона + название катиона в родительном падеже + степень окисления металла.
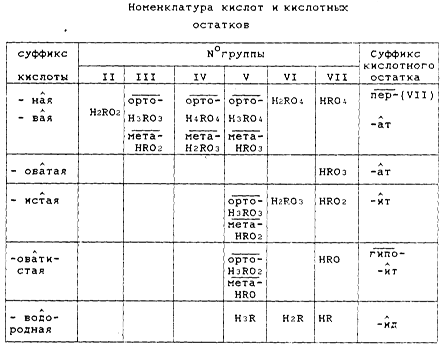
1.B водных растворах соли могут реагировать со щелочами. Так, хлористый магний MgCl2 взаимодействует с едким натром, образуя новую соль и новое основание:
![]()
2. Соли могут реагировать с кислотами. Так, раствор азотнокислого бария Ва(гЮз)а взаимодействует с раствором серной кислоты, образуя новую кислоту и новую соль:
![]()
З.В водных растворах соли могут реагировать между собой.
Если слить вместе водные растворы хлористого кальция CaCl2 я углекислого натрия Na2CO3 TO тотчас же образуется белый осадок нерастворимого в воде углекислого кальция СаСО3, а в растворе — хлористый натрий:
![]()
4. В водных растворах солей металл, входящий в их состав, может замещаться другим металлом, стоящим до него в ряду активности.
Если в раствор сернокислой меди опустить чистую железную проволоку или кусочек цинка, то на их поверхности выделяется медь, а в растворе образуется сернокислое железо (если было опущено железо) или сернокислый цинк (если был опущен цинк):
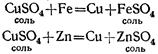
Но из сернокислого цинка нельзя вытеснить цинк медью: медь в ряду активности стоит после цинка.
Билет №18.Гидролиз солей (разобрать первую стадию гидролиза солей, образованных сильным основанием и слабой кислотой, слабым основанием и сильной кислотой).
Взаимодействие ионов соли с водой, в результате которого образуются малодиссоциирующие соединения (ионы или молекулы), называют гидролизом соли
Четыре типа солей, которые по-разному взаимодействуют с водой.
I. Соль образована сильным основанием и сильной кислотой.
NaCI + НОН — ни один из ионов соли с водой не вза-имодействет. Реакция среды нейтральная.
II. Соль образована сильным основанием и слабой кислотой.
![]() - реакция среды щелочная.
- реакция среды щелочная.
Гидролиз солей, образованных сильным основанием и слабой кислотой, заключается в присоединении анионами кислотного остатка ионов водорода и накоплении в растворе гидроксид-ионов, образующихся при диссоциации воды.
Теперь выясним, почему раствор хлорида алюминия приобрел кислую реакцию среды. В растворе АlСl3 диссоциирует на ионы:
![]()
Столкновение ионов Н+ и С– к образованию соединения не приводит. Из имеющихся в растворе ионов малодиссоциирующий продукт образуют ионы Аl3+ и ОН–. Связывание ионов ОН– в малодиссоциирующий ион АlOН2+ (К= 1,38 • 10–9) вызывает дальнейший распад молекул воды на ионы:

Таким образом, в растворе хлорида алюминия осуществляется реакция, в результате которой появляется избыток ионов Н+, т. е. раствор приобретает кислую реакцию. Подобным образом ведут себя в растворах все соли, образованные слабым основанием и сильной кислотой.
III. Соль образована слабым основанием и сильной кислотой.
![]() — реакция среды кислая.
— реакция среды кислая.
Гидролиз соли, образованной слабым основанием и сильной кислотой, заключается в присоединении катионами металла гидроксид-ионов и накоплении в растворе ионов водорода, образующихся при диссоциации воды. Гидролиз хлорида алюминия можно выразить уравнением реакции:
![]()
Реакция среды зависит от сравнительной силы кислоты и основания. В некоторых случаях гидролиз идет до конца:
![]()
Коррозия металлов (химическая и электрохимическая). Способы предупреждения коррозии.
Разрушение металлов и сплавов вследствие химического взаимодействия их с окружающей средой называются коррозией металлов.
Коррозию, вызванную непосредственным химическим взаимодействием между металлом и окружающей средой, называют химической коррозией.
Химическая коррозия — окисление металла без возникновения гальванической пары. Газовая коррозия — при t > 600°С:
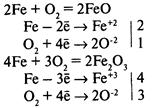
Коррозию, сопровождающуюся возникновением электрического тока за счет появления гальванической пары, называют электрохимической коррозией.
Электрохимическая коррозия – разрушение металла в электролите с возникновением гальванической пары.
![]() – ионы выходят в раствор, электроны перемещаются к менее активному металлу, например к меди.
– ионы выходят в раствор, электроны перемещаются к менее активному металлу, например к меди.
![]() – разряжаются на менее активном металле, например на меди.
– разряжаются на менее активном металле, например на меди.
Одним из наиболее широко распространенных видов электрохимической коррозии является ржавление обычной стали в водной среде и на воздухе. На поверхности металлических изделий всегда имеется пленка влаги, адсорбированной из воздуха. Она является электролитом, так как в ней растворены различные газы (СО2, SO2 и др.). Зерна карбида железа Fe3С химически менее активны, чем железо. Поэтому возникают микрогальваническис элементы: зерна Fe3С играют роль катодов, а зерна чистого железа — роль анодов. Железо разрушается — оно ржавеет. Протекающие при этом процессы весьма сложные. Укажем лишь суммарное уравнение реакции:
![]()
Ржавчина имеет неопределенный состав ![]()
Для защиты от коррозии металлов широко используют лакокрасочные покрытия. Однако краски не вечны, изделия приходится перекрашивать. На это затрачивается ручной труд, расходуется много лакокрасочных материалов.
Из неметаллических покрытий для защиты стали и чугуна большое значение имеет эмаль. Эмаль — это силикатное стекло с добавками оксидов металлов. Ее наносят на поверхность материала в виде порошка и обжигают при 500—1000 °С.
Покрытия из эмалей обладают стойкостью по отношению к щелочам и кислотам, длительно противостоят атмосферной коррозии. Но эмаль легко разрушается при ударе. Благодаря термостойкости, декоративному виду, легкости очистки эмаль широко используется для покрытия изделий домашнего хозяйства и санитарной техники.
С целью защиты металлов от коррозии (и для декоративных целей) издавна используют металлические покрытия. Железо оцинковывают, лудят (покрывают оловом), покрывают никелем, хромируют и т. д.
Защитить металл от коррозии можно с помощью металла и другим способом. Например, если соединить железное изделие или сооружение проводником с куском более активного металла, например магния, то возникает гальванический элемент. При этом сооружение (железо) играет роль катода, а более активный металл выполняет роль анода. Анод разрушается, а катод — защищаемый металл — не изменяется. Такая защита называется протекторной.
Одним из способов борьбы с коррозией является использование ингибиторов. Это химические соединения, ничтожные концентрации которых способны почти полностью предотвращать коррозию. В некоторых случаях применение ингибиторов позволяет изготовлять аппаратуру из обычной стали вместо нержавеющей.
Одно из наиболее эффективных направлений борьбы с коррозией металлов — создание коррозионно-стойких сплавов. В больших количествах выплавляют так называемые нержавеющие стали. В их состав входят металлы (хром, никель), образующие устойчивые защитные оксидные пленки.
Билет №20.Окислительно-восстановительные реакции (разобрать на примерах взаимодействия алюминия с оксидом железа (III), азотной кислоты с медью).
К окислительно-восстановительным реакциям могут быть отнесены химические реакции следующих типов.
Реакции замещения (вытеснения)
Примером реакций этого типа может служить реакция между оксидом железа (III) и алюминием. В этой реакции алюминий вытесняет железо из раствора, причем сам алюминий окисляется, а железо восстанавливается.
![]()
Приведем еще два примера:
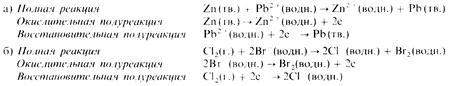
В этой реакции хлор вытесняет бром из раствора (хлор окисляется, бром восстанавливается), содержащего ионы брома.
Реакции металла с кислотами
Эти реакции, в сущности, тоже представляют собой реакции замещения. В качестве примера приведем реакцию между медью и азотной кислотой. Медь вытесняет водород из кислоты. При этом происходит окисление меди, которая превращается в гидратированный катион, а содержащиеся в растворе кислоты гидратированные протоны азота восстанавливаются, образуя оксид азота.

Реакции металлов с водой
Эти реакции тоже принадлежат к типу реакций замещения. Они сопровождаются вытеснением из воды водорода в газообразном состоянии. В качестве примера приведем реакцию между металлическим натрием и водой:
![]()
Реакции металлов с неметаллами
Эти реакции могут быть отнесены к реакциям синтеза. В качестве примера приведем образование хлорида натрия в результате сгорания натрия в атмосфере хлора
![]()
Железо, положение в периодической системе, строение атома, возможные степени окисления, физические свойства, взаимодействие с кислородом, галогенами, растворами кислот и солей. Сплавы железа. Роль железа в современной технике.
Железо находится в побочной подгруппе VIII группы периодической системы. Электронная формула атома железа:
![]()
Типичные степени окисления железа +2 и +3. Степень окисления +2 проявляется за счет потери двух 4s-электронов. Степень окисления +3 соответствует также при потере еще одного Зd-электрона, при этом Зd-уровень оказывается заполненным наполовину; такие электронные конфигурации относительно устойчивы.
Физические свойства. Железо – типичный металл, образует металлическую кристаллическую решетку. Железо проводит электрический ток, довольно тугоплавко, температура плавления 1539°С. От большинства других металлов железо отличается способностью намагничиваться.
Химические свойства. Железо реагирует со многими неметаллами:
![]()
Образуется железная окалина – смешанный оксид железа. Его формулу записывают также так: FeО•Fe2О3.
![]()
Реагирует с кислотами с выделением водорода:
![]()
Вступает в реакции замещения с солями металлов, расположенных правее железа в ряду напряжений:
![]()
Соединения железа. FeО — основной оксид, реагирует с растворами кислот с образованием солей железа (II). Fe2О3 — амфотерный оксид, реагирует также с рас творами щелочей.
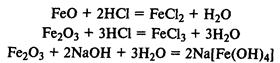
Гидроксиды железа. Fe(ОН)2 — типичный основной оксид, Fe(ОН)3 обладает амфотерными свойствами, реагирует не только с кислотами, но и с концентрированными растворами щелочей.

Гидроксид железа (II) легко окисляется до гидроксида железа (III) кислородом воздуха:
![]()
При реакции солей железа (II) и (III) со щелочами в осадок выпадают нерастворимые гидроксиды:
![]()
Сплавы железа. Современная металлургическая промышленность производит железные сплавы разнообразного состава.
Все железные сплавы разделяются по составу и свойствам на две группы. К первой группе относятся различные сорта чугуна, ко второй — различные сорта стали.
Чугун хрупок; стали же пластичны, их можно ковать, прокаты^ вать, волочить, штамповать. Различие в механических свойствах чугунов и сталей зависит прежде всего от содержания в них углерода — в чугунах содержится около 4% углерода, а в сталях — обычно менее 1,4%.
В современной металлургии из железных руд получают сначала чугун, а затем из чугуна — сталь. Чугун выплавляют в доменных печах, сталь варят в сталеплавильных печах. До 90% всего выплавленного чугуна перерабатывают в стали.
Чугун. Чугун, предназначенный для переработки в сталь, называют передельным чугуном. Он содержит от 3,9 до 4,3% С, 0,3—1,5% Si, 1,5—3,5% Мn, не более 0,3% Р и не более 0,07% S. Чугун, предназначенный'для получения отливок, называется литейным чугуном, В доменных печах выплавляются также ферросплавы, применяемые преимущественно в производстве сталей в качестве добавок. Ферросплавы имеют, по сравнению с передельным чугуном, повышенное содержание кремния (ферросилиций), марганца (ферромарганец), хрома (феррохром) и других элементов.
Стали. Все стали делятся на углеродистые и легированные.
Углеродистые стали содержат в несколько раз меньше углерода, кремния и марганца, чем чугун, а фосфора и серы совсем мало. Свойства углеродистой стали зависят прежде всего от содержания в ней углерода: чем больше в стали углерода, тем она твёрже. Промышленность производит мягкие стали, стали средней твёрдости и твёрдые. Мягкие стали и стали средней твёрдости применяются для изготовления деталей машин, труб, болтов, гвоздей и т. д., а твёрдые стали—для изготовления инструментов.
В сталях должно быть возможно меньше серы и фосфора, так как эти примеси ухудшают механические свойства сталей. В повышенных количествах сера вызывает красноломкость — образование трещин при горячей механической обработке металла. Фосфор вызывает хладноломкость—хрупкость стали при обыкновенной температуре. -
Легированные стали. Физические, химические и механические свойства сталей существенно изменяются от введения в их состав повышенного количества марганца и кремния, а также хрома, никеля, вольфрама и других элементов. Эти элементы называются легирующими, а стали — легированными [от латинского слова ligare – связывать, соединять].
Наиболее широко в качестве легирующего элемента применяется хром. Особенно большое значение для сооружения машин, аппаратов и многих деталей машин имеют хромоникелевые стали. Эти стали обладают высокой пластичностью, прочностью, жаростойкостью и стойкостью к действию окислителей. Азотная кислота любой концентрации не разрушает их даже при температурах кипения. Хромоникелевые стали не ржавеют в атмосферных условиях и в воде. Блестящие, серебристого цвета, листы хромоникелевой стали украшают арки станции «Маяковская» Московского метро. Из этой же стали делают нержавеющие ножи, ложки, вилки и другие предметы домашнего обихода.
Молибден и ванадий повышают твёрдость и прочность сталей при повышенных температурах и давлениях. Так, хромомолибденовые и хромованадиевые стали применяются для изготовления трубопроводов и деталей компрессоров в производстве синтетического аммиака, авиационных моторов.
При резании с большой скоростью инструмент сильно разогревается и быстро изнашивается. При добавлении вольфрама твёрдость стали сохраняется и при повышенных температурах. Поэтому хромовольфрамовые стали применяются для изготовления режущих инструментов, работающих при больших скоростях '
Увеличение содержания в стали марганца повышает её сопротивление трению и удару. Марганцовистые стали применяются для изготовления железнодорожных скатов, стрелок, крестовин, камнедробильных машин.
Применение легированных сталей позволяет значигельно снизить вес металлических конструкций, повысить их прочность, долговечность и надёжность в эксплуатации.
Билет №22.Высшие кислородосодержащие кислоты химических элементов третьего периода, их состав и сравнительная характеристика свойств.
Фосфор образует целый ряд кислородсодержащих кислот (оксокислот). Некоторые из них мономерны. например фосфиновая, фосфористая и фосфорная(V) (ортофосфорная) кислоты. Кислоты фосфора могут быть одноосновными (однопротонными) либо многоосновными (многопротонными). Кроме того, фосфор образует еще полимерные оксокислоты. Такие кислоты могут иметь ациклическое либо циклическое строение. Например, дифосфорная(V) (пирофосфорная) кислота представляет собой димерную оксокислоту фосфора.
Наиболее важной из всех этих кислот является фосфорная(V) кислота (другое ее название - ортофосфорная кислота). При нормальных условиях она представляет собой белое кристаллическое вещество, расплывающееся при поглощении влаги из воздуха. Ее 85%-ный водный раствор называют «сиропообразной фосфорной кислотой». Фосфорнця(V) кислота является слабой трехосновной кислотой:
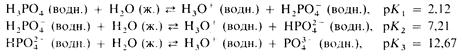
Хлор образует несколько кислородсодержащих кислот. Чем выше степень окисления хлора в этих кислотах, тем выше их термическая устойчивость и сила кислоты:
НОCl < НСlO2 < НСlO3 < НClO4
НClO3 и НClO4 – сильные кислоты, причем НСlO4 – одна из самых сильных среди всех известных кислот. Остальные две кислоты лишь частично диссоциируют в воде и существуют в водном растворе преимущественно в молекулярной форме. Среди кислородсодержащих кислот хлора только НСlO4 удается выделить в свободном виде. Остальные кислоты существуют только в растворе.
Окислительная способность кислородсодержащих кислот хлора уменьшается с возрастанием его степени окисления:
![]()
НОСl и НClO2 – особенно хорошие окислители. Например, кислый раствор НОCl:
1) окисляет ионы железа (II) до ионов железа (III):
![]()
2) на солнечном свету разлагается с образованием кислорода:
![]()
3) при нагревании приблизительно до 75 °С он диспропорционирует на хлорид-ионы и хлорат (V)-ионы:
![]()
Остальные высшие кислотсодержащие кислоты элементов третьего периода (H3AlO3, H2SiO3) более слабые, чем фосфорная кислота. Серная кислота (H2SO4) менее сильнае, чем хлорная (VII) кислота, но более сильная, чем фосфорная кислота. Вообще, при увеличении степени окисления элемента, образующего кислоту, увеличивается сила самой кислоты:
H3AlO3 < H2SiO3 < H3PO4 < H2SO4 < НСlO4
Билет №23.Общие способы получения металлов.
Металлы находятся в природе преимущественно в виде соединений. Только металлы с малой химической активностью (благородные металлы) встречаются в природе в свободном состоянии (платиновые металлы, золото, медь, серебро, ртуть). Из конструкционных металлов в достаточном количестве имеются в природе в виде соединений лишь железо, алюминий, магний. Они образуют мощные залежи месторождений относительно богатых руд. Это облегчает их добычу в больших масштабах.
Поскольку металлы в соединениях находятся в окисленном состоянии (имеют положительную степень окисления), то получение их в свободном состоянии сводится к процессу восстановления:
![]()
Этот процесс можно осуществить химическим или электрохимическим путем.
При химическом восстановлении в качестве восстановителя чаще всего применяют уголь или оксид углерода (II), а также водород, активные металлы, кремний. С помощью оксида углерода (II) получают железо (в доменном процессе), многие цветные металлы (олово, свинец, цинк и др.):
![]()
Восстановление водородом используется, например, для получения вольфрама из оксида вольфрама (VI):
![]()
Применение в качестве восстановителя водорода обеспечивает наибольшую чистоту получаемого металла. Водород используют для получения очень чистого железа, меди, никеля и других металлов.
Способ получения металлов, в котором в качестве восстановителя применяют металлы, называют металлотермическим. В этом способе в качестве восстановителя используют активные металлы. Примеры металлотермических реакций:
алюминотермия:
![]()
магниетермия:
![]()
Металлотермические опыты получения металлов впервые осуществил русский ученый Н. Н. Бекетов в XIX в.
Металлы наиболее часто получают восстановлением их оксидов, которые в свою очередь выделяют из соответствующей природной руды. Если исходной рудой являются сульфидные минералы, то последние подвергают окислительному обжигу например:
![]()
Электрохимическое получение металлов осуществляется при электролизе расплавов соответствующих соединений. Таким путем получают наиболее активные металлы, щелочные и щелочноземельные металлы, алюминий, магний.
Электрохимическое восстановление применяют также для рафинирования (очистки) «сырых» металлов (меди, никеля, цинка и др.), полученных другими способами. При электролитическом рафинировании в качестве анода используют «черновой» (с примесями) металл, в качестве электролита — раствор соединений данного металла.
Способы получения металлов, осуществляемые при высоких температурах, называют пирометаллургическими (по-гречески pyr — огонь). Многие из этих способов известны с древних времен. На рубеже XIX—XX вв. начинают развиваться гидрометаллургические способы получения металлов (по-гречески hydor—вода). При этих способах компоненты руды переводят в водный раствор и далее выделяют металл электролитическим или химическим восстановлением. Так получают, например, медь. Медную руду, содержащую оксид меди (II) CuО, обрабатывают разбавленной серной кислотой:
![]()
Для восстановления меди полученный раствор сульфата меди (II) либо подвергают электролизу, либо действуют на раствор порошком железа.
Гидрометаллургический способ имеет большое будущее, так как позволяет получать продукт, не извлекая руду из земли. (Сравните достоинства гидрометаллургического способа получения металлов с подземной газификацией угля.)
Похожие работы
... оксидами, основаниями, солями (на примере H2SO4, HCl). 2)Задача. вычислить массовую долю (в %) каждого химического элемента в веществе, формула которого Na2SO4. Билет № 15 1)Амфотерные гидрооксиды (на примере Zn(OH)2, Al(OH)3). Взаимодействие их с кислотами, щелочами, и отличительные свойства от оснований. 2)Задача. Вычислить количество одного из продуктов реакции, если известна масса ...
... , Хрущев. 7) Борьба с космополитизмом - идеологией мирового гражданства. Она предусматривает отказ от национальных традиций, культуры, патриотизма. Отрицание гос. и нац. суверенитета. Космополит своим отечеством считает весь мир. В конце 40-х развертывается борьба с космополитизмом. Обвинение - в измене Родине. Опасность Зап. влияния через воинов-победителей, познакомившихся с жизнью в Европе. ...
... Выгодное приморское положение у берегов балтийского моря. 2) Исторический торговый путь «Из варяг в греки», на котором возникла Новгородская Русь. 3)Наличие двух крупных портов международного класса (Калининград, Санкт-Петербург). 4) в 1990 году Санкт-Петербург выведен в зону свободного предпринимательства. 5)Граничит с высокоразвитыми странами Европы. 6)Компактная территория с равнинным рельефом. ...
... учебного времени - четверти, полугодия и т. п.). Заключительный контроль проводится в конце года или в конце всего курса обучения в виде выпускного экзамена. Внутри названных форм и видов контроля усвоения различают методы контроля. Их рассматривают по группам, соответствующим устной, письменной, экспериментальной и компьютерной формам проверки. В арсенале учителя много методов контроля ...
0 комментариев