Навигация
Значение пассивности металлов
5. Значение пассивности металлов.
Пассивное состояние металлов имеет большое практическое значение. Коррозионная стойкость ряда металлов , например алюминия и магния в воздухе и воде , титана во многих коррозионных средах , часто бывает обусловлена их пассивностью .
Коррозионную стойкость металлов можно увеличить , легируя их другими более пассивными металлами . Так , например , легирование сталей хромом (13-18% Cr) делает их нержавеющими и кислотоустойчивыми .
На графике представлена кинетика коррозии хромоникелевой стали Х18Н9 в 50-% H2SO4 при 50°С.
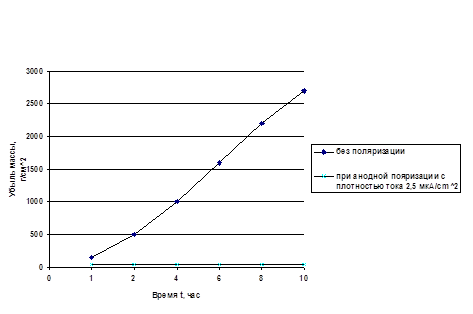
Повышения коррозионной стойкости металлов можно достигнуть одним из трёх основных способов :
а) введением компонентов , способствующих образованию более совершенного экранирующего защитного слоя продуктов коррозии на поверхности сплава ;
б) введением компонентов , уменьшающих катодную активность ;
в) введением компонентов , уменьшающих анодную активность .
Примером первого способа легирования является повышение коррозионной стойкости углеродистой стали при легировании хромом , никелем , титаном и т. д. .
Установлено , что коррозионная стойкость твёрдых растворов , полностью гомогенных и при отсутствии заметной диффузии , при легировании менее устойчивого металла более устойчивым изменяется не непрерывно , а скачками :

Резкое изменение коррозионной стойкости происходит , когда концентрация легирующего элемента достигает 1/8 атомной доли или величины , кратной этому числу , т. е. 2/8 , 3/8 , 4/8 , и т. д. атомной доли- правило n/8 Таммана. Положение границы устойчивости (значение n) зависит не только от системы твёрдых растворов , но и от реагента , т. е. его агрессивности и внешних условий .) зависит не только от системы твёрдых растворов , но и от реагента , т. е. его агрессивности и внешних условий .
Правило Таммана было подтверждено на большом числе примеров , в том числе и на имеющих большое практическое значение технических сплавах , таких как Fe-Cr (n=1,2&3) Для некоторых систем твёрдых растворов в одном реагенте наблюдается несколько границ устойчивости , причём одной из них соответствует наиболее резкое уменьшение скорости коррозии (рис.4) .
Для объяснения границ устойчивости предложено существование сверхструктур (упорядоченного расположения атомов) в твёрдых растворах , при котором возможно появление защитных плоскостей в решётке сплава , обогащённых или сплошь занятых атомами устойчивого элемента (например Cr в твёрдом растворе Cr+Fe) . При действие реагента на сплав разрушается несколько атомных слоёв сплава до тех пор , пока не будут достигнуты эти защитные плоскости и скорость растворения сплава резко снизится .
Правило n/8 Таммана позволяет рационально корректировать содержание легирующего элемента твёрдого раствора , вводимого в целях повышения коррозионной стойкости сплава . При этом следует учитывать возможность обеднения твёрдого раствора легирующим элементом за счёт связывания его другими компонентами сплава (хрома углеродом в карбиды) и в связи с этим необходимости введения в сплав дополнительного количества легирующего элемента для обеспечения необходимого содержания его в твёрдом растворе . Так содержание хрома в коррозионностойких хромистых сталях составляет 12-14 % при содержании углерода 0,1-0,2 % .
6. Структурная гетерогенность сплавов .
Гетерогенность сложно влияет на коррозионную стойкость сплавов .
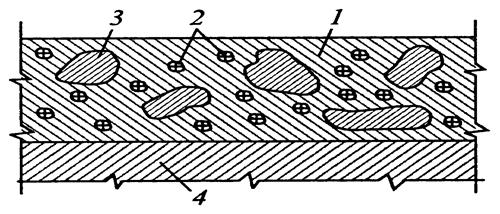
Влияние анодной структурной составляющей сплава на коррозионную стойкость зависит от характера распределения анодной фазы в сплаве: если анодом является узкая зона границы зерна вследствие или обеднения в этой узкой зоне твёрдого раствора легирующим элементом (хромом) , или образование непрерывной цепочки , неустойчивой или затрудняющей образование новой фазы , или больших механических напряжений , возникающих при образовании избыточной фазы , то это приводит к интенсивной коррозии границ зёрен , т. е. к межкристаллитной коррозии .
Электрохимическая гетерогенность сплава в зависимости от условий может или не влиять на коррозионную стойкость металлов , или увеличивать , или уменьшать её .
Опытные данные по коррозии ряда металлов и сплавов , в том числе хромистых сталей , указывают на то , что величина зерна мало влияет на скорость коррозии . Исключения составляют случаи , когда на границе зёрен металла условия таковы , что коррозия может приобрести межкристаллитный характер . Увеличение размеров зерна заметно усиливает межкристаллитную коррозию , так как уменьшится длина границ зёрен , следовательно интенсивность коррозии возрастёт .
7. Механический фактор.
Приведённая ниже таблица наглядно демонстрирует изменение механических характеристик хромистой стали по сравнению с углеродистой :
| Характеристика | Сталь углеродистая (0.25%С) | Хромистая сталь (13%Cr) |
| Предел прочности , кг/мм^2 | 39 | 62 |
| Предел усталости при N=5*10^7 циклов , кг/мм^2 | 16.5 | 38 |
| Условный предел коррозионной усталости при N=5*10^7 циклов , кг/мм^2 в пресной воде в морской воде | 12 --- | 26 21 |
Как видно из таблицы , все вышеприведённые механические показатели для хромистой стали почти в 2 раза выше , чем для углеродистой . Не оставляет сомнений тот факт , что качественный уровень хромистой стали гораздо выше , чем углеродистой , хотя бы даже из-за возможности применения хромистой стали в морской воде .
8. Кавитационное воздействие.
При больших скоростях движения в жидкости образуются пространства с пониженным давлением в виде вакуумных пузырей . Гидравлические удары , возникающие при замыкании этих пузырей на поверхности металла , создают пульсирующие напряжения , которые разрушают не только защитные плёнки , но и структуру самого металла со скоростями иногда доходящими до 75 мм/год . Этот особый вид коррозии называют кавитационной коррозией . На кавитационную стойкость металлов и сплавов большое влияние оказывает механическая прочность , структура и состояние границ зёрен сплава .
Особой устойчивостью к кавитационной коррозии отличается сталь 30Х10Г10 , которая самоупрочняется в процессе кавитации .
Повышения коррозионно-кавитационной стойкости деталей машин достигают наряду с другими необходимыми мероприятиями ещё и повышением прочности и коррозионной устойчивости сплава (легирование хромом , никелем и др.) , а так же нанесением различных покрытий (наплавкой более стойки сплавов ,хромированием , с помощью армированных эпоксидных покрытий и др.) .
Заключение.
Следуя вышесказанному мы можем говорить о том , что даже незначительные добавки хрома в углеродистую сталь делают её коррозионностойкой , кислотостойкой , улучшают её механические характеристики (повышается пластичность с увеличением прочности) , повышается её термодинамическая устойчивость а следовательно значительно расширяют область применения этих сталей . Так стали типа Х13 - самые распространённые и наиболее дешёвые нержавеющие стали ; их применяют для бытовых назначений и в технике (лопасти гидротурбин , лопатки паровых турбин) . Стали эти хорошо свариваются . Из сталей 2Х13 и 4Х13 изготавливают детали повышенной прочности благодаря их хорошим механическим свойствам. Сталь Х17 можно применять как жаростойкую при рабочих температурах до 900°С , стали с содержанием Cr 25-28 % работают при температурах 1050-1150°С .
Большим недостатком этих сталей является то , что возникающая при перегреве (например при сварке) крупнозернистость не может быть устранена термической обработкой , так как в этих сталях нет фазовых превращений . Крупнозернистость создаёт повышенную хрупкость стали (порог хладноломкости переходит в область положительных температур).
СПИСОК ЛИТЕРАТУРЫ.
1. Н. П. Жук «Курс коррозии и защиты металлов».
2. А. П. Гуляев «Металловедение».
3. Под редакцией Туманова А. Т. «Методы исследования механических свойств металлов».
4. А. В. Бакиев «Технология аппаратостроения».
Похожие работы
... они брали ту самую "чистую" медь, почему соединили ее именно с оловом, а не с каким-нибудь другим металлом, в каких месторождениях встречается в природе медь, в каких именно химических соединениях, где эти месторождения расположены и насколько легко было древним людям ее вырабатывать и переплавлять? Очень странно, что кабинетные историки совершенно не утруждают себя подобными вопросами. А, ведь, ...
... Основным критерием, характеризующим состояние поверхности металла, является электродный потенциал. Обычно возможность применения анодной защиты для конкретного металла или сплава определяют методом снятия анодных поляризационных кривых. При этом получают следующие данные: а) потенциал коррозии металла в исследуемом растворе; б) протяженность области устойчивой пассивности; в) плотность тока в ...
... является промывная вода. Глава 4. Катодное поведение металлов и графита в разбавленных Cr-содержащих растворах. Повышение эффективности электрохимического способа очистки промывных и сточных вод от ионов Сг (VI) предусматривает изучение как анодных, так и катодных процессов в разбавленных хромсодержащих электролитах.Т. к. электровосстановление Сг (VI) на графитовом материале протекает легко, то ...
... , технической и патентной литературы (пп.1.1-1.5, [90, 91, 190]) по опыту использования многокомпонентных конденсированных структур, а также используя результаты фундаментальных исследований в области получения различных конденсационных покрытий [27, 54, 60, 124, 125, 135, 142], можно предложить достаточно наглядную классификацию всех существующих и принципиально возможных методов получения ...








0 комментариев