Навигация
Марта 1912 г. Резерфорд написал из Манчестера старому другу: «Бор, датчанин, покинул Кембридж и появился здесь...»
18 марта 1912 г. Резерфорд написал из Манчестера старому другу: «Бор, датчанин, покинул Кембридж и появился здесь...»
После того как на самом рубеже XIX–ХХ вв. – в 1900 г. – пятидесятитрехлетний профессор из Берлина Макс Планк впервые произнес слово квант, в физику вошло странное представление о своеобразных атомах электромагнитной энергии. Свет стал подобен остальной материи. Дробность строения вместо непрерывности. В рамках классической физики осмыслить эту новость не удавалось. И нельзя было питать надежду, что в классическом мире найдется законное место для новой универсальной постоянной, открытой Планком. Многие физики тогда еще полагали, что она не более чем вымышленная величина, родившаяся в теоретических снах. Планк недаром назвал новую константу «таинственным послом из реального мира».
Каков же он, этот реальный мир? Как устроены недра материи, откуда явился сей таинственный посол? Все задавали друг другу вопросы – частные и общие. И чем содержательней был вопрос, тем менее удовлетворителен ответ. А пока... Пока дела складывались отлично. Найдя понимание и сочувствие, Бор нашел себя. 12 июня ушло знаменательное письмо к брату Харальду: «Я начал разрабатывать маленькую теорию, которая... быть может, прольет некоторый свет на ряд проблем, связанных со структурой атомов...»
«Маленькая теория» накрепко привязала его к столу. Суток вдруг перестало хватать для работы. Он стал добровольным затворником. Много лет спустя, вспоминая Резерфорда, Бор написал: «В раннюю пору моего пребывания в Манчестере... я пришел к убеждению, что строение электронного роя в резерфордовском атоме управляется квантом действия (постоянной Планка...)»
Однако далеко не торным оказался путь от верно угаданного принципа до жизнеспособной теории. Бор говорил, Резерфорд молчал. Он не хотел вникать в математические подробности, а физическими не был удовлетворен. Но Бор не услышал: «Ступайте-ка домой, мой мальчик». Кроме антирезерфордовского совета «не спешить», Бор услышал вполне резерфордовское напутствие: бросить возню со сложными атомными системами, а отдаться простейшей – водородному атому... Прощались они недолго, и выглядело это так, точно Бор никуда не уезжал, а только оставлял на четверть часа аудиторию, поскольку прозвучал звонок на перемену...
Возвращение из Англии осенью 1912 г. стало для Бора памятным рубежом. Теперь у него появилась должность в Копенгагенском университете: ассистент профессора Кнудсена. Но профессор чувствовал с первого дня: его ассистент, присутствуя, в действительности отсутствует. И спустя некоторое время он согласился – по просьбе Бора – предоставить его самому себе... Между 3 и 5 февраля 1913 г. в историю физики на минуту заглянул товарищ Бора по студенческим занятиям – Ханс Мариус Хансен. Бор говорил, что Хансен оказался тогда в Копенгагене «единственным физиком, которому интересны были эти вещи». И сердце его нового слушателя-спектроскописта дрогнуло от надежды...
– А спектры? – вдруг спросил Хансен. – Как твоя теория объясняет спектральные формулы?
– Спектральные формулы?!
– Тебе необходимо посмотреть эти формулы. Ты увидишь, с какой замечательной простотой они описывают спектры!
– Я посмотрю...
Они попрощались...
Школьному учителю, швейцарцу Иоганну Якобу Бальмеру было шестьдесят лет, когда в 1885 г. он опубликовал свою формулу – плод великого долготерпения. Он не знал об устройстве атома ничего и располагал лишь таблицей данных о длинах световых волн в спектре водорода. Но, увидев эту формулу, Бор уже не мог от нее оторваться. А Леон Розенфельд засвидетельствовал: «Он говорил мне не раз: “Как только я увидел формулу Бальмера, все немедленно прояснилось передо мной”».
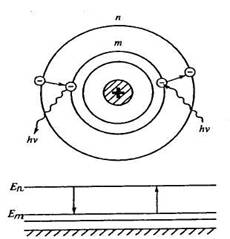
Что же увидел Бор? Лестницу разрешенных Природой уровней энергии в атоме. Двигаться по такой лестнице можно было лишь со ступеньки на ступеньку. Задержаться меж ступенек Природа не позволяла. Кроме электрона некому быть ее строителем. И кроме его планетных орбит нечему служить ее ступеньками. Лестница разрешенных уровней энергии увиделась как паутина дозволенных электронных орбит. Чем дальше от ядра пролегает орбита – тем выше энергия атома. Чем ближе к ядру, тем ниже энергетическая ступенька. На каждой из них, до момента испускания кванта электрон вопреки классике ничего не излучает. А в момент испускания он сваливается вниз, и его подхватывает другая, более близкая к ядру орбита. И он начинает теперь вращаться на ней, снова не излучая. А квант покидает атом в процессе самого перескока электрона. И только от глубины падения с орбиты на орбиту зависит величина улетающего кванта – его частота. Или цвет спектральной линии. Среди орбит электрона есть первая. Ниже – ядро. С этой нижней орбиты электрону некуда падать. И он может вращаться на ней бессрочно. Ее радиус и задавал нормальный размер атома.
...Он явился в хорошо знакомый дом на Уилмслоу-роуд прямо с вокзала. Резерфорды были в тот будний вечер не одни. У них остановился давний друг из Монреаля – профессор Ив. Имя Бора ничего не сказало Иву. И оттого ему особенно запомнилась поспешность, с какой хозяин тотчас увел молодого гостя к себе в кабинет... Все последующее происходило без свидетелей. Время уходило вечер за вечером. Но вряд ли это мучило обоих. Им сладостно было утруждать свои головы размышлениями о реальной природе вещей. И оба навсегда запомнили те вечера, те мартовские вечера, в которые у них было достаточно оснований не щадить времени.
...Меж тем кончился март, начался апрель. Ветер над Северным морем изо всех сил возвещал весну. И в совершенно весеннем настроении возвращался домой доктор философии Копенгагенского университета Нильс Бор. Помеченная датой 5 апреля 1913 г. и снабженная благословением члена Королевского общества Резерфорда, первая его статья о квантовой конституции атома уже держала путь в редакцию «Philosophical Magazine». Знал ли он, что эта статья станет началом новой эпохи в теоретическом познании микромира? Наверняка!
«Краешком истины» назвал Эйнштейн то, что ему открылось в Природе. «Кусочком реальности» назвал Бор то, что Природа открыла ему.
Литература
1. Д. Данин. Нильс Бор//Серия ЖЗЛ. – М.: Молодая гвардия, 1978.
2. Д. Данин. Резерфорд//Серия ЖЗЛ. – М.: Молодая гвардия, 1966.
3. Д. Данин. Резерфорд и Бор. – Природа, 1966, № 4, 5.
4. Лоуренс У. Люди и атомы. – М.: Атомиздат, 1966.
5. Капица П. Мои воспоминания о Резерфорде. – Новый мир, 1966, № 8.
Похожие работы
... оно выявляется 8. Теперь, после краткого обзора развития греческой философии вплоть до формирования понятия атома, мы снова возвратимся к современной физике и спросим, как наше современное понимание атома и квантовая теория относятся к развитию античной натурфилософии. Исторически слово "атом" в физики и химии нового времени было связано с самого начала с ложным объектом. Это произошло в .XVII ...
... , а с другой - к выяснению структуры отдельных атомов и установлению связи между ними. Однако оставалось еще много явлений в этой области, объяснить которые теория Бора не могла. Движение электронов в атомах Бор представлял как простое механическое, однако оно является сложным и своеобразным. Это своеобразие было объяснено новой квантовой теорией. Отсюда и пошло: “Карпускулярно-вролновой дуализм ...
... положений равновесия колеблются электроны; суммарный заряд электронов равен положительному заряду шара, поэтому атом в целом нейтрален. Однако предположение о непрерывном распределении положительного заряда внутри атома не подтвердилось экспериментом. В развитии представлений о строении атома велико значение опытов английского физика Э. Резерфорда (1871-1937) по рассеянию альфа-частиц в веществе ...
... инерциальных системах отсчета. Пространственно-временной континуум – неразрывная связь пространства и времени и их зависимость от системы отсчета. Тема 11. Основные концепции химии 1. Химия как наука, ее предмет и проблемы Важнейшим разделом современного естествознания является химия. Она играет большую роль в решении наиболее актуальных и перспективных проблем современного общества. К ...
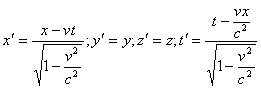
0 комментариев