Навигация
2. Метод отримання
Аспартам отримують синтезом з L – амінокислот:
аспарагінової кислоти
фенілаланіна.
Схема отримання аспартаму:
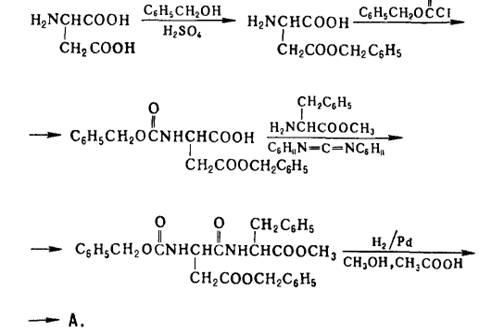
Домішки: дикетопіперазин (продукт розпаду).
Кольорові реакції
Устаткування, прилади й реактиви: водяна баня, спиртівка, 10% розчин NaOH, 1% розчин CuSO4, 0,2% розчин нінгідрину, концентрована азотна кислота, 0,5% розчин аспартама.
Біуретова реакція. У лужному середовищі білки, а також продукти їхнього гідролізу – поліпептиди дають фіолетове або червоно-фіолетове забарвлення із солями міді. Реакція обумовлена наявністю пептидних зв'язків (-NHCO-). Позитивна біуретова реакція проявляється в з'єднаннях, що містять не менш двох пептидних груп. Інтенсивність забарвлення залежить від довжини пептиду і варіює від синьо-фіолетового до червоно-фіолетового й червоного.
Біуретову реакцію дають також аспарагін (амід аспарагінової кислоти) і амінокислоти гістидин, треонін і серін.
Свою назву реакція одержала від біурета – з'єднання, що утворюється при нагріванні сечовини. Ця реакція супроводжується відщіпленням молекули аміаку.
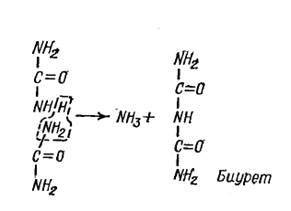
Комплексної мідно-натрієвої солі пептидів і білків приписують наступну будову:
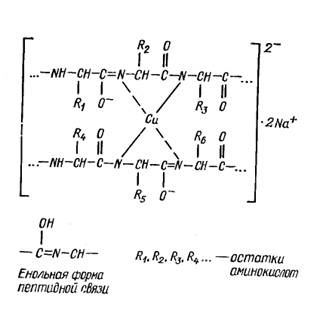
аспартам підсолоджувач сполука хімічний
Техніка виконання роботи: до 1 молярного розчину аспартама додають 1 молярний 10% розчину їдкого натрію й 2 краплі 1% розчину сірчанокислої міді. У присутності білків і пептидів (починаючи із трипептидів) з'являється рожево-фіолетове забарвлення. Реакція заснована на утворенні хелатного з'єднання іонів міді (+2) із двома пептидними зв'язками.
Нінгідринова реакція. Нінгідринова реакція обумовлена наявністю амінокислот, що мають аміногрупи в б-положенні. Білки, поліпептиди і амінокислоти утворюють із нінгідрином з'єднання синього або синьо-фіолетового кольорів (при нагріванні). Нінгідринова реакція є однієї з найбільш чутливих для виявлення б-аміногруп.

Сутність реакції полягає в тім, що б-амінокислоти і пептиди, реагуючи з нінгідрином, піддаються окисному дезамінування і декарбоксілюванню:
Відновлений нінгідрин взаємодіє з аміаком і другою молекулою нінгідрину, утворюють зафарбоване з'єднання (пурпурний Руеманна).
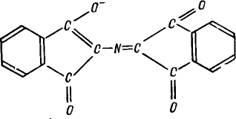
Техніка виконання роботи: до 5–10 крапель розчину аспартама додають 6–10 краплі 0,2% розчину нінгідрину. Нагрівають до кипіння на водяній лазні. З'являється фіолетово-синє забарвлення за рахунок утворення продукту конденсації нінгідрину з амінокислотою.
Ксантопротеїнова реакція. Характерна для деяких ароматичних амінокислот. При нагріванні білків і поліпептидів з концентрованою азотною кислотою утвориться нітросполука жовтого кольору.
Реакція протікає у дві стадії. Протягом першої амінокислота, взаємодіючи з концентрованою азотною кислотою, піддається нітруванню. При цьому утвориться динітросполука (жовтого кольору).
В другій стадії продукти нітрування реагують із їдким натром або гідроксидом амонію з утворенням натрієвої або амонійної солі, що має жовто-помаранчеве забарвлення.
Ксантопротеїнову реакцію, крім білків, пептидів і циклічних амінокислот, дають також багато простих ароматичних з'єднань (бензол, фенол і ін.).
Техніка виконання роботи: до 0,5 молярного розчину аспартаму додають 5–6 краплі концентрованої азотної кислоти. Обережно нагрівають. При наявності в розчині циклічних амінокислот або білків, у яких присутні ці амінокислоти, з'являється жовте забарвлення за рахунок нітрування бензольного кільця.
Після охолодження в пробірку обережно (по стінці) доливають надлишок концентрованого розчину аміаку або їдкого натру – рідина приймає помаранчевий або жовтий колір.
3. Кількісне визначення
1. Хроматографічний метод.
Метод заснований на використанні високоефективної рідинної хроматографії (ВЕРХ). Метод є арбітражним.
Обладнання і реактиви: високоефективний рідкісний хроматограф з програматором лінійного виміру швидкості потоку, обладнаний спектрофотометричний детектор з довжиною хвилі 210 нм; колонки хроматографічні; установка для вакуумної фільтрації; мікрошприці хроматографічні; папір фільтрувальний; ваги лабораторні; рН-метр; мірні колби; градуювальні піпетки; скляний рідинний термометр; бідистильована вода; ацетонітрил; калій фосфорнокислий однозамішенний; бензоат натрію; аспартам; ортофосфорна кислота.
Підготовка до випробування:
а). Приготування градуювального розчину аспартаму (550 мг/дм3).
Наважку аспартаму масою 137,5 мг переносять у мірну колбу місткістю 250 см3, до половини заповнену бідистильованою водою температурою 30–35 оС. Перемішують до повного розчинення, потім бідистилятом доводять до мітки.
б). Приготування градуювального розчину аспартаму (275 мг/дм3).
Відміряють піпеткою 2 см3 градуювального розчину аспартаму концентрацією 550 мг/дм3 переносять у мірну колбу місткістю 50 см3і доводять до мітки бідистильованою водою, добре перемішують.
в). Приготування градуювального розчину аспартаму (138 мг/дм3).
Відміряють піпеткою 25 см3 концентрацією 550 мг/дм3 переносять у мірну колбу місткістю 100 см3 і доводять до мітки бідистильованою водою, добре перемішують.
Приготування рухомої фази:
1,73 г. калія фосфорнокислого однозамішеного (КН2РО4) помішують у мірну колбу місткістю 1000 см3, розчиняють в бідистильованій воді, перемішують до повного розчинення. Отриманий розчин ортофосфорної кислоти (Н3РО4) доводять до мітки рН 3,2 850 см3 отриманого буферного розчину змішують із 150 см3 ацетонітрилу (С2Н3), попередньо відфільтрував їх через фільтрувальний папір діаметром пор 0,5 мкм.
Термін придатності рухливої фази – не більше 7 діб.
Умови хроматографічного аналізу:
Колонка з фазою С – 18,5 – 6 мкм, 0,15 * 4,6 мм.
Рухома фаза: 15% ацетонітрилу, 85% 0,0125 М розчину КН2РО4, доведеного фосфорною кислотою до рН 3,2.
Швидкість потоку: лінійний градіент від 1,2 см3/хв до 1,7 см3/хв за 8 хв.
Температура термостату – 35 оС.
Тиск на колонці при швидкості потоку – 1,2 см3/хв – 120 кг/см2 (тиск буде зростати по мірі експлуатації колонки).
Знаходження за поглинанням в УФ-області спектру при довжині хвилі 210 нм 0,02 од. адсорбції на всю шкалу.
Обробка результатів:
Масову долю аспартаму розраховують за формулою
![]()
де К – поправочний коефіцієнт, установлюваний за загально прийнятими правилами для методу «абсолютної градуїровки»;
S – площина піку досліджуваного компоненту, відповідна до певної масової концентрації компонента, мг;
V – об’єм аналізуємої проби, дм3;
Розрахунки проводять до другого десятичного знаку.
За кінцевий результат дослідження приймають середнє арифметичне результатів двох паралельних визначень.
Похожие работы
... і можливих перешкод при зміні дієти. Необхідним є пропагування серед населення сучасних науково обгрунтованих дієтологічних рекомендацій, що відповідають поняттям раціонального харчування, сприяють налагодженню здорового харчування і знижують ризик виникнення аліментарно зумовлених захворювань. Такий комплексний міжсекторальний підхід сприятиме ефективній діяльності з забезпечення раціонального ...
... єстрацію ГМО проводить Держкомветмедицини. Держреєстрація ГМО проводиться безплатно терміном на п`ять років шляхом внесення до Державного реєстру генетично модифікованих організмів – джерел кормів, кормових добавок і ветеринарних препаратів, які містять такі організми або одержані з їх використанням. Україна не зможе конкурувати на світовому ринку агропродукциі, якщо не вирощуватиме генно-модифі ...
0 комментариев