Навигация
Методы измерения диаметра молекул
1.2 Методы измерения диаметра молекул
В молекулярной физике главные «действующие лица» — это молекулы, невообразимо маленькие частицы, из которых состоят все на свете вещества. Ясно, что для изучения многих явлений важно знать, каковы они, молекулы. В частности, каковы их размеры.
Когда говорят о молекулах, их обычно считают маленькими упругими твердыми шариками. Следовательно, знать размер молекул, значит знать их радиус.
Несмотря на малость молекулярных размеров, физики сумели разработать множество способов их определения. В «Физике 7» рассказывается о двух из них. В одном используется свойство некоторых (очень немногих) жидкостей растекаться в виде пленки толщиной в одну молекулу. В другом размер частицы определяется с помощью сложного прибора — ионного проектора.
Строение молекул изучают различными экспериментальными методами. Электронография, нейтронография и рентгеновский структурный анализ позволяют получать непосредственную информацию о структуре молекул. Электронографии, метод, исследующий рассеяние электронов на пучке молекул в газовой фазе, позволяет рассчитать параметры геометрической конфигурации для изолированных сравнительно простых молекул. Нейтронография и рентгеновский структурный анализ ограничены анализом структуры молекул либо отдельных упорядоченных фрагментов в конденсированной фазе. Рентгенографические исследования кроме указанных сведений дают возможность получить количественные данные о пространственном распределении электронной плотности в молекулах.
Спектроскопические методы основаны на индивидуальности спектров химических соединений, которая обусловлена характерным для каждой молекулы набором состояний и отвечающих им энергетических уровней. Эти методы позволяют проводить качественный и количественный спектральный анализ веществ.
Спектры поглощения или испускания в микроволновой области спектра позволяют изучать переходы между вращательными состояниями, определять моменты инерции молекул, а на их основе - длины связей, валентные углы и другие геометрические параметры молекул. Инфракрасная спектроскопия исследует, как правило, переходы между колебательно-вращательными состояниями и широко используется для спектрально-аналитических целей, поскольку многие частоты колебаний определенных структурных фрагментов молекул являются характеристическими и слабо меняются при переходе от одной молекулы к другой. В то же время инфракрасная спектроскопия позволяет судить и о равновесной геометрической конфигурации. Спектры молекул в оптическом и ультрафиолетовом диапазонах частот связаны главным образом с переходами между электронными состояниями. Результатом их исследований являются данные об особенностях потенциальных поверхностей для различных состояний и значения молекулярных постоянных, определяющих эти потенциальные поверхности, также времена жизни молекул в возбужденных состояниях и вероятности переходов из одного состояния в другое.
О деталях электронного строения молекул уникальную информацию дают фото- и рентгеноэлектронные спектры, а также оже-спектры, позволяющие оценить тип симметрии молекулярных орбиталей и особенности распределения электронной плотности. Широкие возможности для изучения отдельных состояний молекул открыла лазерная спектроскопия (в различных диапазонах частот), отличающаяся исключительно высокой селективностью возбуждения. Импульсная лазерная спектроскопия позволяет анализировать строение короткоживущих молекул и их превращения в электромагнитное поле.
Разнообразную информацию о строении и свойствах молекул дает изучение их поведения во внешних электрических и магнитных полях.
Существует, однако, очень простой, хотя и не самый точный, способ вычисления радиусов молекул (или атомов) Он основан на том, что молекулы вещества, когда оно находится в твердом или жидком состоянии, можно считать плотно прилегающими друг к другу. В таком случае для грубой оценки можно считать, что объем V некоторой массы m вещества просто равен сумме объемов содержащихся в нем молекул. Тогда объем одной молекулы мы получим, разделив объем V на число молекул N.
Число молекул в теле массой m равно, как известно, ![]() , где М — молярная масса вещества NA — число Авогадро. Отсюда объем V0 одной молекулы определяется из равенства
, где М — молярная масса вещества NA — число Авогадро. Отсюда объем V0 одной молекулы определяется из равенства
![]() .
.
В это выражение входит отношение объема вещества к его массе. Обратное же отношение ![]() есть плотность вещества, так что
есть плотность вещества, так что
![]() .
.
Плотность практически любого вещества можно найти в доступных всем таблицах. Молярную массу легко определить, если известна химическая формула вещества.
Объем одной молекулы, если считать ее шариком, равен ![]() , где r - радиус шарика. Поэтому
, где r - радиус шарика. Поэтому
![]() .
.
откуда мы и получаем выражение для радиуса молекулы:
![~r = \sqrt[3] {\frac{3M}{4 \pi \rho N_A}} = \sqrt[3] {\frac{3}{4 \pi N_A}} \sqrt[3] {\frac{M}{\rho}}](/images/referats/a64/193320/7.png) .
.
Первый из этих двух корней — постоянная величина, равная ≈ 7,4 · 10-9 моль1/3, поэтому формула для r принимает вид
![~r \approx 7,4 \cdot 10^{-9} \sqrt[3] {\frac{M}{\rho}} (m)](/images/referats/a64/193320/8.png) .
.
Например, радиус молекулы воды, вычисленный по этой формуле, равен rВ ≈ 1,9 · 10-10 м.
Описанный способ определения радиусов молекул не может быть точным уже потому, что шарики нельзя уложить так, чтобы между ними не было промежутков, даже если они соприкасаются друг с другом. Кроме того, при такой «упаковке» молекул- шариков были бы невозможны молекулярные движения. Тем не менее вычисления размеров молекул по формуле, приведенной выше, дают результаты, почти совпадающие с результатами других методов, несравненно более точных.
Глава II. Определение диаметра молекулы
2.1 Метод Ленгмюра и Дево
Оборудование: микропипетка со шкалой, ванна размером 40х30 см, раствор жидкости в спирте с концентрацией 1:400 (олеиновая кислота и др.), тальк (ликоподий, пудра, порошок мела), линейка измерительная, лист бумаги.
Цель работы: определить приблизительно диаметр молекулы.
Исследуемая жидкость должна растворяться в спирте (эфире) и быть легче воды, не растворяясь в ней. При попадании капли раствора на поверхность воды спирт растворяется в воде, а исследуемая жидкость образует пятно площадью S и толщиной d (порядка диаметра молекул).
Если допустить, что молекула имеет форму шара, то объем одной молекулы равен: ![]() где d – молекулы.
где d – молекулы.
В лабораторной работе необходимо определить диаметр молекулы d. В микропипетку набираю 0,5 мл раствора и, расположив ее над сосудом, отсчитываю число капель n, содержащихся в этом объеме. Проделав опыт несколько раз, нахожу среднее значение числа капель в объеме 0,5 мл, а затем подсчитываю объем исследуемой жидкости в капле:
![]() м3,
м3,
где n – число капель в объеме 0,5 мл, 1:400 – концентрация раствора.
В ванну наливаю воду толщиной 1 – 2 см. Насыпаю тальк тонким слоем на лист бумаги, ударяя слегка пальцем по коробочке. Расположив лист бумаги выше и сбоку от ванны на расстоянии 10 – 20 см, тальк сдуваю с бумаги. На поверхность воды в ванне из пипетки капаю одну каплю раствора. Линейкой измеряю, средний диаметр образовавшегося пятна D и подсчитываю его площадь. Опыт повторяю 2- 3 раза, а затем подсчитываю диаметр молекул d.
При выполнении лабораторной работы следует иметь в виду, что иногда вода из городской сети имеет примеси, затрудняющие растекание капли.
В этом случае необходимо тщательно промыть ванну и использовать дистиллированную воду.
Спирт, имеющий примеси, может легко растекаться по поверхности воды, поэтому для раствора необходим чистый этиловый спирт.
Для приготовления раствора необходимой концентрации нужно отмерить 0,5 мл жидкости и добавить в нее 4,5 мл спирта, затем в 0,5 мл полученного раствора с концентрацией 1:10 добавить 4,5 мл спирта; в 0,5 мл полученного раствора с концентрацией 1:100 добавить 1,5 мл спирта. Получившийся раствор будет иметь концентрацию 1:400. Если применять раствор большей концентрации, то необходимо иметь ванну больших размеров.
Вывод
В результате работы я изучил литературу о строении молекул, о методах определения диаметра молекул. Используя метод Ленмюра и Дево, я провел исследования по определению приблизительного диаметра молекулы олеиновой кислоты и получил следующие результаты: d=9,3×10-10 м.
Данный результат не может быть точным, так как шарики нельзя уложить так, чтобы между ними не было промежутков, даже если они соприкасаются друг с другом. Кроме того, при такой «упаковке» молекул- шариков были бы невозможны молекулярные движения. Тем не менее вычисления размеров молекул по формуле, приведенной выше, дают результаты, почти совпадающие с результатами других методов, несравненно более точных.
Список литературы
молекула атом размер диаметр
1. Анциферов, Л. И. Самодельные приборы для физического практикума в средней школе [Текст] / Л. И. Анциферов.- М.: Просвещение, 1985.
2. Блудов, М. И. Беседы по физике [Текст] / М. И. Блудов. – М.: Просвещение, 1992. - 140 с.
3. Физика. Большой справочник для школьников и поступающих в вузы [Текст]/ - М.: Дрофа, 1999. - 688 с.
4. Физический энциклопедический словарь [Текст]/ - М.: Советская энциклопедия, 1983. - 928 с.
5. Энциклопедический словарь юного физика [Текст]/ - М.: Педагогика, 1984.
Похожие работы
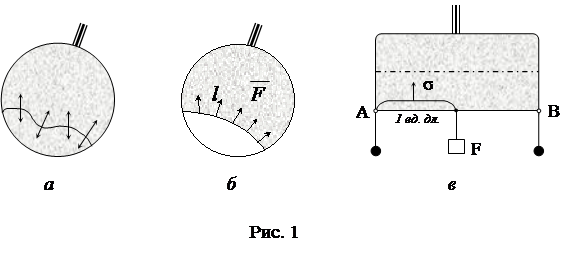
... , и начинаем отпускать его до момента образования плёнки. Отмечая новую тягу Р2, мы найдём для поверхностного натяжения s значение: . (8) §3. Определение коэффициента поверхностного натяжения методом компенсации давления Лапласа Молекулы жидкости взаимодействуют между собой силами притяжения и отталкивания, которые проявляются заметно в ...
... (47) Величина, обратная t, характеризует скорость прироста при данной температуре концентрации триплетных молекул акцептора энергии, q = 1/t , и называется константой скорости процесса [161]. Итак, прирост в результате отжига образца числа молекул, участвующих в излучении сенсибилизированной фосфоресценции происходит по экспоненциальному закону. Константа скорости этого ...
... к решению соответствующего интегрального уравнения, при этом могут быть использованы численные методы - аналитические зависимости в этом случае получить не удается. Еще сложнее описать процессы испарения и конденсации частиц, в среде, состоящей из нескольких летучих компонентов [23]. Предполагалось, что процесс стационарный, испаряющиеся компоненты химически инертны, пары представляют собой ...
... основе "Зеленой тетради". Шредингер был хорошо знаком с авторами этой работы по совместным семинарам физиков-теоретиков (и частично - радиационных генетиков) копенгагенской школы. Это и стало следующим "касанием" создателей великой идеи. Прежде всего Шредингер развил модель гена-молекулы (модель Дельбрюка, как он ее часто называл): "Предположим, что по своей структуре ген является гигантской ...






0 комментариев