Навигация
КДА и концентрирование белка методом обратного диализа с помощью полиэтиленгликоля (ПЭГ)
2.1.1. Выделение митопластов из митохондрий печени крыс
Для одного выделения обычно декапитировали 10 крыс, у которых извлекали печень.
Печень измельчали в специальном прессе, затем гомогенизировали в десятикратном объеме 300 мМ раствора сахарозы в 10 мМ Tris-HCl, рН 7.4 с использованием автоматического гомогенизатора при 240 об/мин.
Далее гомогенат центрифугировали на центрифуге К-70: 4 мин при 1200 об/мин (400g), затем 6 мин при 1500 об/мин (600g). В этих условиях осаждаются ядра и мембранные структуры.
Супернатант центрифугировали на РС-6 20 мин при 4800 об/мин (3500g). В этих условиях осаждается митохондриальная фракция. Осадок собирали и промывали в 300 мМ раствора сахарозы в 10 мМ Tris-HCl рН 7.4, затем ресуспендировали.
Повторное центрифугирование проводили на РС-6 20 мин. при 4800 об/мин (3500g). Осадок собирали, мерили его объем.
Доводили полученные митохондрии Tris-HCl (10 мМ, pH 7.4) до 500 мл.
Оставляли при перемешивании и температуре 4°С на 30 мин. В результате получались митопласты.
Митопласты центрифугировали при 5500 об/мин на РС-6 (4000g) в течение 20 мин.
Осадок объединяли. Измеряли его объем и концентрацию белка. Концентрацию белка измеряли спектрофотометрически (длина волны 750 нм) по методу Лоури (Лоури, 1965). Исходя из полученных данных, митопласты разводили бидистиллированной водой до концентрации 44 мг/мл.
2.1.2. Экстрагирование белков из митопластов
К полученной суспензии митопластов добавляли 9 объемов 66%-го этилового спирта. Экстракцию белков вели при перемешивании суспензии в течение 30 мин при 4°С. После экстракции суспензию центрифугировали при 5500 об/мин (4000g) в течение 15 мин.
2.1.3. Отделение водорастворимых белков от нерастворимых
Полученный супернатант диализовали против 5 мМ Tris-HCl pH 7.4 (c 2-меркаптоэтанолом – 0,0005%). Объем буфера составлял 2 л. Затем центрифугировали при 100000g 30 мин.
2.1.4. Ионообменная хроматография на DEAE-целлюлозе
Буфер «А» (Tris 50 mM, EDTA 0.5 mM pH 7.4; 125 мкл 2-меркаптоэтанола на 250 мл буфера после доведения рН)
Буфер «Б» (1М КСl в буфере «А»). Из него готовили ступенчатый градиент: 50, 100, 150, 200, 250, 300, 500 мМ КСl.
Взвешивалили DEAE-целлюлозу из расчета 1 г целлюлозы на 1 мл колонки. Целлюлозу промывали три раза деионизированной водой, затем буфером «А». Наносили на колонку. Промывали буфером «А» после нанесения.
Супернатант наносили на колонку c DEAE-целлюлозой (высота 2 см, объем 2 мл), предварительно уравновешенную буфером «А». После нанесения белков колонку промывали двойным объемом буфера «А» (Tris 50 мM, EDTA 0.5 мM pH 7.4).
Белки элюировали градиентом KCl: 50, 100, 150, 200, 250, 300, 500 мМ. Собирали по две фракции каждой концентрации соли. Каждая фракция по 2 мл. Полученные фракции проверяли на электрофорезе в ПААГ.
2.1.5. SDS-электрофорез в ПААГ
Белки разделяются по их молекулярным массам. Додецилсульфат натрия (SDS), связываясь с заряженными молекулами, компенсирует различия между зарядами белков.
Приготовление проб: в 30 мкл каждой фракции с DEAE-cell колонки добавляли по 15 мкл SLB.
Приготовление SLB:
1) SLB без меркаптоэтанола: 1.4 г SDS + 6 г глицерина + буфер, pH 6.8, без SDS - 7.5 мл, доводили деионизированной водой до 20 мл.
2) SLB для проб: 1 мл SLB без МЭ (1); 45 мкл МЭ; 45 мкл бромфеноловый синий .
Приготовление маркера:
10 мкл маркера (0.1 мг/мл) + 120 мкл SLB (1)
Приготовление кумасси: 600 мг кумасси голубого; 200 мл 96% этанола; 40 мл ледяной уксусной кислоты растворить в 200 мл воды.
Концентрированный буфер для форезной камеры: 7.6 г Tris-HCl + 36 г глицина доводили дистиллированной водой до 800 мл и рН 8.3-8.8. После этого в буфер добавляли 2.5 г додецилсульфата натрия.
Рабочий буфер для форезной камеры: Разводили концентрированный буфер в 5 раз.
Буфер для разделяющего геля: Tris-HCl 1.5 M (9.1 г на 50 мл воды доводили до рН 8.8), затем добавляли 200 мг SDS на 50 мл.
Буфер для концентрирующего геля: Tris-HCl 0.5 М (3 г на 50 мл). После доведения рН до 6.8 добавляли 200 мг SDS на 50 мл.
40% - бис-акриламид (60 мл): акриламид 23.34г.; бис-акриламид 0.64г.
Приготовление гелей: сведения представлены в таблице 2.
Таблица 2. Приготовление гелей для SDS-электрофореза в ПААГ.
| Вещество | Разделяющий 10 % (20 мл) | Концентрирующий 5% (5 мл) |
| 40% бис-акриламид | 5 мл | 0,72 мл |
| Буфер для геля | 5 мл | 1,6 мл |
| Вода | 9,3 мл | 3,95 мл |
| Персульфат аммония (1%) | 0,7 мл | 0,6 мл |
| TEMED* | 10 мкл | 15 мкл |
П р и м е ч а н и е: TEMED вносится непосредственно перед заливанием геля.
После полимеризации гелей пробы (в т.ч. метчик) кипятили на водяной бане в течение 5 минут и горячими наносили в карманчики геля. Маркер (рабочий) наносили в объеме 1/6 от объема проб.
Электрофорез проводили при силе тока 20 мА на одну пластинку. Когда пробы входили в разделяющий гель, силу тока увеличивали в 2 раза и оставляли до тех пор, пока краска не доходила до конца геля (1.5-2 часа).
Красили кумасси примерно 15 мин. Затем отмывали 7.5 % уксусной кислотой в течение ночи на шейкере. Если было необходимо, окрашивали серебрением (таблица 3).
Таблица 3. Окрашивание серебрением (Silver staining, Shevchenko at al., 1996)
| Реагент | Экспозиция |
| 50 % метанол + 10% уксусная кислота | 2*20 мин |
| 20% этанол | 10 мин |
| Вода | 10 мин |
| Тиосульфат натрия (0.2 г/л) | 1 мин |
| Вода | 2*20 сек |
| Нитрат серебра (2 г/л) | 30 мин |
| Вода | 20 сек |
| Проявитель: карбонат натрия (30 г/л); 37% формалин 1.4 мг/л; тиосульфат натрия 10 мг/л | Пока не проявится (около 20 мин) |
| 1% уксусная кислота | Минимум 20 мин |
Фракции, в которых при электрофорезе обнаружен белок с Mr
Похожие работы
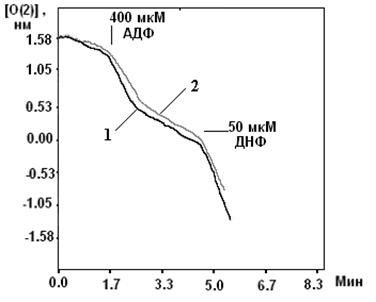
... м, в течение 10-15 мин. Группа низкоустойчивых (НУ) животных выдерживала эту высоту только в течение 1-1.5 мин. Глава 5. Результаты и обсуждения 5.1 Параметры функционирования митоКАТФ канала у крыс с различной резистентностью, а также у животных, адаптированных к гипоксии В этом разделе работы исследовались такие показатели, как дыхание МХ, скорость АТФ-зависимого К+ транспорта, ...
0 комментариев