Навигация
Оксифільноклітинний рак щитоподібної залози: клініки, діагностика, лікування, прогноз
ДЕРЖАВНА УСТАНОВА „ІНСТИТУТ ЕНДОКРИНОЛОГІЇ ТА ОБМІНУ РЕЧОВИН ім. В.П. КОМІСАРЕНКА АМН УКРАЇНИ”
КУЩАЄВА Євгенія Станіславівна
УДК 616.44- 006.6-07-08
ОКСИФІЛЬНОКЛІТИННИЙ РАК ЩИТОПОДІБНОЇ ЗАЛОЗИ: КЛІНІКА, ДІАГНОСТИКА, ЛІКУВАННЯ, ПРОГНОЗ
14.01.14 — ендокринологія
Автореферат
дисертації на здобуття наукового ступеня
кандидата медичних наук
КИЇВ - 2008
Дисертацією є рукопис
Робота виконана на базі Київської міської клінічної лікарні №16 та в Державній установі “Інститут ендокринології та обміну речовин ім. В.П. Комісаренка АМН України”
Науковий керівник
доктор медичних наук Коваленко Андрій Євгенович, Державна установа «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка АМН України», завідувач хірургічного відділення
Офіційні опоненти
доктор медичних наук, професор Олійник Валерій Анатолійович, Державна установа «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка АМН України», завідувач відділу загальної ендокринної патології
доктор медичних наук, професор Процик Володимир Семенович, Національний інститут раку МОЗ України, завідувач відділу пухлин голови, шиї та модифікуючих методів лікування
Захист відбудеться “21” жовтня 2008 р. о 13 годині на засіданні Спеціалізованої вченої ради Д.26.558.01 в ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка АМН України» (04114, м. Київ, вул. Вишгородська, 69).
З дисертацією можна ознайомитися в науковій бібліотеці Державної установи «Інститут ендокринології ім. В.П. Комісаренка АМН України» (04114, м. Київ, вул. Вишгородська, 69).
Автореферат розісланий “11” вересня 2008 р.
Учений секретар
Спеціалізованої вченої ради
доктор біологічних наук
Калинська Л.М.
ЗАГАЛЬНА ХАРАКТЕРИСТИКА РОБОТИ
Актуальність теми. Проблема раку щитоподібної залози (ЩЗ) для населення України є надзвичайно актуальною, що пов’язано з безпрецедентною техногенною катастрофою на Чорнобильській атомній станції, наслідки якої чітко просліджуються в теперішній час та залишаються тривожними у перспективі [Тронько Н.Д., Богданова Т.И. 1997, Богданова Т.И. 2000, Комісаренко І.В. та співав. 2001]. Робота присвячена вивченню оксифільноклітинного раку (ОР), що рідко зустрічається та є цікавим в екологічних умовах, які склались на Україні.
Оксифільноклітинний рак щитоподібної залози, рак із клітин Гюртле, онкоцитарний рак, В–клітинний рак — синоніми одного типу злоякісного новоутворення щитоподібної залози. Згідно останньої класифікації пухлин ЩЗ ВООЗ (1988) оксифільноклітинний рак щитоподібної залози характеризується як оксифільноклітинний варіант фолікулярного раку (ФР) та папілярного раку (ПР) ЩЗ. В більшості наукових робіт під назвою «оксифільноклітинний рак» або «Гюртлеклітинний рак» автори описують оксифільноклітинний варіант ФР ЩЗ [Brennan M. et al. 1991, Carcangiu M. et al. 1991, Azadian A. et al. 1995, Bhattacharyya N. 2003].
На сьогоднішній день багато авторів вважають цей вид пухлини окремою нозологічною одиницею, що відрізняється від ФР більшою агресивністю [Azadian A. et al. 1995, McDonald M. et al. 1996, Shaha A. et al. 1995]. Труднощі, що виникають при вирішенні проблеми ОР як варіанту ФР чи окремої патології, пов’язані насамперед з небагаточисельними групами хворих, що аналізуються. Крім того, в багатьох наукових працях, присвячених раку ЩЗ, оксифільноклітинний рак не виділяється в окрему групу [Brennan M. et al. 1991, Emerick G. et al. 1993, Mazzaferre E., Jhiang S. 1994, Grebe S. Hay I. 1995, Feldt–Rasmussen U. 1999, Gyory F. et al. 2001].
Інше нерозв’язане питання - це тактика хірургічного лікування пацієнтів з ОР ЩЗ. Пропонуються об’єми операції від гемітиреоїдектомії до тотального видалення ЩЗ з профілактичною центральною дисекцією шиї [Khafif A. et al. 1999, Perrier N. et al. 1999, Kebebew E., Clark O. 2000, Yutan E., Clark O. 2001, Besic N. et al. 2002, Stojadinovic A. et al. 2002].
Наступна проблема - це тактика післяопераційного ведення хворих з даною патологією, що пов’язана з низькою чутливістю оксифільноклітинних пухлин до дії радіойоду [Yu N. et al. 1999, Yutan E., Clark O. 2001]. Кількість хворих, у яких відмічено накопичення метастазами I131, не перевищує 10% [Clark O., Duh Q.–Y. 1997, Khafif A. et al. 1999, Clark O.H., Noguchi S. 2000, Kebebew E., Clark O. 2000, Yutan E., Clark O. 2001, Kushchayeva Y.S. et al. 2004]. Остання обставина вимагає пошуку нових ефективних методів діагностики метастазів ОР ЩЗ.
Альтернативними методами діагностики метастазів оксифільноклітинного раку ЩЗ пропонуються дослідження з 99mTc–MІБІ, 99mTc–тетрафосміном та 18–ФДГ–ПET [Wong C., Dworkin H. 1999, Plotkin M. et al. 2002].
Перераховані методики є відносно новими, та недостатньо вивченими при оксифільноклітинному раку ЩЗ. Тому вивчення можливостей доступних в Україні нових радіофармпрепаратів може підвищити якість діагностики у випадках оксифільноклітинного раку ЩЗ.
Всі дискутабельні питання стосовно оксифільноклітинного раку ЩЗ вимагають досконалого вивчення клінічних властивостей цієї пухлини та, виходячи з цього, визначення оптимальної тактики хірургічного лікування та створення алгоритму післяопераційного ведення хворих з даною патологією. Все вищеперераховане свідчить про актуальність та практичну значимість вивчення клінічного перебігу, ефективних підходів до лікування та післяопераційного нагляду хворих з оксифільноклітинними пухлинами щитоподібної залози.
Зв’язок роботи з науковими програмами, планами, темами.
Вивчення цінності радіoнуклідної сцинтіграфії для визначення метастазів оксифільноклітинного раку щитоподібної залози проводилось в рамках отриманого гранту Державного департаменту США (Рада міжнародних наукових досліджень та обмінів) (The program of the bureau of educational and cultural affairs of the US Department of State, funded by the freedom support act and administered by IREX).
Результати роботи є фрагментом теми «Вивчити віддалені результати хірургічного лікування хворих, які захворіли в післячорнобильський період на рак щитоподібної залози, з метою розробки диференційованих схем реабілітації» виконаної в хірургічному відділі Інституту ендокринології та обміну речовин ім.В.П.Комісаренка АМН України, Рег. № 0105U000729.
Мета роботи. Вивчити особливості клінічного перебігу оксифільноклітинного раку у порівнянні з неоксифільноклітинним фолікулярним та папілярним раком ЩЗ. Визначити основні прогностичні фактори захворювання та розробити раціональний лікувально-діагностичний протокол з метою підвищення ефективності лікування та спостереження даної групи пацієнтів.
Враховуючи вищесказане, завданнями роботи є:
1. Вивчити клінічну характеристику оксифільноклітинного раку щитоподібної залози за матеріалами Київської міської клінічної лікарні №16 та ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка АМН України».
2. Визначити тактику хірургічного лікування оксифільноклітинного раку щитоподібної залози.
3. Вивчити можливості радіонуклідної діагностики оксифільноклітинного раку щитоподібної залози.
4. Проаналізувати віддалені результати лікування оксифільноклітинного раку щитоподібної залози та фактори ризику, що впливають на прогноз захворювання.
5. Розробити алгоритм післяопераційного нагляду за хворими з оксифільноклітинним раком щитоподібної залози.
Об’єкт дослідження — злоякісні пухлини щитоподібної залози.
Предмет дослідження — оксифільноклітиний рак щитоподібної залози.
Методи дослідження — клінічні, ультразвукові, радіологічні, морфологічні.
Наукова новизна роботи. Вперше проведений детальній аналіз особливостей клінічного перебігу, методів діагностики та лікування хворих з оксифільноклітинним раком ЩЗ у порівнянні з іншими типами диференційованого раку ЩЗ. Отримані результати свідчать, що оксифільноклітинний рак ЩЗ відрізняється від ПР та ФР ЩЗ старшим середнім віком пацієнтів, високим рівнем локальної екстратиреоїдної інвазійності, раннім лімфогенним метастазуванням, резистентністю до I131-діагностики і терапії та більш частим метастазуванням, що потребує окремого підходу до лікування та спостереження за хворими з даною патологією.
Розроблено новий метод радіонуклідної діагностики метастазів та рецидивів йод-резистентних форм високодиференційованих карцином ЩЗ, який грунтується на застосуванні подвійної сцинтіграфії з 99mТc-пертехнетатом та 99mТc-МІБІ (патент № 9221). Розроблений протокол післеопераційного ведення хворих з ОР ЩЗ.
Практична значимість отриманих результатів. Результати даної роботи дозволили розробити практичні рекомендації, що стосуються тактики ведення хворих з оксифільноклітинним раком ЩЗ.
Розроблений та запатентований метод радіонуклідної діагностики рецидивів та метастазів оксифільноклітинного раку ЩЗ, що мають низьку тропність до традиційного методу діагностики ДРЩЗ (131I). Метод дозволяє діагностувати метастатичний процес без відміни тиреоїдних гормонів та на ранній стадії хвороби, що є запорукою своєчасного лікування.
Особистий внесок здобувача. Автором самостійно обґрунтовані актуальність та необхідність проведення дослідження, його мета та завдання. Проведений аналіз наукової літератури. Автор дисертації є основним розробником викладених у роботі положень, висновків та рекомендацій. Автором особисто виконаний патентний пошук, розроблена програма досліджень, проведений аналіз первинних даних архівного матеріалу хірургічного відділення КМКЛ №16, ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка АМН України», проводилося спостереження за хворими на рак щитоподібної залози. Здобувачем проводилася фотозйомка, розробка карти нагляду та електронних баз даних, оформлення роботи, зроблені висновки дослідження.
Апробація результатів дисертації. За результатами досліджень, що включені до дисертаційної роботи, були зроблені доповіді на: науковій конференції Інституту нейрохірургії АМН України (Київ, 2002); Міжнародному конгресі ендокринних хірургів (Уппсала, Швеція, 2004); 10 конгресі світової федерації Українських лікарських товариств (Чернівці, 2004); симпозіумі «Проблеми діагностики, лікування ендокринної патології та її ускладнень у осіб, які постраждали внаслідок аварії на Чорнобильській АЕС» (Київ, 2004); симпозіумі «Проблеми діагностики, лікування ендокринної патології та її ускладнень у осіб, які постраждали внаслідок аварії на Чорнобильській АЕС» (Київ, 2005); науково-практичній конференції з міжнародною участю "Актуальні проблеми ядерної медицини" (Чернігів, 2005); міжнародному симпозіумі „Сучасні технології у тиреоїдній хірургії” (Галле, Німеччина, 2006); міжнародному конгресі Європейського Товариства ендокринних хірургів (Краків, Польща, 2006).
Публікації. За темою дисертації опубліковано 11 наукових робіт, з яких 8 статей у фахових виданнях, рекомендованих ВАК України, 2 тез доповідей та 1 патент.
Структура та обсяг роботи. Повний обсяг дисертації становить 176 сторінок машинопису. Дисертація складається із вступу, 7 розділів, аналізу та узагальнення результатів дослідження, висновків, практичних рекомендацій, списку використаних джерел. Робота ілюстрована 7 малюнками, 31 фотографією та 44 таблицями, які займають 40 сторінок. Список літератури містить 210 джерел, з яких 41 вітчизняних та 169 англомовних.
ОСНОВНИЙ ЗМІСТ РОБОТИ
Загальна характеристика хворих та методи їх обстеження. В дисертаційній роботі представлені результати хірургічного лікування та післяопераційного нагляду 47 хворих з оксифільноклітинним раком (ОР) у порівнянні зі 178 випадками папілярного раку (ПР) та 139 – фолікулярного раку (ФР) ЩЗ за період 1995-2004 рр.
Загалом в досліджувану групу (364 випадки) ввійшли 45 чоловіків та 319 жінок із співвідношенням 1 : 7,1. Відсоток жінок серед хворих з ОР, ПР та ФР ЩЗ склав 91%, 84,2% та 85% відповідно. Середній вік хворих в досліджуваній групі серед хворих з ОР ЩЗ склав 50.8 + 2,1 років, з ПР ЩЗ - 44.9 + 0,87 років та з ФР ЩЗ - 41.8 + 1,03 років.
Доопераційне обстеження включало збір анамнезу захворювання, фізикальний огляд по органам та системам, пальпацію ЩЗ та зон реґіонарного метастазування. Всім хворим виконувались загальні аналізи крові, сечі, коагулограмма крові, біохімічний аналіз крові, визначався рівень цукру крові, проводилась рентгенографія органів грудної клітини, огляд оториноларингологом, УЗД ЩЗ та лімфатичних колекторів. ТАПБ виконувалась під контролем УЗД. Всі пухлини були досліджені з допомогою інтраопераційної морфологічної діагностики (мікроскопічні зрізи замороженої тканини). Остаточний діагноз виставлявся за результатами заключного патоморфологічного дослідження.
До оксифільноклітинних були віднесені пухлини, що складалися виключно або переважно (більше, ніж на 75%) з онкоцитів з очевидними ознаками інвазії в капсулу та/або кровоносні судини [Rossi R., Caddy B. 1991, Rosai J. 1996].
У післяопераційний період для моніторингу захворювання застосовували УЗД, КТ, МРТ, сцинтиграфія з ¹³¹I, ТАПБ підозрілої тканини, визначали рівень тиреоглобуліну (ТГ) та антитіл до ТГ. У випадках ¹³¹I–негативної сцинтиграфії при наявності інших ознак пролонгації процесу (високий рівень ТГ, наявність патологічної тканини, виявленої з допомогою УЗД, КТ, МРТ) виконували подвійну сцинтиграфію, що включала застосування 99mTc–пертехнетату та 99mTc–МІБІ (рання і пізня фази). Першим етапом дослідження виконували сцинтиграфію з 99мТс–пертехнетатом, що вводився внутрішньовенно активністю 37–75 Мбк з дослідженням через 30 хв. після ін’єкції при матриці збору 128х128. Другим етапом проводили сцинтиграфію з 99mТс–МІБІ, що складалася з двох повторних досліджень: перше виконували через 5–10 хв. після в/в введення 555–740 Мбк 99mТс–МІБІ (рання фаза), друге – через 120 хв (пізня фаза) з ідентичними першому етапу параметрами збору інформації. Принцип дослідження полягає в тому, що 99mТс–МІБІ є туморотропним препаратом, який здатний нагромаджуватися як пухлиною так і залишковою тканиною ЩЗ. Тому для диференціальної діагностики залишкової тканини від пухлинної застосували сцинтиграфію з 99мТс-пертехнетатом, що накопичується тільки залишковою тканиною ЩЗ. Згодом проводилася візуальна оцінка всіх отриманих зображень із урахуванням особливостей розподілу обох радіо фармпрепаратів (патент № 9221).
Для оцінки результатів дослідження використовували порівняльний метод аналізу та визначення значимості різниці між показниками груп. При цьому використовували такі загальноприйняті методи, як метод хі–квадрат (χ2), дисперсійний метод (F) та метод Ст’юдента (t).
Результати досліджень та їх обговорення. За даними госпітального реєстру КМКЛ №16 частота ОР ЩЗ за період 1995-2004 рр. склала 2,05% від всієї кількості раку ЩЗ без тенденції до зростання за 2 останніх п’ятиріччя (2,2% за 1995–1999 та 1,9% за 2000–2004 рр.).
При порівнянні групи хворих з ОР з групами ПР та ФР ЩЗ за статтю виявлена вірогідна різниця з групою ПР ЩЗ (таблиця 1). Середній вік хворих з ОР ЩЗ у порівнянні з іншими групами виявився достовірно більшим тільки серед хворих жіночої статі (р<0,05).
Таблиця 1.
Характеристика хворих з раком ЩЗ за статтю та віком.
| Папілярний рак 178 хворих | Фолікулярний рак 139 хворих | Оксифільно- клітинний рак 47 хворих | |
| Ж/Ч | 162/15 91/9% | 117/ 22 84.2/15.8% | 40/7* 85/15% |
| Відношення Ч : Ж | 1 : 10.1 | 1 : 5.3 | 1 : 5.7* |
| Середній вік: жінки | 46,2 + 0,97 (12-75) | 42,4 + 1,12 (10-74) | 51,6 + 2,01*/** (23-78) |
| Середній вік: чоловіки | 43,7 + 2,88 (27-65) | 39,0 + 3,01 (11-65) | 46,0 + 7,26 (14-62) |
Примітки: * - група ОР порівняно з групою ПР ЩЗ, р<0,05
**- група ОР порівняно з групою ФР ЩЗ, р<0,05
Відносно розмірів первинної пухлини знайдено достовірну різницю між групою ОР (4,1+0,47см) та групою ПР (1,22+0,21см) (р<0,05), але не з групою ФР ЩЗ (3,9+0,16см) (р>0,05). Серед групи хворих з ПР у 51,7% випадків розмір пухлини був до 1см (пухлини до 1 см, що були віднесені до Т1 та Т4 стадії). Такі незначні розміри раку досить рідко зустрічаються серед хворих з ОР та ФР ЩЗ, не перевищуючи 5% за літературними даними [Chow S., et al. 2002]. Серед хворих з ОР та ФР тільки у 4,3% та 0,8% верифіковані пухлини до 1см у порівнянні з ПР ЩЗ (р<0,05).
Згідно TNM класифікації, Т1 стадія була діагностована тільки у 4,3% хворих з ОР та у 0,8% - з ФР ЩЗ, у порівнянні з ПР ЩЗ (46%) (р<0,01) (таблиця 2). Т2-3 стадії превалювали серед хворих з ОР та ФР (р<0,01).
Таблиця 2.
Порівняння досліджуваних груп за характеристиками первинної пухлини.
| Ознаки | Папілярний рак | Фолікулярний рак | Оксифільноклітин-ний рак |
| Середній розмір пухлини, см | 1,22 + 0,21 | 3,9 + 0,16 | 4,1 + 0,47** |
| Т1 | 46,0% | 0,8% | 4,3%** |
| Т2 | 30,0% | 63,2% | 51,3%** |
| Т3 | - | 32,2% | 31,4% |
| Т4 | 24,0% | 3,8% | 13,0%*/** |
| Tб | 30,3% | 1,4% | 4,3%** |
| N1 | 15,7% | 0,7% | 10,6%* |
| M1 | 0,6% | - | 4,3%* |
Примітки: * - група ОР порівняно з групою ПР ЩЗ, р<0,05
**- група ОР порівняно з групою ФР ЩЗ, р<0,05
Для ОР ЩЗ, як і для ПР ЩЗ, характерне екстратиреоїдне розповсюдження процесу в протилежність ФР, який рідко виходить за межі органу. Серед хворих на ОР ЩЗ екстратиреоїдне розповсюдження діагностовано в 13% випадків, що вірогідно більше у порівнянні з ФР (3,8%) та менше, ніж при ПР ЩЗ (24%) (р<0,01). За даними літератури екстратиреоїдне розповсюдження у випадках ОР ЩЗ, що є несприятливою прогностичною ознакою, зустрічається з більшою частотою (27,5 – 39%) [McDonald M. et al. 1996, Evans H., Vassilopoulou–Sellin R. 1998, Stojadinovic A. et al. 2002, Lopez–Penabad L. et al. 2003], ніж у досліджуваній нами групі.
Інтратиреоїдна дисемінація зустрічалась у 4,3% випадків при ОР та у 1,4% випадків при ФР, що вірогідно менше, ніж при ПР ЩЗ (30,3%) (р<0,01). Інтратиреоїдне розповсюдження є притаманною ознакою для ПР [Kebebew E., Clark O. 2000].
За даними дослідження метастази в лімфовузли виявлені в 10,6% випадків ОР ЩЗ, що не має достовірної різниці з частотою ураження реґіонарних лімфовузлів при ПР (15,7%), але вірогідно більше при порівнянні з ФР (0,8%) (р<0,01). Як відомо, метастазування ОР ЩЗ в реґіонарні лімфатичні вузли на момент діагностики злоякісного процесу зустрічається в 10–25% випадків, що теж є несприятливою ознакою для прогнозу [Rosai J. et al. 1992, Clark O., Duh Q.–Y. 1997, Sanders L., Silverman M. 1998, Stojadinovic A. et al. 2001, Lopez–Penabad L. et al. 2003]. Подібна частота залучення лімфовузлів описана при ПР ЩЗ (30–40%) [Kebebew E., Clark O. 2000, Hay I.D. et al. 2002]. При ФР метастатичне ураження лімфатичних вузлів має місце вкрай рідко (<5%) [Yutan E., Clark O. 2001].
За результатами власного дослідження, ОР ЩЗ за здатністю розповсюджуватись лімфогенним шляхом подібний до ПР ЩЗ та відрізняється від ФР ЩЗ, що не протирічить світовими дослідженнями [Rosai J. et al. 1992, Kebebew E., Clark O. 2000].
Віддалені метастази діагностовано у 4,3% хворих з ОР ЩЗ, що є найбільшим показником серед досліджуваних груп хворих (р<0.05). За літературними даними, ОР та ФР мають схожу частоту віддалених метастазів на момент первинної діагностики (9–29%) [Clark O., Duh Q.–Y. 1997, Evans H., Vassilopoulou–Sellin R. 1998, Goldstein N. et al. 2001, Stojadinovic A. et al. 2001, Besic N. et al. 2002]. Найменша частота віддалених метастазів спостерігається серед хворих з ПР ЩЗ (2-14%) [Kebebew E., Clark O. 2000, Shaha A. et al. 2001, Hay I.D. et al. 2002].
Отже, підкреслюючи агресивні властивості ОР, можна відмітити, що ОР ЩЗ за своїми метастатичними властивостями знаходиться між ПР та ФР ЩЗ, маючи схильність метастазувати як лімфогенним, так і гематогенним шляхом. Деякі автори прирівнюють ОР ЩЗ по ступеню злоякісності до інсулярного або медулярного раку ЩЖ [Carcangiu M. et al. 1991].
Серед доопераційних методів діагностики раку ЩЗ на доопераційному етапі ТАПБ є найбільш ефективним та значно підвищує інформативність УЗД. Висока ефективність ТАПБ при ПР ЩЗ є доведеною, що підтверджено і дослідженнями нашої клініки [Аветісян К.Л. та співавт. 2002]. Але у випадках ОР та ФР ЩЗ за власними даними ні в одному випадку доопераційний діагноз „карцинома” не був встановлений. У порівнянні з ТАПБ-діагностикою ПР ЩЗ, цитологічні ознаки ФР чи ОР ЩЗ дають менше можливостей щодо чіткого визначення характеру процесу, залишаючись „сірою зоною в діагностиці” [Clark O., Duh Q.–Y. 1997, Kroll TG. et al. 2000, Koike E et al. 2001]. У цих випадках можлива лише верифікація клітинного складу пухлини без розмежування доброякісності і злоякісності процесу [Nguyen G. et al. 1999] та диференціація пухлин від гіперпластичних вузлів, що містять оксифільні клітини [McIvor N. et al. 1993, Clark O., Duh Q.–Y. 1997]. Оскільки диференційна діагностика онкоцитарних і фолікулярних аденом та карцином лежить у площині гістологічного визначення інвазійних властивостей пухлини в капсулу чи судини, ТАПБ у цих випадках має обмежені можливості [Nguyen G. et al. 1999], тому всі випадки „ онкоцитарних чи фолікулярних неоплазій” вважаються потенційно злоякісними [Аветісян К.Л. та співавт. 2002].
Досліджуючи морфологічні характеристики раку ЩЗ, нами відмічена подібність ОР та ФР ЩЗ у схильності до інвазії в капсулу пухлини (91,5% для ОР та 89,9% для ФР ЩЗ), що дуже рідко зустрічається у випадках ПР ЩЗ (5,6%) (р<0,01). Інвазія в кровоносні судини більше притаманна ОР та ФР ЩЗ (78,7% та 79,1%) і доволі рідко спостерігається при ПР ЩЗ (12,4%) (р<0,01). Капсулярна та васкулярна інвазія у випадках ОР та ФР є основними діагностичними критеріями цих типів раку ЩЗ. Питання прогностичної значимості капсулярної та васкулярної інвазії залишається відкритим [Rosai J. et al. 1992, Goldstein N. et al. 2001,], але вважають, що наявність будь-якої інвазії окреслює групу пухлин, що потенційно можуть метастазувати [Carcangiu M. et al. 1991]. Значимість васкулярної інвазії для ПР ЩЗ описана як прогностично неблагоприємна для виникнення віддалених метастазів [Baloch Z., LiVolsi V. 2000, Gardner R. et al. 2000, Mai K.et al. 2002]. Інвазія в лімфатичні судини ЩЗ мала місце у 4.3% хворих з ОР та 2.2% з ФР ЩЗ, що вірогідно менше у порівнянні з ПР ЩЗ (58,4%) (р<0.01). Просліджується достовірна різниця у частоті інвазії в паренхіму серед досліджуваних груп, що мала місце у 30% випадків ОР, 14,4% - ФР та 90% - ПР ЩЗ (р<0.01). Порівнюючи інвазійні властивості ФР та ОР ЩЗ, за такими ознаками як капсулярна інвазія, інвазія в лімфатичні та кровоносні судини ФР та ОР ЩЗ є схожими. Аналізуючи інвазію в паренхіму та розповсюдження за межі капсули знайдено достовірно більшу частоту даних ознак серед хворих з ОР (30% та 12,8%) у порівнянні з ФР ЩЗ (14,4% та 3,6%) (р<0.05). Інвазія в оточуючу паренхіму та за межі ЩЗ найбільш притаманна ПР ЩЗ (90% та 24.2%), що дозволяє зробити висновок про схожість за деякими морфологічними ознаками ПР та ОР ЩЗ. Отже, вивчаючи інвазійні властивості ОР у порівнянні з ПР та ФР ЩЗ, можна відмітити, що для ОР ЩЗ притаманні характеристики властиві як ПР, так і ФР ЩЗ, що відображається на клінічних проявах хвороби.
У відповідності зі ступенем інвазійності ОР та ФР ЩЗ представлені широкоінвазивним (ШІ) та мінімальноінвазивним (МІ) варіантами. При розподілі пухлин на МІ та ШІ варіанти, були використані рекомендації ВОЗ [Hedinger, Сhr. 1988]. Серед досліджуваної групи хворих з ОР ЩЗ в 31,9% випадків пухлину була представлена ШІ варіантом, тоді як при ФР тільки 13,7% - мали ШІ варіант (р<0.01).
Пухлини розміром понад 4см зустрічались в 31,1% випадків ОР, що вірогідно менше у порівнянні з ФР ЩЗ (66.2%) (р<0.01).
Таблиця 3.
Залежність ступеню інвазійності від розміру пухлини.
| Фолікулярний рак (n=133) | Оксифільноклітинний рак (n=45) | р | |
| Пухлина < 4 см | n=45* | n=31* | |
| МІ | 77,8% (35) | 77,4% (24) | р > 0.05 |
| ШІ | 22,2% (10) | 22,6% (7) | р > 0.05 |
| Пухлина > 4 см | n=88** | n=14** | |
| МІ | 89,8% (79) | 57,1% (8) | р < 0.05 |
| ШІ | 10,2% (9) | 42,9% (6) | р < 0.05 |
Примітки: * - кількість пухлин розміром < 4 см в обох групах
** - кількість пухлин > 4 см в обох групах
Серед оксифільноклітинних пухлин більше 4см майже кожна друга пухлина була представлена ШІ варіантом (42,9%), тоді як у випадках ФР тільки 10,2% пухлин такого розміру мали ШІ варіант (р<0.05) (таблиця 3). Отже, у випадках ОР ЩЗ розмір пухлини достовірно корелює зі ступенем інвазійності: при збільшенні розміру раку (>4см) різко зростає кількість пухлин з ШІ варіантом.
Щодо тактики хірургічного лікування, тотальне видалення ЩЗ, за власними даними, було виконане у 72,4% хворих з ОР, у 77,5% - з ПР ЩЗ та у 63,3% - з ФР ЩЗ. Гемітиреоїдектомія з резекцією протилежної долі мала місце у 8.5% хворих з ОР, 11,2% хворих з ПР та у 16,5% - з ФР ЩЗ. Гемітиреоїдектомія з істмектомією, на думку багатьох авторів, є достатнім об’ємом для пухлин з МІ ОР чи ФР ЩЗ [Sanders L., Silverman M. 1998, Stojadinovic A. et al. 2002]. Крім того, „гемітиреоїдектомія” – це мінімальний об’єм операції, що повинен виконуватися у випадках точно невстановленого інтраопераційного діагнозу („фолікулярна неоплазія”), який доповнюється остаточною тиреоїдектомію у випадку морфологічного підтвердження діагнозу карциноми. Тотальне видалення ЩЗ під час першого оперативного втручання серед хворих з ОР досліджуваної групи виконане у 24 хворих, серед яких 15 – мали ШІ варіант (5 – з ураженням реґіонарних лімфовузлів та 2 – з віддаленими метастазами), 4 хворих мали супутній багатовузловий зоб з ураженням обох долей, в 2 випадках діагностовані «фолікулярні неолазіі» в протилежних долях (фолікулярна та оксифільноклітинна аденоми за даними заключного морфологічного дослідження) та в 3 випадках – супутній папілярний рак ЩЗ. В 10 випадках виконувалось повторне хірургічне втручання – остаточна тиреоїдектомія. Згідно літературних даних, більшість авторів наполягає на тотальному видаленні ЩЖ при ОР [Khafif A. et al. 1999, Kebebew E., Clark O. 2000, Yutan E., Clark O. 2001, Besic N. et al. 2002].
За власними даними серед хворих з ОР ЩЗ відмічено, що діагностика та лікування з I131 у післяопераційному періоді мали вкрай низьку ефективність. Метастатичний процес у післяопераційному періоді був діагностований в 11,4% хворих (5 випадків) з ОР ЩЗ і в жодному випадку I131-лікування не було ефективним. Незначне накопичення I131 відмічене в одному випадку без лікувального ефекту. В єдиному випадку реґіонарного метастазування ефективним методом лікування виявилось оперативне втручання. В інших випадках зафіксовано персистенцію хвороби (2 хворих) або смерть від генералізації процесу (2 хворих). Загалом період нагляду за хворими склав в середньому 3,5 років (1-9 років). Загальний час спостереження за хворими з метастазами був 1.5 років (1–4 роки). Персистенція захворювання мала місце в 3 випадках. В 2 випадках метастази виникли через 1 та 2 роки після операції.
Принциповим питанням у випадках ОР ЩЗ є тактика післяопераційного ведення хворих, що пов’язане з низькою чутливістю оксифільноклітинних пухлин до I131 (близько 10%) [Yutan E., Clark O. 2001], що є однією з головних причин низької ефективності лікування метастатичного процесу [Sanders L., Silverman M. 1998, Stojadinovic A. et al. 2002]. На сьогоднішній день у випадках I131–негативних метастазів запропоноване застосування сцинтіграфії з 131I, 201Tl, 99mTc–тетрофосміну, 99mTc–MІБІ, 18ФДГ, чутливість яких, за даними літератури, становить 42–62%, 45–94%, 86–89%, 50–88%, 50–78% відповідно [Wong C., Dworkin H. 1999, Rubello D. et al. 2000].
Для діагностики I131–негативних метастазів ДРЩЗ нами був розроблений метод, що включає такі загальноприйняті методи, як визначення рівню тиреоглобуліну, виконання ультразвукового дослідження та додатково застосування подвійної сцинтиграфії з 99mТс-пертехнетатомі 99mТс-МІБІ (патент № 9221). До істотних переваг 99mTc–МІБІ відноситься короткий період напіврозпаду (6 год.), незначна доза опромінення (поглинута доза в ЩЗ 0,03-0,06 МЗв), внаслідок цього, можливість введення більш високої активності препарату (555–740 Мбк), що поліпшує якість зображення; відсутність залежності між рівнем накопичення 99mTc–МІБІ в патологічній тканині, функціональним станом ЩЗ і прийомом препаратів, що впливають на функцію ЩЗ. При дослідженні в післяопераційному періоді застосування 99mTc–МІБІ не потребує відміни тиреоїдних препаратів. Феномен "приглушення" («stunning» phenomenon – зменшення накопичення залишковою тканиною або метастазами раку ЩЗ лікувальної дози 131I після застосування діагностичної дози 131I) при застосуванні 99mTc–МІБІ відсутній. Крім того, застосування 99mTc–МІБІ можливе при наявності тканини ЩЗ, коли неможливо застосувати діагностику з 131I.
Результатом даної розробки є доповнення протоколу новим діагностичним методом – подвійною сцинтиграфію з 99mТс–пертехнетатом та 99mТс–МІБІ, що покращує виявлення хворих з метастазами та дозволяє провести своєчасне лікування. Серед досліджуваних хворих з метастазами ОР ЩЗ, яким виконувалась сцинтиграфія з 131I, у всіх випадках (4/4) накопичення було відсутнім, але всі ці пухлини були 99mТс–МІБІ-позитивними. В таких випадках своєчасна діагностика з 99mТс–МІБІ та хірургічне лікування є актуальним для покращення прогнозу хворих. За власними даними діагностична ефективність 99mTc–МІБІ у випадках 131I-негативних метастазів склала 77%. Але необхідно враховувати, що 99mTc–МІБІ має тільки діагностичну цінність.
За даними власного дослідження та аналізу результатів інших робіт застосування 99mТс-МІБІ може бути рекомендоване: 1) при наявності підвищеного рівня тиреоглобуліну (ТГ) або у випадках нормального рівня ТГ чи такого, що не діагностується, та високого рівня антитіл до ТГ у поєднанні з відсутністю накопичення 131I; 2) при неможливості відміни тиреоїдних гормонів у зв'язку з тяжкою соматичною патологією хворого; 3) після виконаної органозберігаючої операції та неможливості використання 131I; 4) при наявності пухлин, низькочутливих до дії 131I (оксифільноклітинний рак, інсулярний рак ЩЗ). Але позитивний результат дослідження з 99mТс-МІБІ без інших ознак пролонгації хвороби (високий рівень ТГ, наявність патологічної тканини, виявленної з допомогою КТ, МРТ, УЗД) не може бути основою для діагнозу метастатичного процесу раку ЩЗ.
За період спостереження від 1 до 9 років у післяопераційному періоді 88,6% хворих з ОР, 98,8% - з ПР та 94,8% - з ФР ЩЗ не мали ознак хвороби на момент останнього огляду. З персистенцією раку спостерігаються 4,5% пацієнтів з ОР, 0,6% - з ПР та 0,7% - з ФР ЩЗ. При порівнянні ПР, ФР та ОР ЩЗ найвища смертність була виявилена у випадках ОР ЩЗ (4.5%). В обох випадках смерть настала внаслідок розповсюдження метастазів з залученням легенів, кісток та межистінних лімфовузлів. Від інших причин, непов’язаних з раком ЩЗ, серед хворих, що перебували під спостереженням, вмерли 2,3% пацієнтів з ОР та 3,7% - з ФР ЩЗ, серед хворих з ПР випадків смерті не було.
Крім того, за період спостереження виявлено, що серед хворих з ОР частота супутніх злоякісних пухлин нетиреоїдного походження була найбільшою — 13.6% (6 випадків), у порівнянні з 0.8% (1 випадок) – при ФР та 4.5% (8 випадків) – при ПР ЩЗ (р<0.01). Супутні нетиреоїдні злоякісні пухлини у хворих на ОР ЩЗ були представлені раком шлунку (2 випадки), базальноклітинним раком шкіри (2 випадки) та раком нирки (2 випадки).
При вивченні факторів ризику у випадках ОР ЩЗ встановлено, що перебіг хвороби серед старшої вікової групи виявився більш агресивним: ні в одному випадку до 45 років метастази не розвинулись, в противагу старшій віковій групі (>45 років), коли метастази виявлені в 15.6%. Розвиток метастазів виявився фатальним для 6,3% хворих (2 випадки). Негативний вплив віку на прогноз захворювання описувався іншими авторами [Khafif A. et al. 1999, Bhattacharyya N. 2003]. Вплив статі на прогноз захворювання залишається відкритим [Khafif A. et al. 1999, Bhattacharyya N. 2003]. Серед досліджуваної групи хворих з ОР тільки серед пацієнтів жіночої статі виявлено пролонгацію хвороби (13.5%, 5/37) з летальністю 5.4% (2/37). Розмір пухлини не мав суттєвого значення для метастазування ОР ЩЗ: метастази розвинулись у 15.4% випадків при первинній пухлині > 4 см та в 10% – < 4 см. В літературі описаний несприятливий прогноз при наявності пухлин більше 4см [Khafif A. et al. 1999, Stojadinovic A. et al. 2001], але без врахування у цих випадках інших факторів ризику (ШІ варіант, Т4). ШІ варіант обумовлював більш агресивну поведінку пухлин: тільки пухлини з ШІ варіантом ОР мали метастази (35.7%, 5/14) та летальні випадки (14.3%, 2/14), що не протирічить літературним даним [Stojadinovic A. et al. 2001, Decaussin M. et al. 2002].
При наявності розповсюдження пухлини за межі ЩЗ (Т4 стадія) пролонгація хвороби відмічена в 66.7% хворих (4/6) з діагностованими метастазами у порівнянні з 2.6% (1/38), коли пухлина обмежена тканиною ЩЗ. Смертність з Т4 стадією хвороби склала 32.3% (2/6) в противагу 0% - при Т1–3.
Серед досліджуваної групи виявлено, що наявність метастазів ОР на момент первинної операції збільшує вірогідність їх появи в подальшому (в середньому через 1,5 років). У 57% хворих (4/7) з метастазами на момент операції розвинулась метастатична хвороба в подальшому з летальністю 28.6% (2/7). Серед хворих, що не мали метастазів на момент операції, у 2.6% (1/37) випадків були діагностовані метастази в подальшому при відсутності смертельних випадків. Наявність метастазів як під час первинної діагностики ОР, так і поява їх згодом, значно погіршує прогноз хвороби [Stojadinovic A. et al. 2002, Kushchayeva Yе. et al. 2004, Kushchayeva Yе. et al. 2008].
За період нагляду у хворих з ОР ЩЗ метастази розвинулись у найкоротший час після операції (1,5 років) у порівнянні з ПР (1,9 років) та ФР ЩЗ (2,5 років) (р < 0.01), що підтверджує агресивність ОР ЩЗ.
Після тиреоїдектомії та органозберігаючих операцій метастазування та смертність зафіксовані в 13,3% (4/30) та 7,1% (1/14) і 3,3% (1/30) та 7,1% (1/14) відповідно. В досліджуваній групі в більшості хворих на ОР виконані радикальні операції (72,4%), оскільки подібна тактика збільшує діагностичні можливості у післяопераційному періоді та можливість раннього виявлення метастазів. Такий хірургічний підхід узгоджується з більшістю дослідників [Kebebew E., Clark O. 2000, Yutan E., Clark O. 2001, Besic N. et al. 2002, Kushchayeva Yе. et al. 2008].
Аналізуючи випадки метастазування серед досліджуваних груп, виявлено, що хворі з метастазами ОР ЩЗ були достовірно старші за хворих з ФР (р<0.05), але не відрізнялись за віком від хворих з ПР ЩЗ (р>0.05). Частота метастазів була вищою у випадках ОР ЩЗ після 45 років, ніж при ФР чи ПР ЩЗ, але без вірогідної різниці (р>0.05). Частота виникнення метастазів серед жінок та чоловіків в залежності від виду пухлини теж не мала достовірної різниці. Середній розмір пухлин у хворих з метастатичною хворобою був більший серед ОР (7.2+0,44см) на відміну від 4.5+0,25см за умов ПР та 4.8+0,03см за умов ФР ЩЗ (р<0.01). При розмірах первинного вогнища більше 4 см серед хворих з ФР та ОР частота метастазування виявилась вищою у випадках ОР ЩЗ (15.4% проти 7%).
В залежності від стадії захворювання пролонгація процесу зустрічалась майже з однаковою частотою для всіх видів досліджуваних раків при стадії Т1–3, складаючи 2.2% (3/135), 3.1% (4/129) та 2.5% (1/38) для ПР, ФР та ОР ЩЗ. При наявності Т4 стадії захворювання ОР та ФР частіше метастазували (66.7%, 4/6 та 20%, 1/5), ніж ПР ЩЗ (7%, 3/43) (р<0.05). Метастази зустрічались достовірно частіше при ОР, ніж при ПР ЩЗ при наявності ініціального метастазування: 57% (4/7) в противагу 10.7% (3/28) (р<0.05).
При наявності ШІ варіанту частота метастазів чи рецидивів була більшою для ОР ЩЗ (р<0.05). В той же час при МІ варіанті пролонгація процесу траплялась дуже рідко (1.7%, 2/115 – для ФР та 0% – для ОР ЩЗ) (р>0.05).
За підсумками даної роботи ОР ЩЗ є найбільш агресивним серед ДРЩЗ з високим рівнем метастазів у післяопераційному періоді, мінімальною ефективністю традиційного методу лікування пролонгації ДРЩЗ - 131I-терапії та найкоротшим періодом, вільним від метастазів. На сьогодні єдиним ефективним методом для лікування 131I –негативних метастазів є хірургічний. Принциповим для лікування захворювання є своєчасна діагностика метастазів, для чого одним з ефективних методів є подвійна сцинтиграфія з 99mТс–МІБІ (патент № 9221).
Отже, ОР за своїми властивостями знаходиться між ПР та ФР ЩЗ, але має найбільш агресивний перебіг з низькою чутливістю до традиційних методів діагностики та лікування ДРЩЗ, що повинно відображатись в протоколі післяопераційного нагляду даної групи хворих.
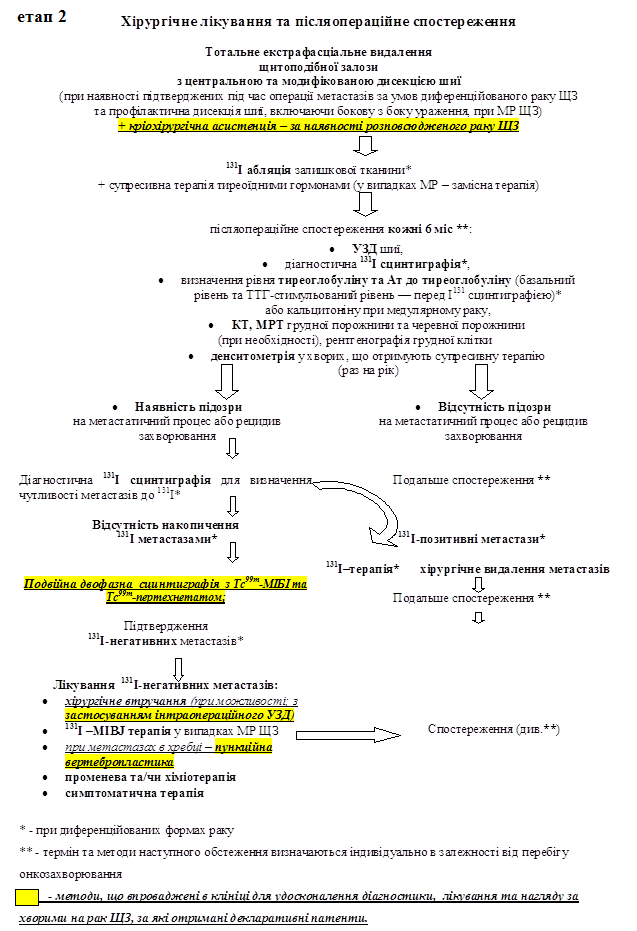
Тотальне екстрафасціальне видалення
щитоподібної залози
з центральною та модифікованою дисекцією шиї
(при наявності підтверджених під час операції метастазів)
![]()
131I абляція залишкової тканини
+ супресивна терапія тиреоїдними гормонами
![]()
післяопераційне спостереження кожні 3-6 міс (індивідуально)**:
· УЗД шиї,
· 131I сцинтиграфія (до кінцевої абляції тканини ЩЗ),
· визначення рівню тиреоглобуліну та а/т до тиреоглобуліну (базальний рівень та ТТГ–стимульований рівень — перед I131 сцинтіграфією),
· КТ, МРТ грудної порожнини та черевної порожнини
(при необхідності), рентгенографія грудної клітки
![]()
| · Наявність підозри на метастатичний процес або рецидив захворювання
| · Відсутність підозри на метастатичний процес або рецидив захворювання
|
|
| Подальше спостереження ** |
|
Відсутність накопичення 131I метастазами |
131I позитивні метастази
|
|
| 131I–терапіяхірургічне лікування
|
| Подвійна двохфазна 99mТс–МІБІ сцинтиграфія;
| Подальше спостереження ** |
| Підтвердження 131I негативних метастазів
| |
| Хірургічне втручання*** | Спостереження (див.**) |
| *** При неможливості оперативного лікування: проводиться паліативна терапія: променева терапія, хіміотерапія, пункційна вертебропластика (при метастатичному ураженні тіл хребців), стабілізуючі операції, можливо проведення редиференціюючої терапії (на сьогодні на стадії клінічних іспитів) та симптоматичне лікування. | |
Рис.1. Протокол лікування та нагляду хворих з оксифільноклітинним раком ЩЗ.
ВИСНОВКИ
1. Оксифільноклітинний рак за даними дослідження зустрічається у 2,05% випадків серед всіх видів карцином ЩЗ і по клінічному перебігу вірогідно відрізняється від ПР та ФР ЩЗ: старшим середнім віком пацієнтів; високим рівнем локальної екстратиреоїдної інвазійності; раннім лімфогенним метастазуванням; резистентністю до I131-діагностики і терапії; та більш частим метастазуванням.
2. Аналіз тактики хірургічного лікування пухлин щитоподібної залози за останні 10 років показав збільшення радикалізму операцій. У випадках оксифільноклітинного раку ЩЗ, враховуючи різке погіршення прогнозу при появі метастатичного процесу, обґрунтованим є тотальне екстрафасціальне видалення ЩЗ з профілактичною центральною дисекцією шиї та модифікованою дисекцією - при наявності підтверджених під час операції метастазів.
3. У випадках метастазів оксифільноклітинного раку ЩЗ радіойодтерапія є малоефективною у зв’язку з низькою чутливістю пухлин до I131 (≈ 10%). Ефективним методом діагностики метастазів ОР ЩЗ є подвійна сцинтиграфія з 99mТс–пертехнетатом та 99mТс–MIBI у поєднанні з визначенням рівню ТГ. Застосування даного методу дозволяє діагностувати йод-негативні метастази ОР на ранньому етапі та своєчасно проводити лікування.
4. Аналіз результатів післяопераційного спостереження показав, що у випадках ОР ЩЗ частота метастазів та рецидивів є більшою (11,4%), ніж у випадках ПР (3,8%) та ФР (3,8%) ЩЗ. Період виникнення метастазів ОР після операції є значно коротшим (1,5 років) у порівнянні з ПР (1,9 років) та ФР (2,5 років) ЩЗ. Летальність серед хворих з ОР ЩЗ виявилась найвищою (4,5%) порівнюючи з ПР (0,6%) та ФР ЩЗ (0,7%).
5. Серед факторів ризику, що вірогідно впливають на прогноз при ОР ЩЗ, є розповсюдження первинного вогнища за межі ЩЗ (Т4), виражена судинна та капсулярна інвазія (ШІ варіант) та наявність метастазів на момент первинного лікування.
6. Враховуючи особливості клінічного перебігу ОР ЩЗ розроблено алгоритм лікування та післяопераційного спостереження, що включає тотальне видалення ЩЗ, абляцію залишкової тканини з 131I та подальшим спостереженням за хворими з визначенням рівня ТГ, а/т до ТГ, виконанням УЗД шиї, КТ та/або МРТ та подвійної сцинтиграфії з 99mТс–пертехнетатомі 99mТс–MIBI.
ПРАКТИЧНІ РЕКОМЕНДАЦІЇ
1. При цитологічному діагнозі «фолікулярна неоплазія» на доопераційному етапі рекомендується ретельне УЗД регіонарних зон лімфовідтоку для планування об’єму операції, враховуючи схильність ОР до лімфогенного метастазування.
2. При експрес-гістологічному дослідженні „оксифільноклітинна неоплазія” рекомендується екстрафасціальна гемітиреоїдектомія з видаленням перешийка та щитоподібно-язикової зв’язки. При встановленні заключного морфологічного діагнозу „оксифільноклітинний рак” необхідною є остаточна тиреоїдектомія.
Похожие работы
... час: тенденції та фактори // Науковий вісник національного медичного університету ім. О.О. Богомольця. – 2007. – №1(11). – С.129 – 133. 23. Гульчій М.В. Клінічні особливості перебігу раку щитоподібної залози у поєднанні з іншою тиреоїдною патологією та без неї // Ліки України. – 2007. – №111. – С. 81 – 85. 24. Пат. № 49711 UA МПК А61В17/00. Спосіб косметичного підшкірного доступу ...
... і гіпотиреозу та на цій основі визначити об’єм оперативного втручання (рис. 2). ВИСНОВКИ У дисертації на основі ретроспективного аналізу результатів хірургічного лікування багатовузлового еутиреоїдного зоба (БВЕЗ), вивчення особливостей морфологічної структури, змін гормонального, імунологічного статусу та генетичних параметрів розроблено математичну модель прогнозування розвитку післяоперац ...



0 комментариев