Навигация
2.5 Физические свойства
Техническая медь — металл красного, в изломе розового цвета, при просвечивании в тонких слоях — зеленовато-голубой. Имеет гранецентрированную кубическую решетку с параметром а = 0,36074 нм, плотность 8,96 кг/м3 (20° С).
Основные физические свойства меди
Температура плавления, °С 1083
Температура кипения, °С 2600
Теплота плавления, кДж/г-ат. 0,7427
Теплота испарения, кДж/г-ат. 17,38
Удельная теплоемкость, Дж/(г.град) (20°С) 0,022
Теплопроводность, Дж/(м.град.с) (20°С) 2,25-10-3
Электрическое сопротивление, Ом.м (20°С) 1,68-Ю-4
Удельная магнитная восприимчивость, 0,086.10-6
абс. эл.-магн. ед./г (18 °С)
Медь — вязкий, мягкий и ковкий металл, уступающий только серебру высокой теплопроводностью и электропроводностью. Эти качества, а также пластичность и сопротивление коррозии обусловили широкое применение меди в промышленности.
2.6 Применение
Большая роль меди в технике обусловлена рядом её ценных свойств и, прежде всего высокой электропроводностью, пластичностью, теплопроводностью. Благодаря этим свойствам медь - это основной материал для проводов; свыше 50 % добываемой меди применяют в электротехнической промышленности. Все примеси понижают электропроводность меди, а потому в электротехнике используют металл высших сортов, содержащий не менее 99,9 % Cu. Высокие теплопроводность и сопротивление коррозии позволяют изготовлять из меди ответственные детали теплообменников, холодильников, вакуумных аппаратов и т. п. Около 30-40 % меди используют в виде различных сплавов, среди которых наибольшее значение имеют латуни (от 0 до 50 % Zn) и различные виды бронз; оловянистые, алюминиевые, свинцовистые, бериллиевые и т. д. (подробнее см. Сплавы меди). Кроме нужд тяжёлой промышленности, связи, транспорта, некоторое количество меди (главным образом в виде солей) потребляется для приготовления минеральных пигментов, борьбы с вредителями и болезнями растений, в качестве микроудобрений, катализаторов окислительных процессов, а также в кожевенной и меховой промышленности и при производстве искусственного шёлка.
Медь как художественный материал используется с медного века (украшения, скульптура, утварь, посуда). Кованые и литые изделия из меди и сплавов украшаются чеканкой, гравировкой и тиснением. Лёгкость обработки меди (обусловленная её мягкостью) позволяет мастерам добиваться разнообразия фактур, тщательности проработки деталей, тонкой моделировки формы. Изделия из меди отличаются красотой золотистых или красноватых тонов, а также свойством обретать блеск при шлифовке. Медь нередко золотят, патинируют, тонируют, украшают эмалью. С 15 века медь применяется также для изготовления печатных форм.
В медицине сульфат меди применяют как антисептическое и вяжущее средство в виде глазных капель при конъюнктивитах и глазных карандашей для лечения трахомы. Раствор сульфата меди используют также при ожогах кожи фосфором. Иногда сульфат меди применяют как рвотное средство. Нитрат меди употребляют в виде глазной мази при трахоме и конъюнктивитах.
2.8 Метод электролитического осаждения
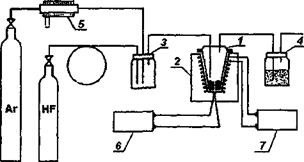
Метод электролитического осаждения – наиболее старый метод получения тонкопленочных структур металлов. В технологии производства изделий электронной техники этот метод для осаждения серебра, золота, меди и никеля, хрома, свинца, платины, олова, цинка и ряда других металлов [1]. Достаточно давно этот метод применяется для получения тонких пленок ферромагнитных металлов и их сплавов [2, 3]. Технологический процесс происходит в электролитической ванне, упрощенная схема которой представлена на рисунке 3.1. В качестве электролита такой ванны используются водные растворы солей осаждаемого металла. Например, для осаждения пленок никеля электролит содержит растворы сульфата никеля и хлористого аммония. Катионы, которые нужно осадить, могут присутствовать в электролите в виде свободных ионов или комплексов. Анод электролитической ванны соединен с положительным полюсом источника постоянного тока, катод, являющийся подложкой осаждаемой пленки – с отрицательным полюсом.
При пропускании через электролитическую ванну электрического тока, величина которого контролируется амперметром, катионы, в числе которых и катионы осаждаемого металла, движутся к катоду (в нашем примере Ni2+ и NH4+), анионы (SO42- и Cl-) – в противоположном направлении.
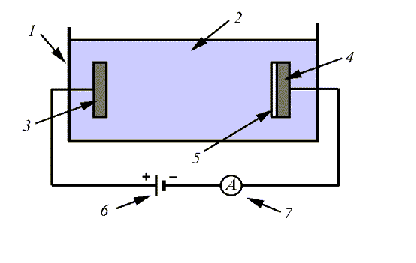
1 – ванна, 2 –электролит, 3 – анод, 4 – катод, 5 – пленка, 6 – источник питания, 7 – амперметр.
Рисунок 3.1 Схема электролитической ванны.
Согласно законам электролиза Фарадея скорость осаждения металла на катоде определяется плотностью электрического тока j , прошедшего через электролитическую ванну:
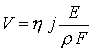 , (3.1)
, (3.1)
где h - выход по току; r - плотность осажденного металла; E – напряженность электрического поля; F – число Фарадея.
На рисунке 3.2. схематически показана вольтамперная характеристика процесса электролиза. При абсолютном значении потенциала катода j выше некоторой величины jН процесс электролитического осаждения достигает насыщения. С другой стороны при j < jР осаждение металлической пленки на катоде прекращается и наблюдается даже растворение катода. В этом режиме электролитическую ванну можно использовать для предварительной очистки подложки. Таким образом, технологический режим электролитического осаждения ограничен значениями потенциала катода от jН доjР.
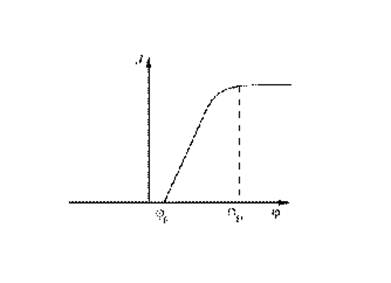
Рисунок 3.2 Зависимость тока электролитического осаждения от абсолютного значения потенциала катода.
На процесс электролитического осаждения металлической пленки существенное влияние оказывают состав электролита, кислотность электролитической ванны, плотность электрического тока, температура подложки и т.д. Технологические режимы, как правило, подбираются опытным путем из условия наилучшего протекания процесса электролитического осаждения. Для улучшения этого процесса в электролит добавляют различные присадки, которые не влияют на состав осаждаемой пленки, а для улучшения самого процесса электролитического осаждения. Например, не восстанавливающие катионы калия и кальция в электролите увеличивают его электропроводность. Добавки различных неорганических соединений уменьшают зависимость процесса от кислотности электролита.
Наиболее простой способ получения многослойных структур металлов возможен при многократном переносе подложки из одного электролита в другой, в каждом из которых осаждается пленка соответствующего металла. Таким способом еще в 1921 г. были получены пленки из чередующихся слоев меди и никеля. В современных методах электролитического осаждения многослойных структур металлов используется тот факт, что у многих металлов существенно отличаются их равновесные потенциалы восстановления [4]. Так, например, немагнитные металлы Cu, Ag, Au могут осаждаться при очень малых (иногда даже положительных) потенциалах катода, магнитные элементы группы железа эффективно осаждаются при достаточно высоких отрицательных потенциалах катода. Разница между ними может составлять 600 мВ и более [4, 5]. Это обстоятельство позволяет при использовании импульсного напряжения на катоде получать многослойные структуры из одного и того же электролита.
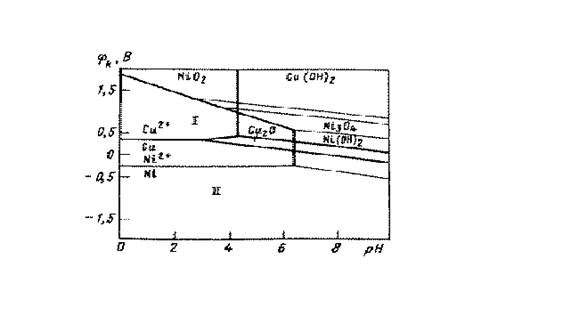
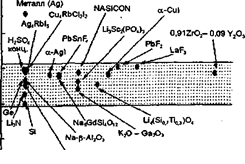
Рисунок 3.3 Совмещеннае диаграмма Пюрбаха меди и никеля [5]
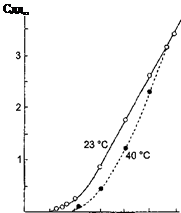
На рисунке 3.3 приведены совмещенные диаграммы Пюрбаха меди и никеля [4,5]. Из них видно, что при потенциале катода в области I на катоде будет осаждаться только медь. Если потенциал находится в области II, то будут осаждаться как медь, так и никель. В технологии электролитического осаждения многослойных структур из одного электролита используется электролит, содержащий соли обоих металлов. Предельная плотность тока осаждения каждого элемента в этом случае зависит от его концентрации в электролите. На рис. 3.4 в качестве примера приведена зависимость плотности тока осаждения меди от потенциала катода для электролитов с разным содержанием ионов меди. Из солей металлов в состав электролита входили никель сернокислый (NiSO4), никель хлористый (NiCl2) и медь сернокислая [5]. Кривая 1 соответствует простому электролиту, содержащему только ионы никеля с потенциалом насыщения, соответствующего точке В (сравнить с данными рисунке 3.2). По мере увеличения в электролите ионов меди в вольтамперной зависимости процесса электролитического осаждения наблюдается вторая область насыщения (точка А), которая определяется предельной плотностью тока осаждения меди. при значительно меньших потенциалах на катоде. Отсюда следует, что при потенциале катода 100…500 мВ (точка А, рисунке 3.4) на нем будет осаждаться чистая медь, так как этого потенциала еще недостаточно для осаждения никеля. Если теперь резко поднять потенциал катода до величины приблизительно 1000 мВ (точка В на рисунке 3.4), то выделяться будет практически только никель, так как скорость осаждения меди остается малой в сравнении со скоростью осаждения никеля.

Рисунок 3.4 Зависимость плотности тока осаждения меди от потенциала катода для электролитов с различной концентрацией ионов Cu2+ [4]
Для получения многослойных структур необходимо на катод электролитической ванны периодически подавать импульсы напряжения разной амплитуды и длительности, в течение которых на катоде будет осаждаться соответствующий металл. В зависимости от режимов подачи импульсов различают потенциостатическое и гальваностатическое импульсное электролитическое осаждение. При гальваностатическом осаждении на катоде поддерживается постоянной в течение каждого импульса плотность тока. Так, при получении Cu-Ni многослойных структур [5] плотность тока при осаждении слоя меди составляла 1,5 мА/см2, в то время как при осаждении слоя никеля плотность тока поддерживалась равной 100 мА/см2. В потенциостатическом режиме постоянными на катоде поддерживались напряжения: 400 мВ для меди и 1000 мВ для никеля. При длительности импульсов 5,5 с и 0,2 с при осаждении Cu и Ni соответственно формировались слои этих металлов одинаковой толщины по 100 Å.
Потенциостатический режим осаждения в большинстве случаев позволяет получать более резкую границу между слоями в магнитных многослойных структурах. При оптимальном выборе режимов электролитического осаждения содержание магнитного элемента в немагнитном и наоборот может не превышать 0,5…0,1 % [4].
Похожие работы
... при изучении синтеза новых материалов и процессов ионного транспорта в них. В чистом виде такие закономерности наиболее четко прослеживаются при исследовании монокристаллических твердых электролитов. В то же время при использовании твердых электролитов в качестве рабочих сред функциональных элементов необходимо учитывать, что нужны материалы заданного вида и формы, например в виде плотной керамики ...
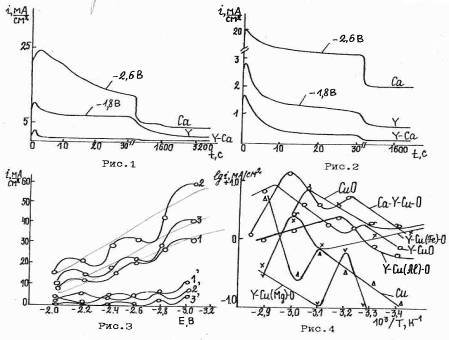
... растворения, обусловленного кислотностью среды (i0) имеют порядок по CuC12 в интервале концентраций последнего 10-2 - 10-1 моль/л 2,1. Рис.4. Зависимость скорости коррозии меди в 5М изопропанольных растворах НС1 от содержания Н2О в растворителе. Неподвижный электрод. Комнатная температура. t=2 часа.Рис.5. Поляризационные кривые на меди в ...
... и приписывают ему решающее значение. Самой характерной и отличительной особенностью процесса ЭХП является подавление структурного травления металлической поверхности, несмотря на её физико-химическую и электрохимическую гетерогенность. Даже при условии равномерного растворения поверхности металла можно объяснить эффект сглаживания шероховатостей, исходя из простых геометрически соображений. В ...
... в системе Са-У-Си-0 ВТСП-фаз. Представлены новые данные для обоснования теории электрохимического внедрения элементов в твердые металлические электроды, развиваемой в работах Кабанова Б.Н., Астахова И.И., Киселевой И.Г., Поповой С.С. и др.) Практическая значимость. Результаты исследований показали принципиальную возможность формирования пленочных купратных систем типа Са-У-Си-0 электрохимическим ...



0 комментариев