Профессор А.М. Шилов
ММА имени И.М. Сеченова
Ключевая роль тромбоза артерий сердца в формировании острого коронарного синдрома, вплоть до развития острого инфаркта миокарда (ОИМ), в настоящее время постулирована. На смену традиционно сложившейся консервативной терапии коронарной патологии, направленной на предотвращение осложнений: опасных нарушений ритма, острой сердечной недостаточности (ОСН), ограничение зоны повреждения миокарда (путем усиления коллатерального кровотока), в клиническую практику внедрены радикальные методы лечения – реканализация ветвей коронарных артерий путем как фармакологического воздействия (тромболитические средства), так и инвазивного вмешательства – чрескожная транслюминальная балонная или лазерная ангиопластика с установкой стента(ов) или без нее.
Накопленный клинический и экспериментальный опыт указывают, что восстановление коронарного кровотока – «обоюдоострый меч», т.е. в 30% и более развивается «синдром реперфузии», манифестирующий дополнительным повреждением миокарда, вследствие неспособности энергетической системы кардиомиоцита утилизировать «нахлынувшее» поступление кислорода. В результате этого увеличивается образование свободно–радикальных, активных форм кислорода (АК), способствующих повреждению липидов мембран – перекисное окисление липидов (ПОЛ), дополнительному повреждению функционально важных белков, в частности, цитохромной дыхательной цепи и миоглобина, нуклеиновых кислот и других структур кардиомиоцитов [1,7,11]. Такова упрощенная модель постперфузионного метаболического круга развития и прогрессирования ишемического повреждения миокарда. В связи с этим в настоящее время разработаны и активно внедряются в клиническую практику фармакологические препараты противоишемической (антигипоксанты) и антиоксидной (антиоксиданты) защиты миокарда [4,8,10,12,13].
Антигипоксанты – препараты, способствующие улучшению утилизации организмом кислорода и снижению потребности в нем органов и тканей, суммарно повышающие устойчивость к гипоксии. В настоящее время наиболее изучена антигипоксическая и антиоксидантная роль Актовегина (Nycomed) в клинической практике лечения различных ургентных состояний ССС.
Актовегин – высокоочищенный гемодиализат, получаемый методом ультрафильтрации из крови телят, содержащий аминокислоты, олигопептиды, нуклеозиды, промежуточные продукты углеводного и жирового обмена (олигосахариды, гликолипиды), электролиты (Mg, Na, Ca, P, K), микроэлементы (Si, Cu).
Основой фармакологического действия Актовегина является улучшение транспорта, утилизации глюкозы и поглощения кислорода:
– повышается обмен высокоэнергетических фосфатов (АТФ);
– активируются ферменты окислительного фосфорилирования (пируват– и сукцинатдегидрогеназы, цитохром С–оксидаза);
– повышается активность щелочной фосфатазы, ускоряется синтез углеводов и белков;
– увеличивается приток ионов К+ в клетку, что сопровождается активацией калий–зависимых ферментов (каталаз, сахараз, глюкозидаз);
– ускоряется распад продуктов анаэробного гликолиза (лактата, -гидроксибутирата).
Активные компоненты, входящие в состав Актовегина, оказывают инсулиноподобное действие. Олигосахариды Актовегина активируют транспорт глюкозы внутрь клетки, минуя рецепторы инсулина. Одновременно Актовегин модулирует активность внутриклеточных носителей глюкозы, что сопровождается интенсификацией липолиза. Что чрезвычайно важно – действие Актовегина инсулинонезависимое и сохраняется у пациентов с инсулинозависимым сахарным диабетом, способствует замедлению прогрессирования диабетической ангиопатии и восстановлению капиллярной сети за счет новообразования сосудов [2,9].
Улучшение микроциркуляции, которое наблюдается под действием Актовегина, видимо, связано с улучшением аэробного обмена сосудистого эндотелия, способствующего высвобождению простациклина и оксида азота (биологических вазодилататоров). Вазодилатация и снижение периферического сосудистого сопротивления являются вторичными по отношению к активации кислородного метаболизма сосудистой стенки.
Таким образом, антигипоксическое действие Актовегина суммируется через улучшение утилизации глюкозы, усвоение кислорода и снижение потребления миокардом кислорода в результате уменьшения периферического сопротивления.
Антиоксидантное действие Актовегина обусловлено наличием в этом препарате высокой супероксиддисмутазной активности, подтвержденной атомно–эмиссионной спектрометрией, наличием препаратов магния и микроэлементов, входящих в простетическую группу супероксиддисмутазы. Магний – обязательный участник синтеза клеточных пептидов, он входит в состав 13 металлопротеинов, более 300 ферментов, в том числе в состав глутатионсинтетазы, осуществляющей превращение глутамата в глутамин [9].
Накопленный клинический опыт отделений интенсивной терапии позволяет рекомендовать введение высоких доз Актовегина: от 800–1200 мг до 2–4 г. Внутривенное введение Актовегина целесообразно:
– для профилактики синдрома реперфузии у больных ОИМ, после проведения тромболитической терапии или балонной ангиопластики;
– больным при лечении различных видов шока;
– больным, переносящим остановку кровообращения и асфиксию;
– больным с тяжелой сердечной недостаточностью;
– больным с метаболическим синдромом Х.
Антиоксиданты – блокируют активацию свободнорадикальных процессов (образование АК) и перекисного окисления липидов (ПОЛ) клеточных мембран, имеющих место при развитии ОИМ, ишемического и геморрагического инсультов, острых нарушений регионального и общего кровообращения. Их действие реализуется через восстановление свободных радикалов в стабильную молекулярную форму, не способную участвовать в цепи аутоокисления. Антиоксиданты либо непосредственно связывают свободные радикалы (прямые антиоксиданты), либо стимулируют антиоксидантную систему тканей (непрямые антиоксиданты).
Энергостим – комбинированный препарат содержащий никотинамидадениндинуклеотид (НАД), цитохром С и инозин в соотношении: 0,5, 10 и 80 мг соответственно.
При ОИМ нарушения в системе энергетического обеспечения происходят в результате потери кардиомиоцитом НАД – кофермента дегидрогеназы гликолиза и цикла Кребса, цитохрома С – фермента цепи переноса электронов, с которым в митохондриях (Мх) сопряжен синтез АТФ через окислительное фосфорилирование. В свою очередь, выход цитохрома С из Мх ведет не только к развитию энергодефицита, но и способствует образованию свободных радикалов и прогрессированию оксидативного стресса, заканчивающихся гибелью клеток по механизму апоптоза. После внутривенного введения экзогенный НАД, проникая через сарколемму и мембраны Мх, ликвидирует дефицит цитозольного НАД, восстанавливает активность НАД–зависимых дегидрогеназ, участвующих в синтезе АТФ гликолитическим путем, способствует интенсификации транспорта цитозольного протона и электронов в дыхательной цепи Мх. В свою очередь, экзогенный цитохром С в Мх нормализует перенос электронов и протонов к цитохромоксидазе, что суммарно стимулирует АТФ–синтезирующую функцию окислительного фосфорилирования Мх. Однако ликвидация дефицита НАД и цитохрома С не нормализует полностью «конвейер» синтеза АТФ кардиомиоцита, так как не оказывает существенного влияния на содержание отдельных компонентов адениловых нуклеотидов, участвующих в дыхательной цепи клеток. Восстановление общего содержания адениловых нуклеотидов имеет место при введении инозина – метаболита, стимулирующего синтез адениловых нуклеотидов. Одновременно инозин усиливает коронарный кровоток, способствует доставке и утилизации кислорода в области микроциркуляции.
Таким образом, целесообразно комбинированное введение НАД, цитохрома С и инозина для эффективного воздействия на метаболические процессы в кардиомиоцитах, подвергнутых ишемическому стрессу.
Энергостим по механизму фармакологического воздействия на клеточный метаболизм имеет комбинированное влияние на органы и ткани: антоксидантное и антигипоксическое. За счет композитного состава Энергостим, по данным различных авторов, по эффективности лечения ИМ в составе традиционного лечения во много раз превосходит действие других признанных в мире антигипоксантов: в 2–2,5 раза оксибутират лития, рибоксин (инозин) и амитазол, в 3–4 раза – карнитин (милдронат), пирацетам, олифен и солкосерил, в 5–6 раз – цитохром С, асписол, убихинон и триметазидин [1,11]. Рекомендуемые дозы Энергостима в комплексной терапии ИМ: 110 мг (1 флакон) в 100 мл 5% глюкозы 2–3 раза в день в течение 4–5 дней. Все изложенное выше позволяет считать Энергостим препаратом выбора в комплексной терапии ИМ, для профилактики осложнений, являющихся следствием метаболических нарушений в кардиомиоцитах [1,3].
Коэнзим Q10 – витаминоподобное вещество, впервые было выделено в 1957 г. из митохондрий бычьего сердца американским ученым Ф. Крейном. К. Фолкерс в 1958 г. определил его структуру. Вторым официальным названием коэнзима Q10 является убихинон (вездесущий хинон), так как он содержится в различных концентрациях практически во всех тканях животного происхождения. В 60–х годах была показана роль Q10, как электронного переносчика в дыхательной цепи Мх. В 1978 г. П. Митчел предложил схему, объясняющую участие коэнзима Q10 как в электронном транспорте в митохондриях, так и в сопряжении процессов электронного транспорта и окислительного фосфорилирования, за что получил Нобелевскую премию [8].
Коэнзим Q10 эффективно защищает липиды биологических мембран и липопротеидные частицы крови (фосфолипиды – «мембранный клей») от разрушительных процессов перекисного окисления, предохраняет ДНК и белки организма от окислительной модификации в результате накопления активных форм кислорода (АК). Коэнзим Q10 синтезируется в организме из аминокислоты – тирозин при участии витаминов группы Ви С, фолиевой и пантотеновой кислот, ряда микроэлементов. С возрастом биосинтез коэнзима Q10 прогрессивно снижается, а его расход при физических, эмоциональных нагрузках, в патогенезе различных заболеваний и окислительном стрессе возрастает [5].
Более чем 20–летний опыт клинических исследований применения коэнзима Q10 у тысяч больных убедительно доказывают роль его дефицита в патологии ССС, что не удивительно, так как именно в клетках сердечной мышцы наиболее велики энергетические потребности. Защитная роль коэнзима Q10 обусловлена его участием в процессах энергетического метаболизма кардиомиоцита и антиоксидантными свойствами. Уникальность обсуждаемого препарата – в его регенеративной способности под действием ферментных систем организма. Это отличает коэнзим Q10 от других антиоксидантов, которые, выполняя свою функцию, необратимо окисляются сами, требуя дополнительного введения [6].
Первый положительный клинический опыт в кардиологии по применению коэнзима Q10 был получен при лечении больных с дилатационной кардиомиопатией и пролапсом митрального клапана: были получены убедительные данные в улучшении диастолической функции миокарда. Диастолическая функция кардиомиоцита – энергоемкий процесс и при различных патологических состояниях ССС потребляет до 50% и более всей энергии, содержащейся в АТФ, синтезируемого в клетке, что определяет ее сильную зависимость от уровня коэнзима Q10.
Клинические исследования последних десятилетий показали терапевтическую эффективность коэнзима Q10 в комплексном лечении ИБС, артериальной гипертонии, атеросклероза и синдрома хронической усталости. Накопленный клинический опыт позволяет рекомендовать применение Q10 не только в качестве эффективного препарата в комплексной терапии СС заболеваний, но и как средство их профилактики.
Профилактическая доза Q10 для взрослых – 15 мг/сутки, лечебные дозы 30–150 мг/сутки, а в случаях интенсивной терапии – до 300–500 мг/сутки. Следует принять во внимание, что высокие лечебные дозы при оральном приеме коэнзима Q10 связаны с трудностью усвоения жирорастворимых веществ, поэтому в настоящее время для улучшения биодоступности создана водорастворимая форма убихинона.
Экспериментальные исследования показали профилактический и лечебный эффект коэнзима Q10 при реперфузионном синдроме, документируемые сохранением субклеточных структур кардиомиоцитов, подвергнутых ишемическому стрессу, и функции окислительного фосфорилирования Мх [5,6].
Клинический опыт применения коэнзима Q10 пока ограничен лечением детей с хроническими тахиаритмиями, синдромом удлиненного интервала QT, кардиомиопатиями, синдромом слабости синусового узла [14].
Таким образом, четкое представление о патофизиологических механизмах повреждения клеток тканей и органов, подвергнутых ишемическому стрессу, в основе которых лежат метаболические нарушения – перекисное окисление липидов, имеющих место при различных СС заболеваниях, диктуют необходимость включения антиоксидантов и антигипоксантов в комплексную терапию ургентных состояний.
Список литературы
1. Андриадзе Н.А., Сукоян Г.В., Отаришвили Н.О и др. Антигипоксант прямого действия энергостим в лечении ОИМ. Росс. Мед. Вести,2001,№2, 31–42.
2. Бояринов А.П., Пенкнович А.А., Мухина Н.В. Метаболические эффекты нейротропного действия актовегина в условиях гипоксии. Актовегин. Новые аспекты клинического применения. М., 2002, 10–14.
3. Джанашия П.Х., Проценко Е.А., Сороколетов С.М. Энергостим в лечении хронических форм ИБС. Росс. Кард. Ж., 1988,№5, 14–19.
4. Закирова А.Н. Корреляционные связи перикисного окисления липидов, антиоксидантной защиты и микрореологических нарушений в развитии ИБС. Тер.архив, 1966,№3, 37–40.
5. Капелько В.И., Рууге Э.К. Исследование действия коэнзима Q10 (убихинона) при ишемии и реперфузии сердца. Применение антиоксидантного препарата кудесан (коэнзим Q 10 с витамином Е) в кардиологии. М., 2002. 8–14.
6. Капелько В.И., Рууге Э.К. Исследования действия Кудесана при повреждении сердечной мышцы, вызванной стрессом. Применение антиоксидантного препарата кудесан (коэнзим Q10 c витамином Е) в кардиологии. М., 2002, 15–22.
7. Коган А.Х., Кудрин А.Н., Кактурский Л.В. и др. Свободнорадикальные перикисные механизмы патогенеза ишемии и ИМ и их фармакологическая регуляция. Патофизиология, 1992, №2, 5–15.
8. Коровина Н.А., Рууге Э.К. Использование коэнзима Q10 в профилактике и лечении. Применение антиоксидантного препарата кудесан (коэнзим Q10 с витамином Е) в кардиологии. М.,2002, 3–7.
9. Нордвик Б. Механизм действия и клиническое применение препарата актовегина. Актовегин. Новые аспекты клинического применения. М., 2002, 18–24.
10. Румянцева С.А. Фармакологическая характеристика и механизм действия актовегина. Актовегин. Новые аспекты клинического применения . М.,2002, 3–9.
11. Слепнева Л.В. Алексеева Н.И., Кривцова И.М. Острая ишемия органов и ранние постишемические расстройства. М., 1978, 468–469.
12. Смирнов А.В., Криворучка Б.И. Антигипоксанты в неотложной медицине. Анест. И реаниматол., 1998, №2, 50–57.
13. Шабалин А.В., Никитин Ю.П. Защита кардиомиоцита. Современное состояние и перспективы. Кардиология, 1999, №3, 4–10.
14. Школьникова М.А. Отчет Ассоциации детских кардиологов России по применению Кудесана. Применение антиоксидантного препарата кудесан (коэнзим Q10 с витамином Е) в кардиологии. М., 2002, 23.
Похожие работы
... ферментов, уменьшается также разрушение фосфолипидов как источников субстратов для перекисного окисления). Во многих ситуациях использование антиоксидантной активности антигипоксантов является более рациональным, чем применение антиоксидантов, поскольку профилактика заболевания (в данном случае предотвращение образования свободных радикалов антигипоксантами) обычно эффективнее его лечения ( ...
... развития инфекционно-токсического шока, гиповолемического шока, острой дыхательной недостаточности, полиорганной недостаточности и обострением течения сопутствующих заболеваний. На догоспитальном этапе в оказании экстренной медицинской помощи чаще нуждаются больные с менигококковой инфекцией, острой кишечной инфекцией, тяжелыми и осложненными формами гриппа, дифтерией, малярией, ботулизмом, ...
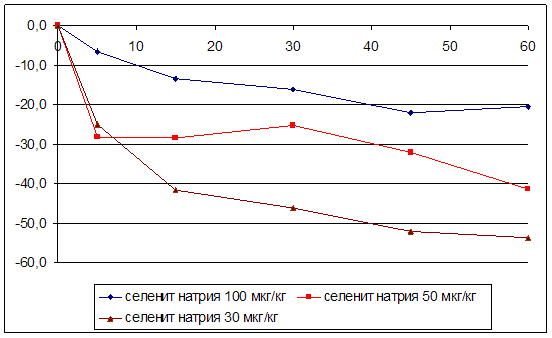
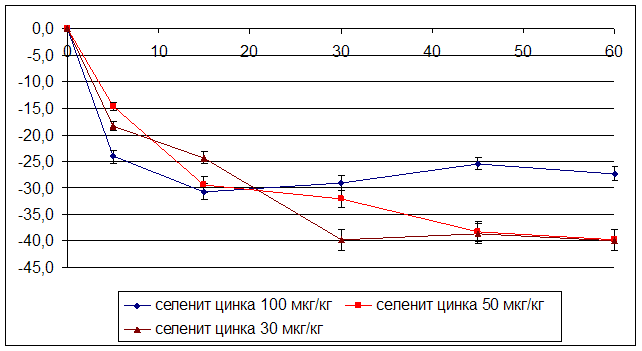
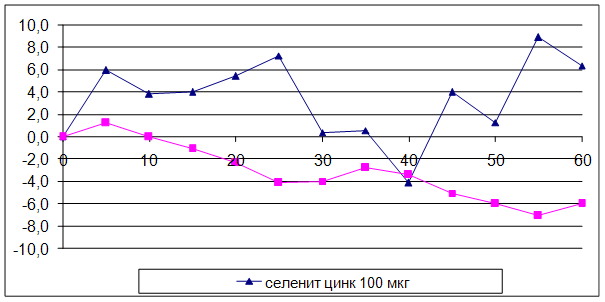
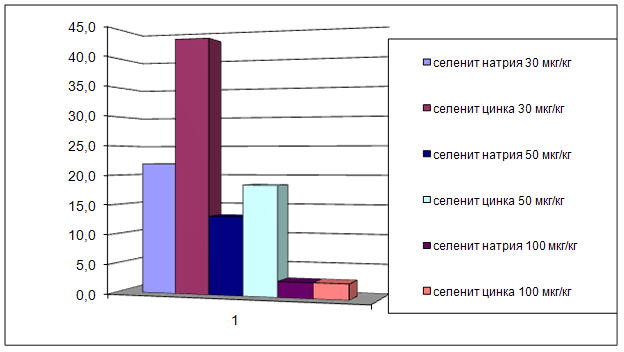
... на мозговой кровоток, динамику развития постишемических феноменов и психоневрологический статус остаётся неизученным. Указанные обстоятельства и послужили основанием для сравнительного изучения влияния селенита натрия и селенита цинка на системную гемодинамику и мозговой кровоток в условиях нормы и при патологических состояниях. ГЛАВА 2 МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ 2.1 Изучение острой ...
0 комментариев