Навигация
Кислотные свойства
3.11 Кислотные свойства
Кислотные свойства фенола проявляются в реакциях со щелочами (сохранилось старинное название «карболовая кислота»):
С6Н5ОН + NaOH <-> C6H5ONa + Н2O
Фенол, однако, является очень слабой кислотой. При пропускании через раствор фенолятов углекислого или сернистого газов выделяется фенол – такая реакция позывает, что фенол – более слабая кислота, чем угольная и сернистая:
C6H5ONa + СO2 + Н2O -> С6Н5ОН + NaHCО3
Кислотные свойства фенолов ослабляются при введении в кольцо заместителей I рода и усиливаются при введении заместителей II рода.
4. Способы получения
Производство фенола в промышленном масштабе осуществляется тремя способами:
– Кумольный метод. Этим способом получают более 95% всего производимиого в мире фенола. В каскаде барботажных колонн кумол подвергают некаталитическому окислению воздухом с образованием гидропероксида кумола (ГПК). Полученный ГПК, при катализе серной кислотой, разлагают с образованием фенола и ацетона. Кроме того, ценным побочным продуктом этого процесса является α-метилстирол.
– Около 3% всего фенола получают окислением толуола, с промежуточным образованием бензойной кислоты.
– Весь остальной фенол выделяют из каменноугольной смолы.
4.1 Окислением кумола
Фенолы выделяют из каменноугольной смолы, а также из продуктов пиролиза бурых углей и древесины (деготь). Промышленный способ получения самого фенола С6Н5ОН основан на окислении ароматического углеводорода кумола (изопропилбензол) кислородом воздуха с последующим разложением получающейся гидроперекиси, разбавленной H2SO4. Реакция проходит с высоким выходом и привлекательна тем, что позволяет получить сразу два технически ценных продукта – фенол и ацетон. Другой способ–каталитический гидролиз галогензамещенных бензолов.
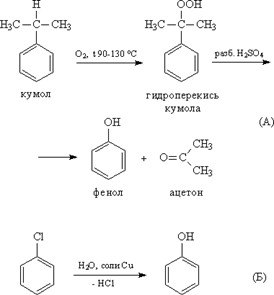
4.2 Получение из галогенбензолов
При нагревании хлорбензола и гидроксида натрия под давлением получают фенолят натрия, при дальнейшей обработке которого кислотой образуется фенол:
С6Н5-CI + 2NaOH -> С6Н5-ONa + NaCl + Н2O
4.3 Получение из ароматических сульфокислот
Реакция проводится при сплавлении сульфокислот с щелочами. Первоначально образующиеся феноксиды обрабатывают сильными кислотами для получения свободных фенолов. Метод обычно применяют для получения многоатомных фенолов:
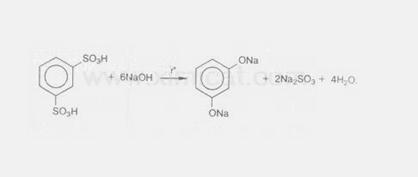
4.4 Получение из хлорбензола
Известно, что атом хлора прочно связан с бензольным кольцом, поэтому реакцию замены хлора на гидроксильную группу проводят в жестких условиях (300 °С, давление 200 МПа):
C6H5-Cl + NaOH – > C6H5-OH + NaCl
5. Применение фенолов
Раствор фенола используют в качестве дезинфицирующего средства (карболовая кислота). Двухатомные фенолы – пирокатехин, резорцин (рис. 3), а также гидрохинон (пара-дигидроксибензол) применяют как антисептики (антибактериальные обеззараживающие вещества), вводят в состав дубителей для кожи и меха, как стабилизаторы смазочных масел и резины, а также для обработки фотоматериалов и как реагенты в аналитической химии.
В виде отдельных соединений фенолы используются ограниченно, зато их различные производные применяют широко. Фенолы служат исходными соединениями для получения разнообразных полимерных продуктов – феноло-альдегидных смол, полиамидов, полиэпоксидов. На основе фенолов получают многочисленные лекарственные препараты, например, аспирин, салол, фенолфталеин, кроме того, красители, парфюмерные продукты, пластификаторы для полимеров и средства защиты растений.
Мировое потребление фенола имеет следующую структуру:
· 44% фенола расходуется на производство бисфенола А, который, в свою очередь, используется для производства поликарбона и эпоксидных смол;
· 30% фенола расходуется на производство фенолформальдегидных смол;
· 12% фенола гидрированием превращается в циклогексанол, используемый для получения искусственных волокон – нейлона и капрона;
· остальные 14% расходуются на другие нужды, в том числе на производство антиоксидантов (ионол), неионогенных ПАВ – полиоксиэтилированных алкилфенолов (неонолы), других фенолов (крезолов), лекарственных препаратов (аспирин), антисептиков (ксероформа) и пестицидов.
· 1,4% фенола применяется в медицине (орасепт), как обезболивающее и антисептическое средство.
6. Токсические свойства
Фенол ядовит. Вызывает нарушение функций нервной системы. Пыль, пары и раствор фенола раздражают слизистые оболочки глаз, дыхательных путей, кожу (ПДК 5 мг/м³, в водоёмах 0,001 мг/л).
Попадая в организм, Фенол очень быстро всасывается даже через неповрежденные участки кожи и уже через несколько минут начинает воздействовать на ткани головного мозга. Сначала возникает кратковременное возбуждение, а потом и паралич дыхательного центра. Даже при воздействии минимальных доз фенола наблюдается чихание, кашель, головная боль, головокружение, бледность, тошнота, упадок сил. Тяжелые случаи отравления характеризуются бессознательным состоянием, синюхой, затруднением дыхания, нечувствительностью роговицы, скорым, едва ощутимым пульсом, холодным потом, нередко судорогами. Зачастую фенол является причиной онкозаболеваний. При остром отравлении, сопровождающем попадание фенола на кожу или вдыхание его паров, наблюдается сильное жжение в местах, подвергшихся его непосредственному воздействию. Проявляются ожоги слизистых тканей; возникает сильная боль в области рта, в глотке, животе; тошнота, рвота, понос; резкая бледность, слабость, отек легких; возможны острые аллергические проявления; артериальное давление понижено; развивается сердечно-легочная недостаточность, возможны судороги; моча бурая, быстро темнеет на воздухе.
Первая помощь – снять одежду (желательно сразу под душем), промыть пораженное место большим количеством воды. Прикрыть места ожогов фенолом чистой белой тканью. Если брызги фенола попали в глаза, необходимо обильно промывать их водой не менее 15 минут. Промыть желудок водой, внутрь дать активированный уголь. Спирт и вазелиновое масло противопоказаны. Во время стационарного лечения больному даются обволакивающие средства и анальгетики, подается О2 с обеспечением адекватной вентиляции легких, производится коррекция водноэлектролитного баланса.
7. Физико-химические методы определения фенола
7.1 Фотоколориметрическое определение массовой доли фенолов в очищенных производственных сточных водах после установки обессмоливания
фенол химический токсический получение
1. Цель работы.
1. Ознакомление с использованием фотометрии при проведении лабораторного аналитического контроля за составом сточных вод, работой очистных сооружений и влиянием их на гидрохимический состав водоема.
2. Ознакомление с методикой определения содержания фенолов в очищенных сточных производственных водах фотоколориметрическим методом.
3. Оценка качества очистки воды.
2. Основные теоретические положения.
Группу фенолов образуют ароматические, гидроксил содержащие соединения, в которых гидроксилы находятся в бензольном ядре. Фенолы присутствуют и бытовых сточных водах и различных производственных сточных водах заводов, производящих пластические массы, анилокрасочных, химико-фармацевтических заводов, в водах от пирогенного разложения топлива и горючих сланцев. Фенолы очень токсичны, и потому в воде водных объектов хозяйственно-питьевого и культурно-бытового во-допользования предельно-допустимые концентрации их очень малы (ПДК = 0.001 мг/л).
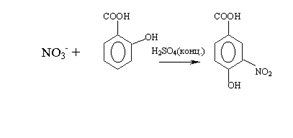
Рассматриваемый метод распространяется на воды сточные производственные, очищенные от смол, разбавленные технической водой до определенной концентрации фенолов после установки обессмоливания. В этом случае допустимая концентрация фенолов, определяемая стандартом предприятия, конечно, значительно выше – 800 мг/л. Метод основан на том, что фенолы С6Н5NH2, сочетаясь с диазосоединением, образуют красители, растворы которых интенсивно окрашены даже при малых концентрациях. Реакция протекает в щелочной среде, в которой фенол превращается в фенолят С6Н5ONa. Фенолят реагирует с диазотированным паранитроанилином в соответствии с уравнением:
О2N−NH2⋅HCl + HNO2 → ON2−N≡NCl + H2O
O2N−N≡NCl + ONa → ON2−N=N− ONa + HCl
Продукт реакции окрашен в оранжевый цвет. По этой методике можно определять от 0.5 до 4.0 мг/л фенолов. При больших концентрациях необходимо предварительное разведение. Жесткость устраняется добавлением 0.5 – 1 мл 50%-ного (масс.) раствора сегнетовой соли (калий-натрий виннокислый) и трилона Б на 550 мл пробы. Взвешенные вещества устраняются центрифугированием и фильтрованием. Объем отбираемой пробы должен быть не более 200 мл.
3. Методика выполнения работы.
Выполнение работы включает следующие этапы:
1.) Приготовление раствора паранитроанилина.
2.) Построение калибровочного графика.
3.) Проведение анализа отобранной пробы сточной воды.
4.) Оценка результатов определения.
1. Приготовление раствора паранитроанилина.
Взвешивают на аналитических весах 0.6900 г. паранитроанилина, помещают навеску в термостойкий химический стакан и растворяют в 65 мл 1 М HCl при нагревании. Переносят приготовленный раствор в мерную колбу вместимостью 1 л, доводят до метки дистиллированной водой и перемешивают.
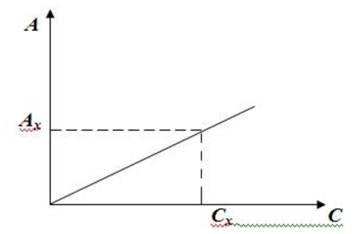
2. Построение калибровочного графика.
Для построения калибровочного графика используют ту же фенольную воду, которая подверглась очистке на данном очистном сооружении. Предварительно в ней определяется концентрация фенола гравиметрическим методом конденсации. Для серийных анализов этот метод не пригоден вследствие его длительности и потому его используют только для установления точной концентрации фенола в стандартном растворе, который будет использован для построения калибровочного графика.
2.1. Основной стандартный раствор.
Основной стандартный раствор – это фенольная вода, очищенная в данном очистном сооружении, концентрацию в которой уже установили методом конденсации.
2.2. Рабочий стандартный раствор.
Для его приготовления 10 мл основного стандартного раствора переносится пипеткой в мерную колбу вместимостью 1 л и доводится до метки дистиллированной водой.
2.3. Растворы для построения калибровочного графика.
Эти растворы готовят из рабочего стандартного раствора. Для этого в мерные колбы вместимостью 100 мл наливают с помощью бюретки рассчитанные количества рабочего стандартного раствора и доводят до метки дистиллированной водой с таким расчетом, чтобы в результате получился следующий ряд растворов фенолов: 0,5; 1,0; 1,5; 2,0; 2,5; 3,0; 3,5; 4,0 мг/л.
Похожие работы
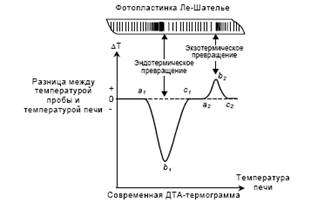
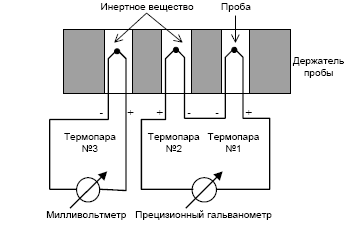
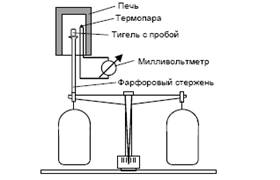
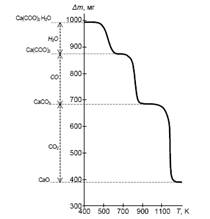
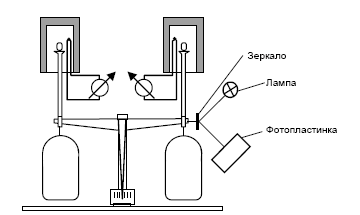
... анализа, что делает его одним из наиболее точных методов (наряду с классическим весовым анализом). 7.2 Дериватография коррозия бетон термических физический превращение Комплексный метод исследования химических и физико-химических процессов, происходящих в образце в условиях программированного изменения температуры, который основан на сочетании дифференциального термического анализа (ДТА) с ...
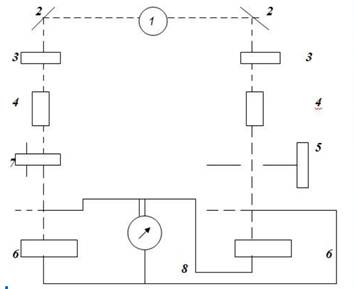
... свет вещества и толщине слоя раствора, через который он проходит. Закон Бугера - Ламберта - Бера является основным законом светопоглощения и лежит в основе большинства фотометрических методов анализа. Математически он выражается уравнением: или Величину lg I /I0 называют оптuческой плотностью поглощающего вещества и обозначают буквами D или А. Тогда закон можно записать так: ...
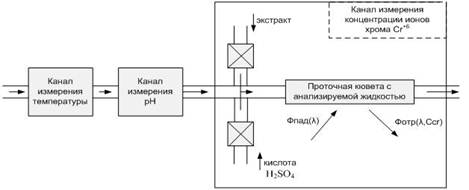
ления тяжелых металлов в природных водах Экстракционно-фотометрический метод определения хрома[16] На протекание естественных процессов в воде большое влияние оказывает содержание в ней тяжелых металлов. Были проведены исследования, целью которых являлась количественная оценка загрязнения реки Кальмиус тяжелыми металлами. Результаты данного исследования показали, что одним из тяжелых металлов ...
... . Сигнал детектора фиксируется регистратором (в виде пиков) и обрабатывается вычислительным интегратором. В ГХ используют детекторы, которые преобразуют в электрический сигнал изменения физических или физико-химических свойств газового потока, выходящего из колонки, по сравнению с чистым газом - носителем. Существует множество детекторов, однако широкое применение находят только те из них, ...



0 комментариев