Навигация
Молокосвертывающие ферментные препараты, используемые в сыроделии
Министерство образования Республики Беларусь
Учреждение образования «МОГИЛЕВСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
ПРОДОВОЛЬСТВИЯ»
Кафедра технологии молока и молочных продуктов
МОЛОКОСВЕРТЫВАЮЩИЕ ФЕРМЕНТНЫЕ ПРЕПАРАТЫ, ИСПОЛЬЗУЕМЫЕ В СЫРОДЕЛИИ
Специальность 1-49 01 02 «Технология хранения и переработки животного сырья»
Специализация 1-49 01 02 02 «Технология молока и молочных продуктов»
МОГИЛЕВ 2007
СОДЕРЖАНИЕ
Введение
1 Номенклатура. Классификация ферментов
2 Свойства молокосвертывающих энзимов
3 Молокосвертывающие ферменты растительного происхожденя
4 Описание марок молокосвертывающих ферментных препаратов.Сычужные препараты
5 Описание марок молокосвертывающих ферментных препаратов. Пепсин
6 Разработкякомпании «Даниско»
7 Роль в сыроделии ферментных препаратов
8 Ферментные препараты «КЛЕРИЧИ»
Заключение
Список литературы
ВВЕДЕНИЕ
Молокосвертывающие ферменты растительного и животного происхождения известны человечеству очень давно, а в последние годы получили распространение бактериальные и грибковые препараты. Однако на заре сыроделия для получения сгустков из молока использовался преимущественно натуральный коагулянт — сычуг, полученный из желудков млекопитающих.
Следует отметить, что для приготовления сырных сгустков наряду с коровьим молоком используют молоко козы, овцы, буйвола, северного оленя, яка и ламы; востребованным оказывается также молоко нежвачных млекопитающих (верблюдицы, кобылы и ослицы). Эти виды молока для некоторых народов имеют большое питательное и экономическое значение. Несмотря на пригодность для производства не-ферментированных молочных продуктов молока верблюдицы, кобылы, ослицы, верблюжье молоко коагулирует под действием сычуга.
Тип образованного коагулята зависит от используемого фермента, баланса солей молока, рН, содержания в молоке других ингредиентов (жира, белков сыворотки) и состава самого казеина. Казеин, предварительно подвергнутый воздействию ферментов, не может формировать такой однородный сгусток, как нативный казеин. Сгусток, полученный при низком рН (4,6-5,0), характеризуется зернистой, колющейся и неэластичной структурой вследствие осаждения казеина в изоэлектрической точке растворимости или около нее. Коагулят, образующийся с помощью фермента при высоком рН (5,8-6,6), — более мягкий, гладкий, связанный и эластичный по сравнению с кислыми сгустками.
Несмотря на то что взаимодействия между отдельными компонентами молока достаточно сложны, субстратом, на который действует коагулирующий фермент (при наличии ионов кальция) с получением нерастворимого коагулята, включающего остальные компоненты молока (воду, жир, соли, белки), является казеин. Коагулят можно использовать как «сычужный сгусток молока», часто подслащенный и ароматизированный, но чтобы он стал сырной массой, из него следует удалить влагу/1/.
В настоящее время, в связи с дефицитом сычужного фермента из-за нецелесообразности забоя молодняка в молочный период жизни и снижения количества скота при резком возрастании его продуктивности, широко используются другие ферменты, близкие по действию к сычужному: пепсины, энзимы, продуцируемые некоторыми микроорганизмами.
Разработаны методы генной инженерии, позволяющие включать гены, осуществляющие синтез сычужного фермента, в геномы микроорганизмов, и тем самым осуществлять синтез сычужного энзима микроорганизмами. Сычужный фермент, полученный методами генной инженерии, уже вырабатывается и применяется в промышленных масштабах/2/.
1 НОМЕНКЛАТУРА .КЛАССИФИКАЦИЯ ФЕРМЕНТОВ
Для сыроделия пригодны энзимы, быстро разрывающие связь между гидрофобной и гидрофильной частями х-казеина и не оказывающие отрицательного влияния на выход и органолептические показатели сыров. Энзимы, удовлетворяющие этим требованиям, называются «молокосвертывающими ферментами», хотя слово «ферменты» не совсем удобно, поскольку на французском и английском языках оно означает «закваска», «дрожжи» или глагол «бродить». Ферменты в нашем понимании за рубежом называются энзимами.
Перечень нашедших достаточно широкое применение в сыроделии молокосвертывающих энзимов приведен в таблице 1.
Таблица 1 — Номенклатура и источники молокосвертывающих ферментов
| Название | Название (МКФ)* | Другие названия | Источники |
| Пепсии | Пепсин А (ЕС 3.4.23.1) | Пепсин II | Жвачные, цыплята, свиньи |
| Гастриксин** | Пепсин С (ЕС 3.4.23.3) | Пепсин I Парапепсин II Пепсин В | Жвачные, свиньи |
| Химозин | Химозин (ЕС 3.4.23.4) | Реннин | Жвачные |
| М.miehei протеиназа (ММР) | (ЕС 3.4.23.6) | Реннилаза (Nоѵd), Ха-нилаза(Сhr. Наnserі), Фромаза (Wa11еrstеm), Марзим (Міlеs) | Мисоr mіеhеі |
| М рusillus протеиназа (МРР) | (ЕС 3.4.23.6) | Емпораз(Dairуlаnd), Мейто(Меіtо Sаngо), Ноури (Ѵіtех) | Мucor рusillus ѵаr. Lіndt. |
| К.раrasitica протеиназа (ЕРР) | (ЕС 3.4.23.6) | Супарен (Рfizer) Сур Курд | Еndothia раrаsitіса |
* МКФ - Международная классификация энзимов (ферментов).
* * Гастриксин отличается от других пепсинов и химозина, поэтому он помещен в отдельную группу.
Молокосвертывающий энзим, доминирующий в четвертом отеле желудка телят в возрасте до 14 дней, до недавнего времени занимал господствующее положение в сыроделии. Он получил название «химозин» от греческого слова «сhуmе», означающего «желудочный сок». На английском языке его называют «реннин» (от «реннет» - сычуг). Международная номенклатура энзимов рекомендует для него название «химозин», потому что реннин легко спутать с названием другого энзима - «ренин», образующегося в почках.
В коммерческих экстрактах из сычугов молодняка млекопитающих, именуемых «сычужным ферментом», или, что правильнее, «сычужным порошком», кроме химозина содержатся другие энзимы, главным образом пепсины. В английском языке эти препараты называют «реннет». В соответствии с техническими условиями доля молокосвертывающей активности сычужного порошка за счет пепсинов не должна превышать 30% от его общей молокосвертывающей активности. Доля химозина в экстрактах из сычуга уменыыается с возрастом: в экстрактах сычугов коровы его содержится в семь раз меныпе, чем в экстрактах сычугов телят.
В связи с недостатком сычужного порошка в сыроделии начали широко применять другие препараты, которые можно разделить на две группы: пепсины — желудочные протеазы жвачных и некоторых других животных - и кислые протеазы микробиального происхождения. Из первой группы наиболыпее распространение получили говяжий, свиной и куриный пепсины. Пепсины чаще всего используют в, виде смесей друг с другом или с сычужным порошком. Из микробиальных молокосвертывающих энзимов получили достаточно широкое применение только некоторые протеазы (ММР, МРР и ЕРР), образуемые плесневыми грибами (табл. 1).
Все более широкое применение получают препараты рекомбинантного химозина, получаемые с помощью микроорганизмов. Химический состав, степень использования белка и жира молока, органолептические показатели сыров, вырабатываемых с препаратами обычного и микробиального химозина из Кіиуѵегошусез Іасгіз, Е. соіі и Азр. пі§егѵаг. а\ѵатогі, идентичны.
Молокосвертывающие энзимы в международной классификации энзимов помещены в одну группу ЕС 3.4.23, хотя плесневые протеазы сильно отличаются от молокосвертывающих энзимов животного происхождения по специфичности и структуре/2/.
Классификации МФП по природе происхождения ферментов, то есть сырье, из которого они производятся.По природе происхождения (используемому сырью) можно выделить следующие группы:
1. Ферменты животного происхождения;
2. Ферменты микробного происхождения;
3. Ферменты растительного происхождения /3/.
Следующим признаком может являться технология получения ферментов из исходного сырья. По этому признаку можно выделить следующие группы:
1. Технология экстракции или автолиза ферментов из сырья;
2. Технология контролируемой ферментации;
3. Технология рекомбинационной (геннонаправленной) ферментации. Третьим признаком должна быть методика нормализации молоко-свертывающих препаратов до товарного продукта по:
1. Ферментному составу;
2. Молокосвертывающей активности;
3. Наполнителям;
4. Консервантам и прочим добавкам/4/.
2 СВОЙСТВА МОЛОКОСВЕРТЫВАЮЩИХ ЭНЗИМОВ
Все молокосвертывающие энзимы, достаточно широко используемые и сыроделии, принадлежат к кислым протеазам, проявляющим максимальную активность в кислой среде. Они характеризуются высоким содержанием дикарбоновых аминокислот, низким содержанием основных аминокислот . Их еще называют аспарагиновыми протеазами, потому что в их активном центре имеются два остатка аспартата .Кислые протеазы содержат 325-360 аминокислотных остатков; молекулярная масса их находится в пределах 33000-38000. Молекулярные массы говяжьего химозина и свиного пепсина равны 35600 и 34600 соответственно.
Молокосвертывающие энзимы животного происхождения выделяются в виде проферментов, которые превращаются в активные энзимы путем отщепления от N-терминального конца ингибитора, содержащего около 45 аминокислотных остатков. Плесневые кислые протеазы образуются в активной форме. Активизацию проферментов инициируют водородные ионы. Активизация - процесс автокаталитический, протекает при рН 2,0-4,6. На молочные заводы препараты молокосвертывающих энзимов поступают в активной форме и концентрированном виде.
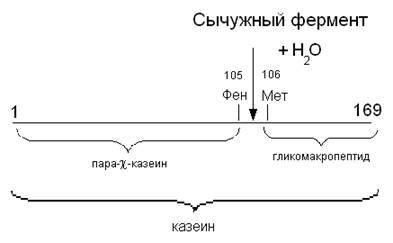
В природе нет энзимов, катализирующих разрыв только связи Феню5-Метюб в χ -казеине, но молокосвертывающие энзимы должны расщеплять эту связь во много раз быстрее, чем другие связи в протеинах молока, так как весь χ-казеин должен быть гидролизован молокосвертывающими энзимами во время выработки сыра, иначе не произойдет коагуляция казеина или значительная часть казеина останется в сыворотке. Любая другая протеолитическая активность молокосвертывающих энзимов во время выработки сыра нежелательна, так как растворимые продукты протеолиза остаются в сыворотке, что снижает выход сыра. По-видимому, теряется для сыра и макропептид, отделяемый от х-казеина в результате гидролиза молокосвертывающими энзимами, но с этим нужно мириться, так как без гидролиза χ-казеина сычужный сыр выработать нельзя.
Способность быстро гидролизовать χ-казеин - общее свойство молокосвертывающих энзимов, применяемых в сыроделии, - называют молокосвертывающей активностью, в отличие от способности расщеплять другие связи в белках, получившей название общей протеолитической активности. Общая протеолитическая активность молокосвертывающих энзимов по отношению к молокосвертывающей должна быть как можно более низкой.
Одна часть кристаллического химозина может свернуть 72 млн. частей молока при 35° С. Химозин гидролизует в χ-казеине связь Фен105 -Метюб в 200 раз быстрее, чем другие связи. Это обусловлено составом и последовательностью расположенных рядом с ней аминокислот. χ-Казеины женского и свиного молока вообще не содержат этой связи, но оба гидролизуются говяжьим химозином, хотя и медленнее, чем χ-казеин коровьего молока. По данным Foltmfn с соавт., говяжий химозин свертывает коровье молоко в два раза быстрее, чем свиное, а свиной химозин свертывает свиное молоко в шесть раз быстрее, чем коровье.
Молокосвертывающие энзимы существенно различаются по отношению общей протеолитической активности к молокосвертывающей. При оптимальном для каждого фермента рН и равной молокосвертывающей активности соотношение общей протеолитической активности (по гемоглобину) говяжьего химозина, говяжьего и свиного пепсина составило 1:3:6. На рис.1 показан гидролиз казеина некоторыми молокосвертывающими препаратами при рН 5,5, близком к рН созревающих сыров и содержимому желудка телят в молочный период. Неспецифический протеолиз (избыточный по отношению к химозину) после 3-часовой инкубации составил для свиного пепсина 0,275 мг, для говяжьего -0,10 мг, для смеси химозин + говяжий пепсин - 0,05 мг, что соответствовало 87,9; 30 и 12% к протеолизу под действием химозина. Химозин обладает самой низкой общей протеолитической активностью по отношению к молокосвертывающей активности.
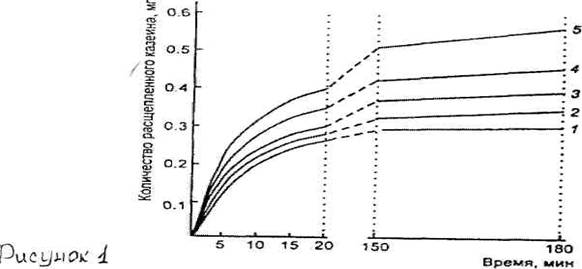
Рисунок 1. Сравнительиые данные по гидролизу казеина прирН 5,5 (/ -рентш; 2 -реннин + бычий пепсин (1:1); 3 - бычий пепсин-4 - решшн + свиной пепсин (!: 1); 5 - свиной пепсин)
Характер протеолиза в результате совместного действия молокосвертывающих энзимов и Lc. lactis svbsp. lactis зависит от вида энзима: если содержание растворимого белка, пептидов и свободных аминокислот в обезжиренном молоке с сычужным порошком после роста молочного лактококка принять за 100%, то оно будет равно соответственно: в молоке со свиным пепсином 41,1; 105,5; 22,8%; с куриным пепсином 45,2; 125 и 17,7%). При замене сычужного порошка пепсинами содержание растворимых белков и свободных аминокислот в результате кооперативного протеолиза уменьшилось, а содержание пептидов увеличилось. Появление горечи в сырах связано с накоплением в них специфических пептидов.
Следует отметить более высокую общую протеолитическую активность промышленных препаратов сычужного порошка по сравнению с кристаллическим химозином (рис. 2), что обусловлено наличием в первых не только химозина, но и пепсинов. После расщепления χ-казеина и свертывания молока кристаллическим химозином содержание продуктов протеолиза практически не увеличивается, тогда как при использовании сычужного порошка их накопление идет интенсивнее до свертывания и продолжается после свертывания.
Рисунок 2
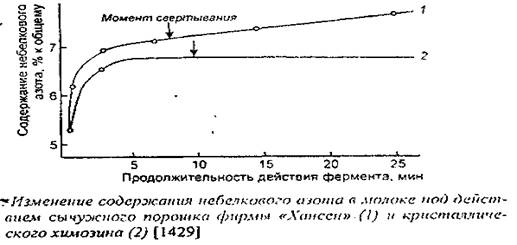
Более низкая общая протеолитическая активность химозина по сравнению с пепсинами имеет важное физиологическое значение, поскольку новорожденные в первый период жизни не имеют собственных защитных систем и нуждаются в нативных иммуноглобулинах молозива для защиты от инфекций.
Гидролиз других, чем χ -казеин, казенное молокосвертывающими энзимами протекает во время созревания сыров. Исключением являются твердые сыры с высокими температурами II нагревания и с плавлением сырной массы, во время выработки которых молокосвертывающие энзимы полностью или частично разрушаются. Участие молокосвертывающих энзимов в протеолизе во время созревания сыра необходимо для формирования органолептических показателей созревающих сыров, но количественные и/или качественные отклонения от нормального хода протеолиза вызывают пороки вкуса и консистенции. Под нормальным протеолизом в сыроделии понимают протеолиз под действием химозина при характерных для сыра условиях.
Более высокая общая протеолитическая активность молокосвертываюших энзимов по сравнению с химозином, как правило, оказывает отрицательное влияние на качество сыров, особенно с длительными сроками созревания. Например, потери молочного жира с сывороткой были выше, а плотность сгустка и качество сыра Чеддер ниже при использовании для свертывания молока пепсина вместо химозина. Однако сыры, вырабатываемые с кристаллическим химозином, имеют менее выраженный вкус и медленнее созревают, по сравнению с сырами, вырабатываемыми из этого же молока и по этой же технологии, но с сычужным порошком. Следовательно, общая протеолитическая активность молокосвертывающих энзимов в определенной степени необходима для получения сыров высокого качества.
Атака химозином χ-казеинов направлена на связи, включающие фенилаланин или лейцин. Первичная атака на χ-казеин направлена на связи Фен24-Фен25 или Фен24-Вал25 с образованием пептида άsl-І казеина. Дальнейший протеолиз может идти в растворе и сыре с последовательным образованием пептидов II, III, IV и так до XX. Под действием химозина и свиного пепсина из
άs-казеина образуется άsl пептид, но этот пептид далее расщепляется только химозином.
Гидролиз α- и β-казеинов идет с гораздо более низкой скоростью, чем χ-казеина, но благодаря длительности созревания и участия протеолитических энзимов микрофлоры закваски к концу созревания άsl -казеин и часть β-казеина бывают расщеплены. Пептиды, получающиеся в результате гидролиза казеинов молокосвертывающими энзимами, более доступны, чем исходный казеин, для протеолитических энзимов молочнокислой микрофлоры, которые играют главную роль в созревании твердых сыров. Участие в созревании, т.-е. в формировании характерных для сыров органолептических показателей, - вторая функция молокосвертывающих энзимов в сыроделии.
Из молокосвертывающих энзимов по общей протеолитинеской активности ближе всего к химозину стоит говяжий пепсин, свиной пепсин обладает более высокой общей протеолитической активностью; наименее пригоден для сыроделия куриный пепсин . Однако по другим данным, белый рассольный сыр, выработанный с цыплячьим пепсином или его смесью с реннетом, ничем не отличались от контрольных, выработанных только с реннетом, кроме более высокого содержания сухих веществ и общего азота.
Физико-химические факторы влияют как на скорость катализируемой реакции, так и на стабильность самого энзима, причем характер этого влияния на каждый процесс различается для разных энзимов. Протеолитическая активность энзимов в сырах может существенно отличаться от их активности в жидких средах. Так, сыры из молока, свернутого свиным пепсином, имеют удовлетворительные характеристики, потому что свиной энзим почти полностью инактивируется во время выработки сыров, и его высокая общая протеолитическая активность в сырах не реализуется .
Степень участия молокосвертывающих энзимов в созревании зависит от того, сколько их остается в сыре. Количество химозина, остающегося в сыре, увеличивается при снижении рН сыворотки и сырной массы.
Стабильность молокосвертывающих энзимов зависит от ионной силы среды, температуры, продолжительности выдержки и концентрации энзимов . Пепсин и химозин автолизируются при величине рН, оптимальной для их общей протеолитической активности. Плесневые протеиназы стабильны при рН до 2,5.
Общим свойством молокосвертывающих энзимов является снижение общей протеолитической активности при рН среды выше оптимального уровня. Одной из причин этого является инактивация энзимов при высоком рН. Скорость инактивации зависит от вида энзима (рис. 3). Так, говяжий пепсин начинает инактивироваться после 20-минутной выдержки только при рН выше 6,4, а при рН 7,0 сохраняет более трети исходной активности. В то же время свиной пепсин после 20-минутной выдержки при рН 6,4 теряет свыше 50% исходной активности, а при рН 7,0 почти моментально полностью инактивируется. Для свертывания молока с рН 6,6 за 5 мин, требуется одинаковая масса говяжьего и свиного пепсина, а при свертывании за 20 мин, свиного пепсина требуется в 2,5 раза болыне, чем говяжьего. Быстрая инактивация свиного пепсина в слабокислой среде, какой является молоко, является главным недостатком его как молокосвертывающего энзима.
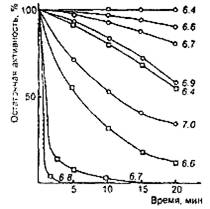
Зависимость устойчивости бычьего (о) и свиного (□) пепсина от рН при 35 ºС
Оптимальный рН для гидролиза χ-казеина химозином равен примерно 6,0, однако в интервале рН от 5,6 до 6,4 разница в скорости реакции невелика; активность снижается при рН выше 6,5 с несколько меньшей скоростью, чем для говяжьего пепсина (рис. 4). В интервале рН 6,6-6,7, характерном для молока в начале выработки сыра, скорость гидролиза χ-казеина химозином остается достаточно высокой. Куриный пепсин, гастриксин, фромаза стабильны в диапазоне рН, характерном для выработки и созревания сыра .
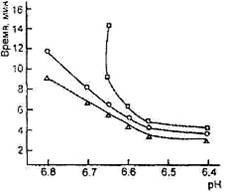
Зависимость моло-косвертывающей активности фер-ментов от рН (о- бычий пепсин, ∆'-реннин, □ - свиной пепсин)
Молокосвертывающие энзимы различаются по отношению к температуре. Изменение молокосвертывающей активности фромазы и сычужного порошка в зависимости от температуры показано на рис.4 (по материалам фирмы «Гист-Брокадес»). Отношение к температуре говяжьего пепсина почти такое же, как у сычужного порошка. В порядке возрастания устойчивости к нагреванию молокосвертывающие энзимы располагаются следующим образом: свиной пепсин, говяжий пепсин, химозин, фромаза и М. pusillus протеазы
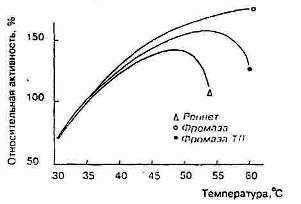
Рисунок 5 Влияние температуры на активность реписта и фромазы
Устойчивость к нагреванию понижается при повышении рН. Молокосвертывающая активность сычужного порошка максимальна при 45° С, чистого пепсина - при 35° С.(рис.5)
Желудочные протеазы млекопитающих показывают различную чувствительность к мочевине: пепсин к ней устойчив, химозин нет. Эти различия используют для их идентификации.
Обработка молока для выработки сыра 0,01-0,15% перекиси водорода повышает активность молокосвертывающих энзимов и микрофлоры закваски, увеличение дозы перекиси до 0,03-0,15% оказывает ингибирующее действие.
Исследования молокосвертывающей и общей протеолтичсскои активности показывают явное преимущество химозина перед другими молокосвертывающими энзимами. Отношение молокосвертывающей активности к общей протеолитической у химозина равно 40:9, а у говяжьего пепсина 4:3, что свидетельствует о высокой общей протеолитической активности пепсина, а следовательно, о большей опасности появления пороков в сырах, выработанных с пепсином /2/
Похожие работы
... для всех позиций порядке возрастания кодов. "Нулевые" группировки отмечены в конце наименования условным знаком "*". При необходимости отражения конкретных типов, марок, моделей и других характеристик отдельных видов продукции, в создаваемых для этих целей отраслевых классификаторах продукции в качестве первых шести знаков должны использоваться коды из настоящего Общероссийского классификатора ...
... разрезе ассортиментных групп по изготовителям представлены только белорусские производители. Руководителю торговой организации следует обратить внимание на правильность и четкость формирования торгового ассортимента сыров сычужных твердых. Следует дополнить ассортимент торговой группы по основным требованиям: развернутый, полный, оптимальный. Так же учитывать широту и новизну ассортимента. 2.2 ...
... А, Д, Е, В1, В2, В3, В6, РР, С. По калорийности сыры занимают среди продуктов питания одно из первых мест: 3580 – 3890 ккал на 1 кг. 1.4 Факторы, формирующие качество и сырье. Процессы производства Применение различных технологических схем производства дает возможность получить разнообразные по химическому составу и органолептическим показателям сыры. Процесс производства натуральных ...
... , при температуре не выше 10° С и относительной влажности не более 75%. 2.1.3.10 Вода питьевая В сыроделии используется вода питьевая по ГОСТ Р 51232-99. 2.1.4 Технологический процесс производства сычужного сыра “Российского нового” с использованием бактериальной закваски Поступающее на завод молоко насосом Н1 через воздухоотделитель ВО и счетчик С1 полают в промежуточные резервуары Р1. Из ...





0 комментариев