ТЮМЕНСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ.
Исполнитель: ВИЗГАЛОВ О.В.
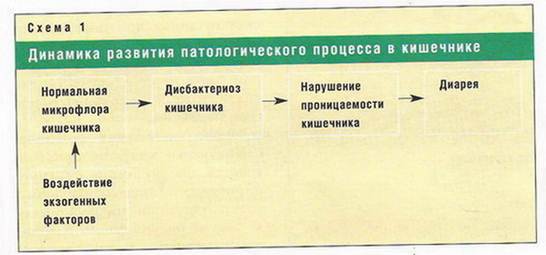
Дисбактериоз- это изменение количества и состава физиологически необходимой для организма микрофлоры. В результате нарушается пищеварение, ухудшается всасывание , что приводит к гиповитаминозу, анемии, снижению иммунитета, возникновению аллергических реакций организма.
Лактозная непереносимость: худшее, что может дать материнское молоко. Материнское молоко - драгоценная жидкость, дающая младенцу все самое необходимое и самое полезное. И на сегодняшний день большинство мам с удовольствием кормят своих малышей грудью. Но к великому сожалению, возможность вскормить младенца своим молоком предоставляется далеко не всем женщинам. И дело тут не в отсутствии молока, отказе крохи или болезни матери, а в том, что 18-20% новорожденных детей страдают от лактозной непереносимости.
Лактозная непереносимость, т.е. непереносимость молочного сахара, возникает у ребенка при наличии лактозной недостаточности (специального фермента в кишечнике).
В настоящее время непереносимость молочного сахара, содержащегося в материнском молоке, а в дальнейшем и в коровьем, встречается все чаще и чаще. У новорожденных обычно лактозная недостаточность начинается именно с материнского молока, потому что молочного сахара в женском молоке 7%, а в коровьем - в два раза меньше - 3,5%. Если в тонком кишечнике маленького ребенка не хватает фермента, который расщепляет молочный сахар (лактозу), то, вместо того чтобы расщепиться и всосаться в тонком кишечнике, он (молочный сахар) проходит в толстый кишечник, где его быть не должно (тем более в большом количестве). Попав в толстый кишечник, лактоза начинает бродить. У ребенка появляется пенистый стул, с пузырьками, зеленого цвета, потому что реакция кала становится кислой и имеет запах творога, кефира. В результате брожения образуются газы - у малыша расширяется кишечник, его пучит, его мучают боли, он кричит и отказывается от еды.
Непереносимость молочного сахара бывает двух видов: наследственно обусловленная и временная.
Наследственная непереносимость- это когда в семье кто-то не может пить молоко.
Второй вид лактозной непереносимости - временная. На сегодняшний день большое число детей рождаются недоношенными, а чем менее зрелый ребенок, тем более высок процент лактозной непереносимости. Кроме того, нормальных родов - 20%, а патология у матери во время беременности влияет на формирование ферментов у ребенка, еще находящегося в ее утробе. Такой вид лактозной непереносимости врачи называют транзиторной (временной), т.е. на период, пока у грудничка незрелый кишечник, он будет питаться специальными смесями. Постепенно все придет в норму.
Для питания детей и взрослых, страдающих лактозной непереносимостью, нужно молоко и молочные продукты, лишенные лактозы в результате брожения: кефир, мацони, йогурт. Западные ученые создали фермент, расщепляющий лактозу. В Голландии он носит название "керулак", в Израиле и Америке он называется "лактейд". Его применение очень удобно: капсула открывается и препарат дается непосредственно перед грудным кормлением или добавляется в молоко, и лактоза прекрасно расщепляется и всасывается. К сожалению, в России пока этот препарат не зарегистрирован и, если младенец страдает лактозной непереносимостью, матери приходится отказаться от кормления грудью, что, конечно, очень обидно.
Но зато сейчас на нашем рынке появились специальные смеси - заменители грудного молока, где молочный сахар заменен на другие моносахара, что избавляет и младенца и маму от мучений. Среди таких смесей "Хумана безлактозная", а фирма "Нестле" выпустила на рынок смесь "Аль 110", изготовленную на основе коровьего молока, но без лактозы. Вместо нее присутствует глюкоза, сахароза, фруктоза, поскольку дети, страдающие недостаточностью лактозы, не могут употреблять только молочный сахар, а обычный переносят легко.
Как выявить и отличить непереносимость лактозы у грудного ребенка и не спутать ее с кишечной инфекцией или дисбактериозом?
В Москве уже разработана специальная система определения сахара в кале. Если сахара в кале 0,025% - это нормально, а вот 1% и более - это уже непереносимость лактозы. Метод определения разработан и передан в лабораторию Филатовской больницы. Сейчас такие исследовательские лаборатории существуют еще в Чебоксарах и Грозном. А поскольку в родильном доме ребенок еще мало ест, то обычно первые проявления лактозной непереносимости наблюдаются именно дома: жидковатый зеленый стул, вздутия. И именно мама должна обратить на это внимание и своевременно обратиться к врачу. И если сданы анализы и дисбактериоз и кишечная инфекция у вашего ребенка не выявлены, надо обратиться в консультативную поликлинику при Филатовской больнице, где у малыша возьмут анализ непосредственно на содержание сахара в кале. [U1]
В Минздраве России проходит регистрацию бактериальный биопрепарат (эубиотик) Биококтейль "НК". В коктейль входят биологически активные пищевые экстракты из сои, свеклы, петрушки, укропа, чеснока и прополиса, которые благодаря оригинальной методике становятся стимулятором роста полезной для человека микрофлоры. Кроме того, в коктейле присутствует необходимая для нормального пищеварения - кишечная палочка М-17.
Биококтейль "НК" способен в достаточно короткий срок создать в кишечнике условия для активного размножения полезной для человека микрофлоры, что в свою очередь нормализует пищеварение, обеспечивая поступление в организм необходимых для его нормальной работы веществ.
Хронические болезни органов пищеварения относятся к числу наиболее часто встречающихся заболеваний детского возраста. Распространенность их в настоящее время превышает 100 на 1000 детского населения.
За последние 20 лет распространенность гастроэнтерологических заболеваний у детей выросла более чем на 30%. Причем, согласно материалам исследований, проведенных по унифицированной программе в Нижнем Новгороде, Москве, Иркутске, Новокузнецке, Ижевске, Уфе, Саратове, Ярославле, Минске, Киеве, Ташкенте, ее уровень не имеет существенных региональных особенностей.
Следует указать и на факт повышенной распространенности болезней органов пищеварения у детей в возрасте 5 – 6 и 9 – 12 лет, т.е. в периоды наиболее интенсивных морфофункциональных изменений в детском организме, когда вследствие неравномерного роста отдельных органов и систем возникает дезинтеграция роста. Установлено, что до 30% выявленных в эти возрастные периоды заболеваний являются ничем иным, как функциональными расстройствами, более половины из которых бесследно исчезают без какого-либо лечения. В то же время значительная часть функциональных нарушений при условии постоянного воздействия на ребенка факторов внешней среды прогрессирует и переходит в хронические болезни. Таким образом, указанные возрастные периоды с точки зрения формирования болезней органов пищеварения следует рассматривать как критические и необходимо учитывать при разработке профилактических программ.
Важна и такая особенность гастроэнтерологической патологии детского возраста, как сочетанный характер поражения системы пищеварения в 70 – 90% случаев. Это обосновывает необходимость всестороннего и комплексного обследования гастроэнтерологического больного, которое не может быть ограничено изучением какого-то одного органа желудочно-кишечного тракта (ЖКТ).
За последние 10 лет существенно возросла роль нервно-психического фактора в формировании патологии органов пищеварения. Психосоматический генез гастроэнтерологических болезней у детей прослеживается в той или иной степени у 40 – 50 % больных.
Среди факторов риска развития болезней органов пищеварения у детей большое значение имеют перенесенные и сопутствующие инфекционные и паразитарные заболевания. Сегодня ни у кого нет сомнений в связи хронического гепатита с вирусами гепатита А, В, С, D, Е; а заболеваний желчевыводящих путей, поджелудочной железы и кишечника с дизентерией, сальмонеллезом, гельминтозами, лямблиозом, дисбактериозом.
В связи с этим большой интерес представляют данные о роли Helicobacter pylori (H. pylori) в развитии и течении гастродуоденальной патологии, однако значение его в формировании патологических состояний продолжает дискутироваться [2 – 5]. Так, среди детей с хроническими заболеваниями желудка и двенадцатиперстной кишки инфицированность H. pylori составила до 81% при хроническом гастродуодените и 91 – 100% при деструктивных эрозивно-язвенных поражениях гастродуоденальной области [1].
Таким образом, имеются все основания рассматривать инфекционный фактор как специфический фактор риска формирования большинства гастроэнтерологических заболеваний детского возраста.
Особое место среди инфекционных факторов риска занимает кишечный дисбактериоз, значимость которого в формировании и развитии болезней, в том числе и органов пищеварения, следует считать несомненной. При дисбактериозе наблюдается снижение резистентности организма, что приводит к нарушению компенсаторных механизмов защиты и повреждению слизистой оболочки кишечной стенки. Следует заметить, что вероятность развития гастроэнтерологического заболевания особенно велика при сочетании дефицита бифидофлоры в кишечном содержимом со сниженной лизоцимной активностью пищеварительных секретов.
Одной из центральных проблем детской гастроэнтерологии является изучение механизмов хронизации патологического процесса, а также факторов, влияющих на характер течения болезни. Среди эндогенных факторов развития заболеваний желудка и двенадцатиперстной кишки важнейшее значение придается соотношению между агрессивными факторами, воздействующими на слизистую оболочку желудка и двенадцатиперстной кишки (уровень кислотной продукции, высокая протеолитическая активность, особенно за счет повышенного содержания пепсиногена А), и состоянием ее защитных элементов (характер и степень слизеобразования, в том числе обмен гликопротеидов и гликозаминогликанов, выработка простагландина Е2, бикарбонатов, секреторного иммуноглобулина А; кровоток в слизистой оболочке). Показано, например, что у больных с язвенной болезнью отмечается снижение в сравнении со здоровыми лицами индекса муцинообразования.
В последние годы получены новые данные о механизмах развития хронического гастродуоденита у детей. Установлено, что в детском возрасте патологический процесс не ограничивается желудком и, как правило, захватывает двенадцатиперстную кишку.
У детей дошкольного возраста хронический гастродуоденит нередко развивается на фоне аллергического воспаления слизистой оболочки. При этом выражена тканевая эозинофилия и значительно увеличено число клеток – продуцентов IgЕ. Исключение пищевых аллергенов из рациона питания заметно снижает местную продукцию IgЕ и одновременно уменьшает воспалительные изменения в слизистой оболочке .
У детей всех возрастных групп воспалительные изменения в фундальном отделе желудка встречаются реже и степень выраженности патологического процесса в нем значительно меньше, чем в антральном отделе. Сравнительная оценка морфологии слизистой оболочки в различные возрастные периоды показала нарастание частоты более тяжелых патологических изменений к подростковому возрасту. У подростков в 3 раза чаще наблюдается атрофический гастрит, появляются не встречающиеся у детей школьного возраста нарушения регенерации покровно-ямочного эпителия (дисплазия и метаплазия) [11]. Следует отметить, что у 2/3 подростков хронический гастродуоденит был диагностирован еще в детском возрасте и длительность заболевания превышала 3 – 5 лет.
Общепризнано, что болезни органов пищеварения возникают как результат взаимодействия генетических и средовых факторов. Роль семьи, микроэкологической среды в формировании фенотипа здоровья и болезни ребенка несомненны. Не меньшее значение в этом отношении имеет и макроэкология, т. е. среда обитания семьи, так как пищеварительная система в условиях неблагоприятной экологической обстановки нередко оказывается центральным органом-мишенью. Результаты специальных исследований показали, что экологически детерминированные формы хронической гастродуоденальной патологии у детей по частоте в 3 раза превышают таковую в “чистых”регионах. Неблагоприятная экология усугубляет наследственную предрасположенность, усиливает влияние отрицательных семейных факторов, что приводит к более частому возникновению и более тяжелому течению заболеваний органов пищеварения.
Очевидно, что ухудшение экологической обстановки, увеличение частоты аллергических заболеваний, режим повышенных нервно-психических нагрузок, испытываемых в дошкольных учреждениях и школах, малоподвижный образ жизни приводят к росту частоты заболеваний пищеварительного тракта. Кроме того, в последние годы у детей в 2,5 раза увеличился удельный вес тяжелых форм гастродуоденита и язвенной болезни. Множественные и хронические язвы регистрируются у 40,8% больных с этой патологией, 6,3% из них не поддаются консервативной терапии. Полной обратимости патоморфологических изменений слизистой оболочки желудка и двенадцатиперстной кишки удается достичь только у 18,5% больных детей. У 25 – 30%, несмотря на проведение комплексной терапии, отмечаются рецидивы заболеваний.
Таким образом, вопросы профилактики, ранней диагностики и лечения заболеваний органов пищеварения у детей в последние годы вышли за рамки собственно педиатрии и представляют собой сложную и большую медико-социальную проблему.
Принципы терапии заболеваний верхних отделов ЖКТ у детей
Лечение заболеваний органов пищеварения в детском возрасте относится к числу сложных, противоречивых и недостаточно изученных разделов педиатрии. Многогранность патогенетических механизмов повреждения ЖКТ, высокий риск хронизации и утяжеления заболевания диктуют необходимость проведения комплексной терапии болезней органов пищеварения у детей, учитывающей возможность сочетанного воздействия на общие и местные механизмы патологического процесса. Именно поэтому лечебный процесс должен складываться из двух основных этапов – лечения и вторичной профилактики – и осуществляться в течение достаточно длительного времени с учетом при этом особенностей растущего организма в целом и эволюции гастроэнтерологических заболеваний у детей в частности.
Перечисленные проблемы, а также значительное число лекарственных средств, имеющихся в арсенале врача в настоящее время, ставят педиатров перед нелегким выбором оптимального варианта лечения.
Основу комплексной терапии гастроэнтерологических заболеваний у детей составляют:
•режим, создание физического и психического покоя;
•диета;
•медикаментозные и немедикаментозные средства;
•санаторно-курортное лечение;
•диспансерное наблюдение.
В каждом конкретном случае перед врачом стоит задача выбора рациональной программы терапии с учетом не только этиологии и патогенеза гастроэнтерологического заболевания, но и множества других аспектов: возраста ребенка, особенностей его режима и диеты, психоэмоционального состояния, сопутствующих заболеваний и т. д. Особое значение в детском возрасте приобретают такие факторы, как функциональное состояние центральной нервной системы, характер и темпы формирования нейроэндокринной регуляции. Кроме того, сочетанный характер гастроэнтерологических заболеваний создает немалые трудности при выборе лечебных средств. Наряду с этиотропной и патогенетической терапией посиндромное лечение занимает важное место в детской гастроэнтерологии.
Режим
В период обострения болезни надо создать для ребенка режим физического и психического покоя. Необходимо определить рациональный режим сна и бодрствования, включая обязательный дневной отдых. Важно уменьшить психоэмоциональные нагрузки. Для снятия у больных эмоциональной напряженности, страха, бессонницы в гастроэнтерологии нашли обоснованное применение седативные фитосборы (настойки и отвары валерианы, пустырника, пиона, пассифлоры) и некоторые транквилизаторы (диазепам, хлордиазепоксид, медазепам). У детей старшего возраста возможно использование психотерапевтических методов. Вопрос о стационарном лечении ребенка в период обострения заболевания необходимо решать строго индивидуально, исходя из конкретной медицинской, семейно-бытовой, социальной и психоэмоциональной ситуации.
Диета
Лечебное питание при заболеваниях органов пищеварения является основой комплексной терапии. Оно должно быть физиологическим, полноценным и сбалансированным по набору основных ингредиентов и одновременно воздействовать на патогенетические механизмы заболевания. Диета в период обострения строится на принципах использования антацидных свойств пищи, механического, химического, термического щажения слизистой оболочки верхних отделов ЖКТ, дробности питания (не менее 4 – 6 раз в день).
В зависимости от уровня и глубины поражения ЖКТ используют различные виды диет, отличающиеся по степени кулинарной обработки, составу основных продуктов и количеству пищевых ингредиентов. Соблюдая принцип щажения, тем не менее нельзя допускать необоснованно длительного ограничения в употреблении тех или иных пищевых продуктов, при возможности необходимо расширять диету.
Медикаментозное лечение
Антисекреторные средства. Антисекреторным средствам принадлежит приоритет среди других препаратов, применяющихся при лечении заболеваний гастродуоденальной зоны пищеварительного тракта. Однако, несмотря на многочисленные исследования процессов кислото- и ферментообразования при гастроэнтерологической патологии, а также изучение соотношения факторов агрессии и защиты, до настоящего времени единого мнения о широком применении антисекреторных препаратов у детей нет.
Антисекреторные средства, применяемые в гастроэнтерологии, способны воздействовать на механизмы секреции практически на всех этапах. Так, блокаторы H2-рецепторов гистамина взаимодействуют с рецепторами гистамина и прекращают секреторный ответ на самом начальном его этапе. Холинолитики блокируют рецепторы ацетилхолина на поверхности клеточной мембраны и тоже воздействуют на пусковые механизмы секреции. В последние годы активно изучаются также блокаторы рецепторов гастрина. На этапе трансдукции воздействуют антагонисты кальция, простагландины, опиоиды, блокирующие передачу рецепторного сигнала в области париетальной клетки. На этапе секреции Н+ эффекторными механизмами клетки отчетливое антисекреторное действие проявляют ингибиторы карбоангидразы. Ингибиторы протонной помпы, препятствующие подаче активного иона водорода в желудочный секрет, действуют на конечный этап секреторного процесса в париетальной клетке.
В полости желудка нейтрализующее действие в отношении желудочного содержимого оказывают антацидные препараты. Они не относятся к истинно антисекреторным средствам, но благодаря выраженному влиянию на кислотно-пептическую активность желудочного содержимого не потеряли своего былого значения в терапии гастродуоденальных заболеваний. Более того, в последние годы эти препараты привлекают пристальное внимание врачей как средства базисной терапии.
В настоящее время в детской гастроэнтерологии наиболее часто используют следующие группы антисекреторных препаратов:
•блокаторы Н2-рецепторов гистамина; синтезировано пять поколений препаратов этой группы, из которых первые три уже заняли прочное место в лечении заболеваний желудка и двенадцатиперстной кишки: циметидин, ранитидин, фамотидин; •селективные блокаторы М1-холинорецепторов: пирензепин; •блокаторы Н+, К+ - АТФазы (ингибиторы протонной помпы), наиболее мощные ингибиторы желудочной секреции: омепразол.
Необходимо также упомянуть и об антисекреторных препаратах других групп. Антисекреторным свойством обладают простагландины Е и А, но их эффект проявляется только в больших дозах. В терапии также используются синтетические аналоги простагландинов (энпростил). В последние годы в литературе появились сведения об антисекреторном действии антагонистов кальция (верапамил, нифедипин). На этапе трансдукции возможно также торможение аденилатциклазной активности клетки эндогенными опиоидами. Синтетический препарат даларгин, активирующий периферические опиоидные рецепторы, уже использовался в педиатрии для лечения язвенной болезни двенадцатиперстной кишки. Хорошо известен антисекреторный эффект ингибиторов карбоангидразы (ацетазоламида). В последние годы особый интерес гастроэнтерологов вызывает синтетический аналог соматостатина – октреотид, однако опыт его применения в детской клинике пока невелик.
Следует отметить, что педиатры-гастроэнтерологи с осторожностью относятся к длительному назначению антисекреторных средств в связи с их выраженными побочными проявлениями, в частности с так называемым синдромом рикошета, который может развиться после отмены препарата.
Антацидные препараты. К антацидам относят ряд соединений, которые взаимодействуют в желудке с соляной кислотой, инактивируя ее. Основными фармакологическими эффектами данной группы препаратов является способность снижать протеолитические свойства желудочного сока, уменьшать прямое раздражающее действие соляной кислоты на слизистую желудка, повышать внутрижелудочную рН до 4,0 – 5,0. Всасывающиеся антациды в клинической практике применяют редко, так как они дают много побочных эффектов. Невсасывающиеся антациды разнообразны по своему составу. Наиболее часто применяются Al/Mg-содержащие антациды: маалокс, альмагель и др. Они обладают нейтрализующими свойствами, адсорбируют соляную кислоту и образуют с ней буферные соединения. Имеются комбинации невсасывающихся антацидов с обволакивающими и адсорбирующими свойствами (подробнее об этой группе препаратов см. ниже).
Антипептические препараты. Протеолитические ферменты играют немаловажную роль в патогенезе заболеваний желудка и двенадцатиперстной кишки. Протеазы пепсиногенов при усиленном кислотообразовании трансформируются в активные пепсины. Поэтому патогенетически обоснованным является использование антипептических средств, способных тормозить протеолитический эффект ферментов желудка. Некоторые антацидные препараты обладают и антипептическими свойствами (висмута субцитрат, альфогель, анацид). Однако существуют препараты преимущественно антипептической направленности: сукральфат, депепсин .
Антигеликобактериальные средства. Как уже упоминалось, представления об этиопатогенезе хронических заболеваний желудка и двенадцатиперстной кишки значительно изменились после открытия H. pylori, однако роль и место H. pylori в патогенезе этих заболеваний остаются до конца не выясненными. Установлено, что нарушение равновесия между факторами агрессии и защиты, являясь основным звеном патогенеза, приводит к изменению морфофункционального состояния слизистой оболочки желудка и двенадцатиперстной кишки, вызывая ее метаплазию, а H. pylori либо непосредственно, либо запуская аутоиммунные механизмы приводит к развитию воспаления, а в некоторых случаях и к образованию язвенного дефекта.
Антигеликобактериальная терапия показана детям с хроническим гастритом и гастродуоденитом при условии обнаружения у них H. pylori, а также всем детям с эрозивно-язвенным поражением слизистой оболочки верхних отделов ЖКТ. С этой целью используют препараты висмута, полусинтетические пенициллины (оксациллин, амоксициллин), макролиды нового поколения (кларитромицин, азитромицин, роскситромицин), а также метронидазол. Данные литературы [18] свидетельствуют о быстром формировании устойчивости H. pylori к часто используемым антибактериальным препаратам, поэтому в настоящее время идет поиск новых, более эффективных в отношении H. pylori лекарственных средств, а также способов их сочетанного применения (двух- и трехкомпонентные схемы лечения).
Цитопротекторы. Препараты, защищающие слизистую оболочку гастродуоденальной зоны и получившие название цитопротекторов, находят все большее применение при заболеваниях желудка и двенадцатиперстной кишки. К эндогенным цитопротекторным факторам ЖКТ относят секрецию бикарбонатов эпителиальными клетками, состояние регенерации клеток и кровоток в слизистой оболочке.
Цитопротекторы подразделяют на две группы: пленкообразующие (препараты висмута) и простагландины (мизопростол).
Цитопротективной активностью обладает ряд лекарственных средств, оказывающих и другие воздействия (маалокс, сукральфат и др.).
Репаранты. Лекарственные средства, улучшающие процессы регенерации и получившие название “репаранты”, относятся к различным фармакологическим группам: стимуляторы муцинообразования (алантон), биогенные вещества (хлорид карнитина) и др. Кроме того, многие препараты, используемые в качестве базисной терапии при лечении органов пищеварения, оказались способными корригировать процессы репаративной регенерации. Это – холинолитики, блокаторы Н2-рецепторов гистамина, цитопротекторы и др. Необходимость назначения средств, улучшающих регенерацию и метаболизм, обусловливается затяжным течением гастроэнтерологических заболеваний, выраженными нарушениями обмена веществ и местного иммунитета.
Спазмолитические средства применяются в комплексной терапии заболеваний органов пищеварения, главным образом в период обострения, когда необходимо купировать болевой синдром, возникающий вследствие спазма гладкой мускулатуры ЖКТ. Обычно используют производные изохинолина (папаверин, но-шпа), сложных эфиров карбоновых кислот (ганглерон), а также препараты растительного происхождения (комбинированные препараты с экстрактом красавки). Назначение спазмолитиков должно тщательно контролироваться, так как они могут нивелировать клиническую картину абдоминального синдрома.
Прокинетики – препараты, регулирующие моторную функцию ЖКТ. В отечественной литературе до недавнего времени им уделялось явно недостаточное внимание. Хотя многие лекарственные средства, применяемые в гастроэнтерологиии, например антациды, холинолитики и др., обладают способностью нормализовать желудочную и кишечную моторику, избирательными регуляторами являются по существу антагонисты дофамина: метоклопрамид, домперидон, сульпирид и стимуляторы высвобождения ацетилхолина, в частности цизаприд.
Ферментные препараты. Лекарственные средства, содержащие энзимы, широко используются как при заболеваниях поджелудочной железы, так и при различных нарушениях пищеварения, возникающих у детей с патологией ЖКТ. Правильно подобранный препарат и его доза довольно быстро приводят к улучшению состояния больных. Различают препараты:
•содержащие экстракты слизистой оболочки желудка (пепсин, абомин, мукоза); •содержащие панкреатические ферменты (панкреатин, ораза, панкреалипаза); •содержащие панкреатин и панкреатические ферменты, компоненты желчи и гемицеллюлозу (дигистал, фестал, энзистал, дигистекс); •содержащие панкреатин и другие ингредиенты (панзинорм).
Желчегонные средства. Препараты этой группы применяются при болезнях желчевыводящих путей, а также при сочетанных поражениях поджелудочной железы, желудка и кишечника. Средства этой фармакологической группы отличаются разнообразием действия, составом и показаниями к использованию. Условно их подразделяют на препараты, стимулирующие желчеобразование (холеретики) и стимулирующие желчевыделение (холекинетики). Некоторые лекарственные препараты сочетают различные механизмы действия. Отношение к желчегонным средствам в настоящее время неоднозначное. В детской гастроэнтерологии наиболее оправдано применение желчегонных препаратов сочетанного действия и растительного происхождения: фламина, экстракта кукурузных рыльцев, осалмида, холафлукса.
Холелитолитические средства. Изменениям биохимизма желчи придается существенное значение в патогенезе заболеваний гепатобилиарной системы, в частности желчнокаменной болезни. В перенасыщенной, т.е. литогенной, желчи создаются условия для образования камней. В целях предотвращения камнеобразования в комплексной терапии используют препараты, влияющие на литогенность желчи (лиобил, олиметин, ментол), а также холелитолитические средства, способствующие растворению уже имеющихся конкрементов (препараты урсо- и хенодеоксихоловой кислоты).
Препараты гепатопротективного действия. Печень является органом, в котором интегрированы все важнейшие химико-биологические процессы, необходимые для поддержания гомеостаза. При заболеваниях печени, а также при сочетанных заболеваниях органов гепатобилиарной зоны ЖКТ клетки печени испытывают особое патологическое воздействие. Поэтому назначение гепатопротекторов, препаратов, обладающих способностью стабилизировать мембраны гепатоцитов (эссенциальные фосфолипиды, препараты с экстрактом печени, растительные средства, липоевая кислота), становится патогенетически обоснованным.
Не медикаментозные методы лечения
В комплексной терапии заболеваний верхних отделов ЖКТ лекарственные препараты, безусловно, занимают важное место. Однако не медикаментозные методы лечения продолжают широко использоваться в детской гастроэнтерологии.
Физиотерапевтическое лечение в острый период может включать лечение лазером, индуктотермию, озокеритовые или парафиновые аппликации, электрофорез с лекарственными средствами, светолечение, иглорефлексотерапию, гипербарическую оксигенацию. В период неполной и полной ремиссии дополнительно могут использоваться грязелечение, гидротерапия, лечебная физкультура. У подростков оправдано применение психотерапии, аутогенной тренировки.
Санаторно-курортное лечение показано в период ремиссии, спустя 3 мес после периода обострения. Рекомендуются местные санатории или бальнеологические курорты.
Диспансерное наблюдение при гастроэнтерологических заболеваниях подразумевает активное выявление больных на ранних стадиях болезни, наблюдение за ними, проведение лечебно-профилактических и социальных мероприятий с целью предотвращения рецидивов и осложнений. Правильно выбранная тактика, индивидуальный подход и противорецидивное лечение предупреждают прогрессирование патологического процесса.
В настоящее время к наиболее распространенным средствам поддержания баланса кишечной микрофлоры на оптимальном уровне и ее коррекции относятся пробиотики. Это вещества микробного или немикробного происхождения, оказывающие при естественном способе введения благоприятное действие на гомеостаз посредством нормализации баланса микрофлоры в организме хозяина. В странах СНГ наряду с термином “пробиотики” широко используют в качестве его синонима термин “эубиотики” — фармакопейные бактерийные препараты из живых микроорганизмов, предназначенные для коррекции микрофлоры хозяина. Однако по своей сути эубиотики, согласно современным представлениям, следует рассматривать как разновидность пробиотиков, и в зарубежной литературе термин “эубиотики” не используется.
В зависимости от природы составляющих компонентов и формы использования, можно выделить следующие основные группы пробиотиков:
препараты, содержащие живые микроорганизмы (монокультуры или их комплексы); препараты, содержащие структурные компоненты микроорганизмов — представителей нормальной микрофлоры или их метаболитов; препараты микробного или иного происхождения, стимулирующие рост и активность микроорганизмов — представителей нормальной микрофлоры; препараты, представляющие собой комплекс живых микроорганизмов, их структурных компонентов и метаболитов в различных сочетаниях, а также соединений, стимулирующих рост представителей нормальной микрофлоры; препараты на основе живых генно-инженерных штаммов микроорганизмов, их структурных компонентов и метаболитов с заданными характеристиками; продукты функционального питания на основе живых микроорганизмов, их метаболитов, других соединений микробного, растительного или животного происхождения, способных поддерживать и восстанавливать здоровье посредством коррекции микробной экологии организма хозяина.
Пробиотики на основе компонентов микробных клеток или метаболитов реализуют свое положительное влияние на гомеостаз непосредственно влияя на метаболическую активность клеток соответствующих органов и тканей или опосредованно — регулируя активность микрофлоры на слизистой оболочке кишечника.
Пробиотики используют в медицинской практике в виде различных лекарственных форм. Разработаны дозы и схемы их применения с профилактической целью при различных заболеваниях и патологических состояниях.
Эффективность лечения дисбактериоза определяется правильным выбором препарата-пробиотика (в случаях, когда чужеродные микроорганизмы обнаруживаются в кишечнике в небольшом количестве) или комбинацией пробиотика и антибактериального препарата. К препаратам выбора при этой патологии можно в полной мере отнести ХИЛАК® (ХИЛАК® ФОРТЕ), производимый компанией “Меркле” (Германия). Капли для приема внутрь во флаконах по 30 и 100 мл содержат стерильный концентрат продуктов обмена веществ бактерий, образующих молочную кислоту, продукты обмена веществ граммположительных и граммотрицательных симбионтов тонкой и толстой кишок (ХИЛАК® ФОРТЕ), биологическую молочную кислоту, молочные буферные соли, лактозу, аминокислоты летучие жирные кислоты с короткой цепью; 1 капля препарата соответствует биосинтетическим активным веществам 100 млрд. микроорганизмов.
ХИЛАК® способствует восстановлению нормальной микрофлоры кишечника биологическим путем, вызывая сдвиг и поддержание значений рН в пищеварительном тракте в границах физиологической нормы, что создает неблагоприятные условия для жизнедеятельности патогенных микроорганизмов, обеспечивает санацию кишечника. На фоне ускорения развития нормальных симбионтов кишечника под действием препарата нормализуется естественный синтез витаминов группы В и К, улучшаются физиологические функции слизистой оболочки пищеварительного тракта. Содержащиеся в препарате летучие жирные кислоты с короткой цепью обеспечивают восстановление нарушенного баланса микрофлоры кишечника при инфекционных заболеваниях пищеварительного тракта, стимулируют репарацию кишечного эпителия, восстанавливают нарушенный водно-электролитный баланс в просвете кишечника.
Все вышеперечисленные свойства позволяют рекомендовать ХИЛАК® при нарушениях биоценоза кишечника во время и после лечения антибиотиками, сульфаниламидами, лучевой терапии; при синдромах мальабсорбции и мальдигестии, диарее, метеоризме, запоре; гастроэнтерите, колите; гипо- и анацидных состояниях (в том числе во время беременности); энтерогенных заболеваниях желчного пузыря и печени; кожно-аллергических заболеваниях, в частности экземе, крапивнице (в составе комбинированной терапии), а также в период реконвалесценции после перенесенного сальмонеллеза (в том числе для долечивания детей грудного возраста). ХИЛАК® можно применять у детей, начиная с 1-го дня жизни, а также у женщин в период беременности и кормления грудью.21:50.
Список литературы
1. Баранов А. А., Климанская Е. В. Актуальные проблемы детской гастроэнтерологии // Педиатрия. – 1995 – №5. – с. 48–51.
2. Салмова В. С., Филин В. А., Трифонова И. В. и др. Роль геликобактериоза при гастродуоденальной патологии у детей./ Педиатрия, №1 1994, с. 13–15 .
3. Сапожников В. Г., Куклина Н. А. Об этиопатогенетической роли пилорического геликобактера в развитии заболеваний желудочно-кишечного тракта // Педиатрия, № 1, 1997, с. 67–72.
4. Щербаков П. Л., Филин В. А., Мазурин А. В. и др. Актуальные проблемы пилорического геликобактериоза на современном этапе // Педиатрия, № 1 ,1997, с. 7–12.
5. Аруин Л. И., Григорьев П. Я, Исаков В. А и др. Хронический гастрит. Амстердам, 1993, 362 с.
6. Практические вопросы детской гастроэнтерологии Санкт-Петербурга. (Сборник лекций и научных работ) / Под ред. проф. В. Л. Пайкова, С.-Петербург, 1996, 185 с.
7. Заболевания органов пищеварения у детей / Под ред. А.А.Баранова. – М., 1996. – 304 с.
8. Мазурин А. В., Филин В. А., Цветкова Л. Н. Современные представления о патологии верхних отделов желудочно-кишечного тракта у детей // Педиатрия, № 1, 1997, с. 5–7.
9. Балаболкин И. И. Гастроинтестинальная пищевая аллергия у детей // Педиатрия. № 1, 1997, с. 32–36.
10. Справочник по детской гастроэнтерологии / Под ред. А. М. Запруднова, А. И. Волкова. – М.: Медицина, 1995. – 384 с.
11. Запруднов А. М. “Новые болезни” в детской гастроэнтерологии // Педиатрия, № 1.1995. c. 77–81.
12.Закономерный А. Г. Современные клинико-эпидемиологические особенности язвенной болезни в детском возрасте и подходы к этапному лечению больных: Автореф. дис. ... докт. мед. наук. – М.,1992.
13. Фитотерапия в детской гастроэнтерологии . Из серии “В помощь практическому врачу”. Вып., 4, М.,1991,85 с.
14. Запруднов А. М. Лекарственные средства в гастроэнтерологии. М.,1996. – 123 с.
15. Гребенев А. Л., Шептулин А. А. Современные принципы антацидной терапии. // Клиническая медицина, №3, 1993, с. 12–5.
16. “Маалокс” в клинической практике. /Под ред. проф. О. Н. Минушкина, М., 1996, 80 с.
17. Шептулин А. А. Маалокс. // Клиническая фармакология и терапия, № 2, 1993, с. 68–9.
18. Бушуев С. Л., Зайцева О. В., Намазова О. С. и др. Применение препарата Maalox в комплексном лечении детей с заболеваниями желудочно-кишечного тракта // Педиатрия, № 1, 1997, с. 52-7.
Похожие работы
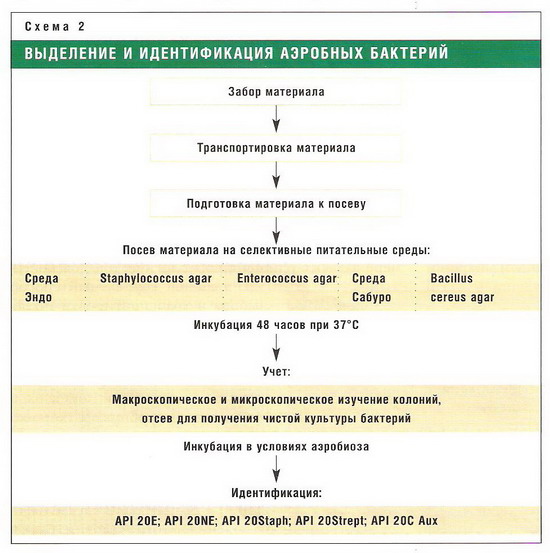
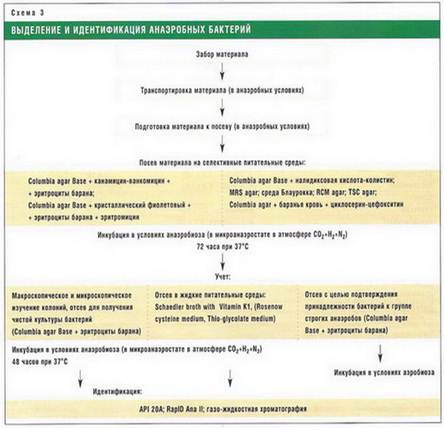
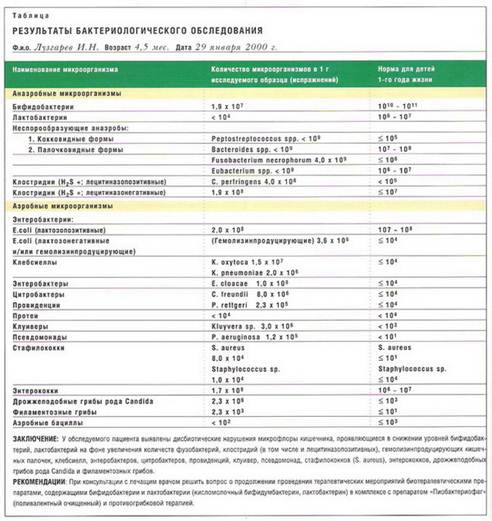
... а также соответствующую диету. Второй этап. У пациентов с измененными показателями ММПФ проводят детальное бактериологическое исследование фекалий и определяют микробиологические критерии дисбактериоза кишечника. Оценивают степень тяжести, выраженность микроэкологического дисбаланса и анализируют его фазы и формы. На основании данных биохимического и бактериологического исследования подбирают ...
... функционирование ее составных частей – организма человека, его микрофлоры и окружающей среды, а также механизмов их взаимодействия, в результате чего развивается заболевание. 2. Понятие дисбактериоза. Дисбактериоз кишечника отражает состояние бактериальных форм представителей микрофлоры при ее существенных и стойких нарушениях. Его следует рассматривать как симптомокомплекс, но не как ...
... нарушением процессов переваривания пищевых веществ в кишечнике (диспепсии кишечные, хронические гастриты с секреторной недостаточностью, хронические панкреатиты, энтериты, колиты и т. д. ). Причиной кишечного дисбактериоза может быть длительный, неконтролируемый прием антибиотиков, особенно широкого спектра действия, подавляющих нормальную кишечную флору и способствующих развитию тех ...
Препараты, применяемые для лечения дисбактериоза кишечника, относятся к группе [А07] "Противодиарейные, кишечные противовоспалительные и противомикробные препараты" по АТС-классификации ВОЗ (Anatomical Therapeutic Chemical classification Index with Defind Daily Doses) (табл. 1). Лекарственную терапию при дисбактериозе кишечника начинают с назначения одного из бифидосодержащих средств, ...
0 комментариев